-
钨 具有很大的工业价值,主要用于电子工业,合金添加剂等。工业上利用白钨矿精矿为原料
具有很大的工业价值,主要用于电子工业,合金添加剂等。工业上利用白钨矿精矿为原料 主要成分为钨酸钙
主要成分为钨酸钙 ,还含有CaO、
,还含有CaO、 等杂质
等杂质 生产钨粉的一种工艺流程如下:
生产钨粉的一种工艺流程如下:

已知:
 钨酸钙微溶于水,能溶解在热盐酸中。
钨酸钙微溶于水,能溶解在热盐酸中。
 降低溶液pH可以从钨酸铵溶液中析出仲钨酸铵晶体,常温时可析出带11个结晶水的仲钨酸铵晶体,但是由于颗粒很细小,难以进一步提纯。在
降低溶液pH可以从钨酸铵溶液中析出仲钨酸铵晶体,常温时可析出带11个结晶水的仲钨酸铵晶体,但是由于颗粒很细小,难以进一步提纯。在 时可析出颗粒较大的带5个结晶水的仲钨酸铵晶体,可进一步提纯精制。
时可析出颗粒较大的带5个结晶水的仲钨酸铵晶体,可进一步提纯精制。
 酸浸时为了提高浸出率,可采取的措施有___________。
酸浸时为了提高浸出率,可采取的措施有___________。 答出两条即可
答出两条即可
 酸浸时,需控制反应温度在
酸浸时,需控制反应温度在 之间的原因是________。
之间的原因是________。
 酸浸时发生的主要反应的化学方程式是____。
酸浸时发生的主要反应的化学方程式是____。
 将废酸与粗钨酸分离的操作是_____
将废酸与粗钨酸分离的操作是_____ 填操作名称
填操作名称 。
。
 加入过量氨水后过滤,得到滤渣的主要成分是______
加入过量氨水后过滤,得到滤渣的主要成分是______ 填化学式
填化学式 。
。
 工艺流程中“结晶析出”,采用的结晶方法是________。
工艺流程中“结晶析出”,采用的结晶方法是________。
 仲钨酸铵的化学式为
仲钨酸铵的化学式为 ,写出仲钨酸铵煅烧转化为
,写出仲钨酸铵煅烧转化为 的化学方程式_______________。
的化学方程式_______________。
 已知白钨矿精矿中的钨酸钙质量分数为
已知白钨矿精矿中的钨酸钙质量分数为 ,
, 该精矿经上述流程制得
该精矿经上述流程制得 钨粉。则该生产中钨的产率为_______
钨粉。则该生产中钨的产率为_______ 用含“a”“w”“m”的代数式表示
用含“a”“w”“m”的代数式表示 。
。
-
我国是世界上最大的钨储藏国,金属钨可用于制造灯丝、合金钢和光学仪器,有“光明使者”的美誉;现以白钨矿(主要成分为CaWO4,还含有二氧化硅、氧化铁等杂质)为原料冶炼高纯度金属钨,工业流程如下:
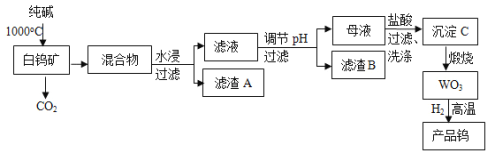
已知:①钨酸酸性很弱,难溶于水;
②完全沉淀离子的pH值:SiO32-为8,WO42-为5;
③碳和金属钨在高温下会反应生成碳化钨。
回答下列问题:
(1)工业上生产纯碱常先制得碳酸氢钠,此法叫“联碱法”,为我国化工专家侯德榜创立,即向饱和食盐水中先通入NH3,再通入CO2,最终生成碳酸氢钠晶体和氯化铵溶液,写出该化学反应方程式:____________。
(2)流程中白钨矿CaWO4和纯碱发生的化学反应方程式是:________________________。
(3)滤渣B的主要成分是(写化学式)______。调节pH可选用的试剂是:_____(填选项)。
A.氨水 B.盐酸 C.NaOH溶液 D.Na2CO3溶液
(4)检验沉淀C是否洗涤干净的操作是________________________________________。
(5)为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而必须用氢气作还原剂的原因是_________。
(6)将氢氧化钙加入钨酸钠碱性溶液中可得到钨酸钙,已知某温度时,Ksp(CaWO4)=1×10-10,Ksp[Ca(OH)2]=4×10-7,当溶液中WO42-恰好沉淀完全(离子浓度等于10-5mol/L)时,溶液中c(OH-)=_____。
-
我国是世界上最大的钨储藏国,金属钨可用于制造灯丝、合金钢和光学仪器,有“光明使者”的美誉,现以白钨矿(主要成分为CaWO4,还含有二氧化硅、氧化铁等杂质)为原料冶炼高纯度金属钨,工业流程如图:
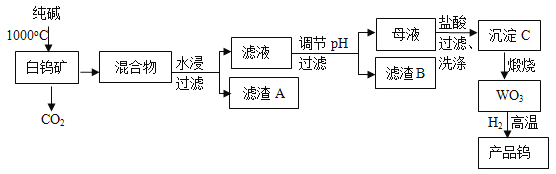
已知:①钨酸酸性很弱,难溶于水;
②完全沉淀离子的pH值:SiO32﹣为8,WO42﹣为5;
③碳和金属钨在高温下会反应生成碳化钨。
回答下列问题:
(1)工业上生产纯碱常先制得碳酸氢钠,此法叫“联碱法”,为我国化工专家侯德榜创立,即向饱和食盐水中先通入NH3,再通入CO2,最终生成碳酸氢钠晶体和氯化铵溶液,写出该化学反应方程式:____。
(2)流程中白钨矿CaWO4和纯碱发生的化学反应方程式是:____。
(3)滤渣B的主要成分是(写化学式)___。调节pH可选用的试剂是:__(填选项)。
A.氨水 B.盐酸 C.NaOH溶液 D.Na2CO3溶液
(4)检验沉淀C已经洗涤干净的操作是____。
(5)为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而必须用氢气作还原剂的原因是:___。
(6)将氢氧化钙加入钨酸钠碱性溶液中可得到钨酸钙,已知某温度时,Ksp(CaWO4)=1×10﹣10,Ksp[Ca(OH)2]=4×10﹣7,当溶液中WO42﹣恰好沉淀完全(离子浓度等于10﹣5mol/L)时,溶液中c(OH﹣)=____。
-
钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,钨在自然界主要以钨(VI) 酸盐的形式存在。有开采价值的钨矿石之一白钨矿的主要成分是CaWO4 ,含有二氧化硅、氧化铁等杂质,工业冶炼钨流程如下:
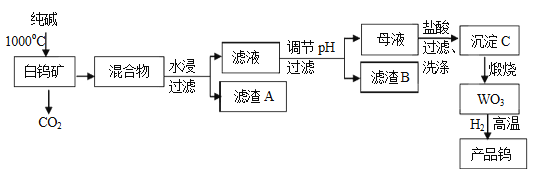
已知:
① 钨酸酸性很弱,难溶于水
② 完全沉淀离子的pH值:SiO32--为8,WO42--为5
③碳和金属钨在高温下会反应生成碳化钨
(1)74W在周期表的位置是第________周期。
(2)CaWO4与纯碱发生的化学反应方程式是_________________。
(3)滤渣B的主要成分是(写化学式)_____________。
调节pH可选用的试剂是:__________(填写字母序号)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.碳酸钠溶液
(4)母液中加入盐酸的离子方程式为____________________。
检验沉淀C是否洗涤干净的操作是:_______________________
(5)为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而须用氢气作还原剂的原因是:______________________________
将氢氧化钙加入钨酸钠碱性溶液中可得到钨酸钙,已知温度为T时Ksp(CaWO4) =1×10-10,Ksp[Ca(OH)2]= 4×10-7,当溶液中WO42-恰好沉淀完全(离子浓度等于10-5mol/L)时,溶液中 等于_________________
等于_________________
-
钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,钨在自然界主要以钨(VI) 酸盐的形式存在。有开采价值的钨矿石之一白钨矿的主要成分是CaWO4 ,含有二氧化硅、氧化铁等杂质,工业冶炼钨流程如下:
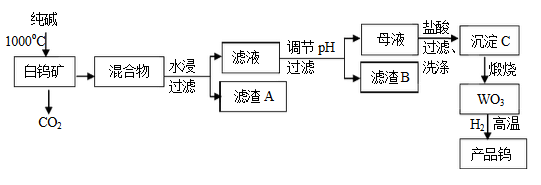
已知:
① 钨酸酸性很弱,难溶于水
② 完全沉淀离子的pH值:SiO32--为8,WO42--为5
③碳和金属钨在高温下会反应生成碳化钨
(1)74W在周期表的位置是第________周期。
(2)CaWO4与纯碱发生的化学反应方程式是_________________。
(3)滤渣B的主要成分是(写化学式)_____________。
调节pH可选用的试剂是:__________(填写字母序号)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.碳酸钠溶液
(4)母液中加入盐酸的离子方程式为____________________。
检验沉淀C是否洗涤干净的操作是:_______________________
(5)为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而须用氢气作还原剂的原因是:______________________________
将氢氧化钙加入钨酸钠碱性溶液中可得到钨酸钙,已知温度为T时Ksp(CaWO4) =1×10-10,Ksp[Ca(OH)2]= 4×10-7,当溶液中WO42-恰好沉淀完全(离子浓度等于10-5mol/L)时,溶液中 等于_________________
等于_________________
-
钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,钨在自然界主要以钨(W) 酸盐的形式存在。有开采价值的钨矿石之一白钨矿的主要成分是CaWO4 ,含有二氧化硅、氧化铁等杂质,工业冶炼钨流程如下:
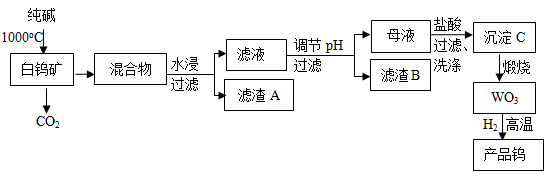
已知:① 钨酸酸性很弱,难溶于水
② 完全沉淀离子的pH值:SiO32—为8,WO42—为5
③ 碳和金属钨在高温下会反应生成碳化钨
(1)74W在周期表的位置是第 周期。
(2)CaWO4与纯碱发生的化学反应方程式是________________。
(3)滤渣B的主要成分是(写化学式)_____________。
调节pH可选用的试剂是:__________(填写字母序号)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.碳酸钠溶液
(4)母液中加入盐酸的离子方程式为 。检验沉淀C是否洗涤干净的操作是 。
(5)为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而必须用氢气作还原剂的原因是 。
(6)将氢氧化钙加入钨酸钠碱性溶液中可得到钨酸钙,已知温度为T时Ksp(CaWO4) =1×10—10,
Ksp[Ca(OH)2]= 4×10—7,当溶液中WO42-恰好沉淀完全(离子浓度等于10-5mol/L)时,溶液中 = 。
= 。
-
四氧化三锰(Mn3O4)是电子工业的磁性材料,而氯化铅(PbCl2)常用于焊料和助溶剂、制备其他铅盐等。用方铅矿精矿(主要成分为PbS)和软锰矿(主要成分是MnO2,还含有Fe2O3、Al2O3等杂质)制备PbCl2和Mn3O4的工艺流程如下:

已知:PbCl2(s) + 2Cl-(aq)  PbCl42- ( aq) ΔH > 0
PbCl42- ( aq) ΔH > 0
(1)80℃时,为提高方铅矿精矿、软锰矿与盐酸反应的速率,可采取的措施有________(写出一条即可)。
(2)试剂X是___________。(填“化学式”)
(3)用盐酸处理两种矿石粉末,生成MnCl2、PbCl2和S的总反应化学方程式为___________。
(4)结合化学用语回答,向酸浸液中加入饱和食盐水的目的是___________。
(5)向滤液b中通入NH3和O2发生反应后,总反应的离子方程式为___________。
(6)金属锰可以用Mn3O4为原料,通过铝热反应来制备,当生成5.5 kg Mn 时,理论上消耗金属铝的质量最少为___________kg。
-
钨是熔点最高的金属,是重要的战略物资,广泛用于钢铁工业,电真空照明材料等方面。黑钨矿是一种有开采价值的钨矿石,其主要成分是铁和锰的钨酸盐(常用FeWO4、MnWO4表示)。它的传统冶炼工艺的第一阶段如下图所示:

注:①上述流程中钨的化合价不变 ②钨酸(H2WO4)是一种难溶性酸
(1)写出C的化学式:______;写出生成B的化学方程式:_________
(2)上述流程中,第一次过滤所得滤渣的主要成份除MnO2外,还含有_________,请写出FeWO4在熔融条件下发生反应生成该成分的化学方程式_________
(3)冶炼金属钨是用非整比的钨氧化物为原料,钨元素在其中存在两种价态:+5价和+6价,试确定组成为WO2.7的氧化钨中两种对应价态的钨原子个数的整数比为_____________。
(4)黑钨矿还含少量Si、As的化合物,上述流程需优化(见下图)。向含Na2WO4的滤液中加硫酸调节pH=10后,再除杂净化。

则“净化”过程中,加入H2O2的目的是__________,滤渣Ⅰ的主要成分是____________。
(5)某温度下,Ca(OH)2、CaWO4的相关数据见下表
| 项目 | CaWO4 | Ca(OH)2 |
| -lgc(阴离子) | 4 | 2 |
| -lgc(Ca2+) | 6 | 4 |
将钨酸钠溶液加入石灰乳中,发生反应的离子方程式为WO42-(aq)+Ca(OH)2(s)  CaWO4(s)+2OH-(aq)该温度下此反应的平衡常数为______mol/L。
CaWO4(s)+2OH-(aq)该温度下此反应的平衡常数为______mol/L。
-
钨是熔点最高的金属,是重要的战略物资,广泛用于钢铁工业、电真空照明材料等方面。黑钨矿是一种有开采价值的钨矿石,其主要成分是铁和锰的钨酸盐(常用FeWO4、MnWO4表示)。它的传统冶炼工艺的第一阶段如下图所示:

注:①上述流程中钨的化合价不变;②钨酸(H2WO4)是一种难溶性酸
(1)写出C的化学式____________;写出生成B的化学方程式____________________;
(2)上述流程中,第一次过滤所得滤渣的主要成份除MnO2外,还含有___________,请写出FeWO4在熔融条件下发生反应生成该成分的化学方程式_____________________;
(3)冶炼金属钨是用非整比的钨氧化物为原料,钨元素在其中存在两种价态:+5价和+6价,试确定组成为WO2.7的氧化物中两种对应价态的钨原子个数的整数比为_______;
(4)黑钨矿还含有Si、As的化合物,上述流程需优化(见下图),向含有Na2WO4的滤液中加硫酸调节pH=10后,再除杂净化。

则“净化”过程中,加入H2O2的目的是_________________________________________;滤渣I的主要成分是__________________________。
(5)某温度下,Ca(OH)2、CaWO4的相关数据见下表
| 项目 | CaWO4 | Ca(OH)2 |
| -lgc(阴离子) | 4 | 2 |
| -lgc(Ca2+) | 6 | 4 |
将钨酸钠溶液加入石灰乳中,发生反应的离子方程式为:WO42−(ag)+Ca(OH)2(s) CaWO4(s)+2OH−(ag),该温度下此反应的平衡常数为______mol/L。
CaWO4(s)+2OH−(ag),该温度下此反应的平衡常数为______mol/L。
-
铋(83号元素)主要用于制造合金,铋合金具有凝固时不收缩的特性,用于铸造印刷铅字和高精度铸型。湿法提铋新工艺以氧化铋渣(主要成分为 ,含有
,含有 、
、 、
、 杂质)为原料提Bi的工艺流程如下:
杂质)为原料提Bi的工艺流程如下:
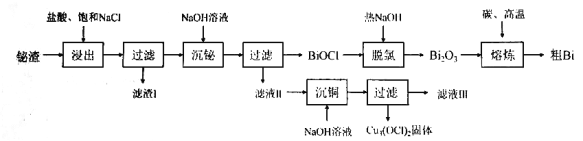
已知:Ⅰ. 不溶于水,加热至700℃就分解生成
不溶于水,加热至700℃就分解生成 ,
, 的沸点为447℃。
的沸点为447℃。
Ⅱ.25℃时, ;
; 。
。
回答下列问题:
(1)铋在元素周期表中的位置为___________________。
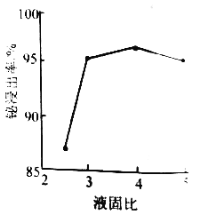
(2)“浸出”时,在盐酸浓度 、浸出温度70℃、浸出时间2h及不同浸出液固比条件下进行浸出实验,浸出率与液固比的关系如图所示,最合适的液固比应选__________。
、浸出温度70℃、浸出时间2h及不同浸出液固比条件下进行浸出实验,浸出率与液固比的关系如图所示,最合适的液固比应选__________。
(3)“滤渣Ⅰ”的成分为_____________(填化学式)。
(4)“脱氯”的化学方程式为___________________。
(5)“沉铜”时,向“滤液Ⅱ”中加入NaOH溶液调节pH,促进 水解生成
水解生成 ,则此过程中
,则此过程中 水解的离子方程式为_________________________。若“滤液Ⅱ”中
水解的离子方程式为_________________________。若“滤液Ⅱ”中 为
为 ,当加入等体积的NaOH溶液时,pH恰好为6,出现沉淀
,当加入等体积的NaOH溶液时,pH恰好为6,出现沉淀 ,此时
,此时 的去除率为________(忽略溶液体积变化)。
的去除率为________(忽略溶液体积变化)。
(6)“滤液Ⅲ”经加热浓缩后可返回____________工序循环使用。
具有很大的工业价值,主要用于电子工业,合金添加剂等。工业上利用白钨矿精矿为原料
主要成分为钨酸钙
,还含有CaO、
等杂质
生产钨粉的一种工艺流程如下:

钨酸钙微溶于水,能溶解在热盐酸中。
降低溶液pH可以从钨酸铵溶液中析出仲钨酸铵晶体,常温时可析出带11个结晶水的仲钨酸铵晶体,但是由于颗粒很细小,难以进一步提纯。在
时可析出颗粒较大的带5个结晶水的仲钨酸铵晶体,可进一步提纯精制。
酸浸时为了提高浸出率,可采取的措施有___________。
答出两条即可
酸浸时,需控制反应温度在
之间的原因是________。
酸浸时发生的主要反应的化学方程式是____。
将废酸与粗钨酸分离的操作是_____
填操作名称
。
加入过量氨水后过滤,得到滤渣的主要成分是______
填化学式
。
工艺流程中“结晶析出”,采用的结晶方法是________。
仲钨酸铵的化学式为
,写出仲钨酸铵煅烧转化为
的化学方程式_______________。
已知白钨矿精矿中的钨酸钙质量分数为
,
该精矿经上述流程制得
钨粉。则该生产中钨的产率为_______
用含“a”“w”“m”的代数式表示
。











