-
实验室中需要22.4 L(标准状况)SO2气体。化学小组同学依据化学方程式Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(ρ=1.84g/mL)110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(ρ=1.84g/mL)110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
(1)化学小组所制得的气体中混有的主要杂质气体可能是____________(填分子式)。产生这种结果的主要原因是______________________________(用化学方程式和必要的文字加以说明)
(2)为证实相关分析,化学小组的同学设计了实验,组装了如下装置,对所制取的气体进行探究。
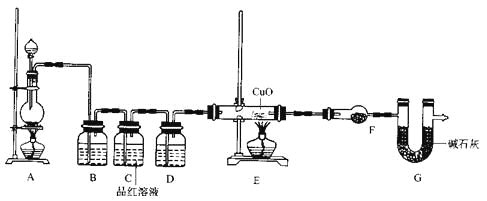
①装置B中加入的试剂_________,作用是_____________________。
②装置D加入的试剂_________,装置F加入的试剂_____________________。
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有某杂质气体的实验现象是______________________________________。
④U型管G的作用为_______________________________________。
-
实验室中需要22.4L(标准状况)SO2气体。化学小组同学依据化学方程式Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(ρ=1.84g/cm3)110mL充分反应,锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
(1)化学小组所制得的气体中混有的主要杂质气体可能是_______(填分子式)。产生这种结果的主要原因是_______________________(用化学方程式和必要的文字加以说明)。
(2)为证实相关分析,化学小组的同学设计了实验,组装了如下装置,对所制取的气体进行探究。
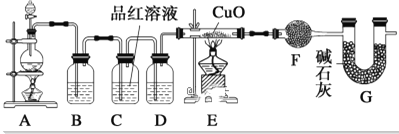
①装置B中加入的试剂_______,反应的离子方程式:______________。
②装置D加入的试剂及作用_______,装置F加入的试剂试剂及作用_______。
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有某杂质气体的实验现象是______________。④U形管G的作用为______________。
-
实验室中需要22.4 l(标准状况)SO2气体。化学小组同学依据化学方程式Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4(
ZnSO4+SO2↑+2H2O计算后,取65.0g锌粒与98%的浓H2SO4( )110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
)110mL充分反应锌全部溶解,对于制得的气体,有同学认为可能混有杂质。
(1)化学小组所制得的气体中混有的主要杂质气体可能是____________(填分子式)。产生这种结果的主要原因是____________________________________________
(用化学方程式和必要的文字加以说明)
(2)为证实相关分析,化学小组的同学设计了实验,组装了如下装置,对所制取的气体进行探究。
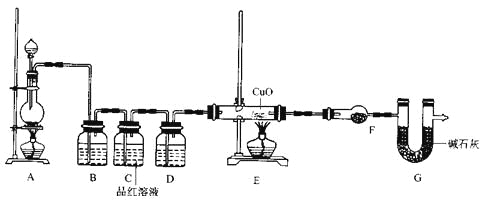
①装置B中加入的试剂_________,作用是_____________________。
②装置D加入的试剂_________,装置F加入的试剂_____________________。
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有某杂质气体的实验现象是______________________________________。
④U型管G的作用为_______________________________________.
-
(10分)化学小组同学依据化学反应Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。
ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。
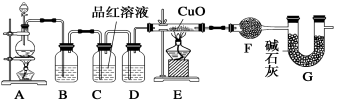
请回答下列问题:
(1)装置A中添加液体的仪器名称为 ;98%的浓H2SO4(ρ=1.84 g/cm3)的物质的量浓度是 ;
(2)请写出产生氢气的反应的离子方程式 ;
(3)①装置B是为了吸收SO2,则不能选用下列试剂中的 (填序号);
A.NaOH溶液 B.浓H2SO4 C.KMnO4溶液
②可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有氢气的实验现象是 ;
-
将一定量的锌粉加入浓硫酸中,反应过程中产生混合气体SO2和H2在标准状况下体积为4.48L。( 已知:Zn +2H2SO4(浓)= ZnSO4 +SO2 ↑+ 2H2O )
(1)需要锌粉的质量至少多少克?
(2)若生成H2标准状况下体积为1.12L,消耗硫酸物质的量为多少mol?
-
化学探究小组的同学将过量锌粉与44mL浓硫酸在加热条件下充分反应,至不再产生气体时共收集到标准状况下11.2L的气体,其质量为19.6g.(若锌与浓硫酸在加热情况下发生的反应为:
Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O)
ZnSO4+SO2↑+2H2O)
| 气体的成分(化学式) | 气体的物质的量(mol) |
| ① | | |
| ② | | |
| ③ | | |
(1)试根据相关信息判断11.2L气体的成分,并计算气体中各成分的物质的量,填在以上表格内,每种气体只填一行(不一定填满).
(2)浓硫酸的物质的量浓度为______.
-
如图是某学校实验室从化学试剂商品店买回的硫酸试剂标签上的部分内容,据此,下列说法正确的是( )

(已知:Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O;Zn+H2SO4(稀)=ZnSO4++H2↑)
A.该硫酸的物质的量浓度为9.2mol·L-1
B.1molZn与足量的该硫酸反应产生2mol气体
C.配制200mL4.6mol·L-1的稀硫酸需取该硫酸50.0mL
D.该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2mol·L-1
-
Zn与浓硫酸反应的化学方程式:Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O.向100ml 18mol/L H2SO4溶液中加入足量的锌粒充分反应后,被还原的H2SO4的物质的量为( )
A.等于1.8mol
B.小于0.90mol
C.等于0.90mol
D.在0.90mol和1.8mol之间
-
已知标准状况下气体摩尔体积为22.4 L/mol,但很多化学实验并非在标准状况下进行,而是在常温常压下进行,下图为测定常温常压下气体摩尔体积的实验装置图。图中反应原理为:2C2H5OH+2Na→2C2H5ONa+H2↑(反应放热)。
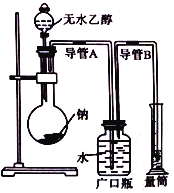
(1)①该装置有明显错误处,请指出错误之处:_________;
②作图修改(只针对需修改部位):_____________。
(2)经过(1)改正后进行实验,实验过程如下:
a.检查装置气密性;
b.常温常压下,取4.6g 乙醇与足量的金属钠反应并利用排水法收集产生的H2(假设广口瓶和量筒足够大);
c.当圆底烧瓶中不再有气泡产生,不能立即读数,必须先_____,后________,再平视读取量筒中收集到水的体积为1240.0 mL。经计算常温常压下气体摩尔体积为__________。
(3)经过(1)改正后仍有实验误差,下列哪些选项会导致实验误差_______。
A.收集到的氢气中含有装置中原有的空气
B.收集H2前导管B中无蒸馏水
C.分液漏斗中的无水乙醇进入圆底烧瓶后占用了装置内气体空间
-
下列说法正确的是( )
A.能电离出H+的化合物叫做酸
B.实验测得1mol某气体体积为22.4L,测定条件一定是标准状况
C.虽然SO2的水溶液能导电,但SO2不是电解质
D.有单质参加的化学反应一定是氧化还原反应





