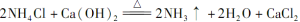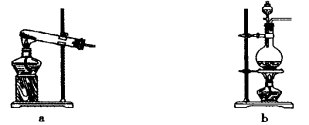-
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。A中发生反应的化学方程式: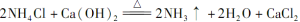
【实验探究】
(1)A中的反应 (填“是”或“不是”)氧化还原反应。
(2)A装置还可用于制取气体 (只填一种)
(3)若有10.7gNH4Cl固体,最多可制取NH3(标准状况)的体积是 L (NH4C1的摩尔质量为53.5g·mol-1)。
(4)实验室收集氨气的方法是
(5)C、D装置中颜色会发生变化的是 (填“C”或“D”)
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴人1-2滴浓盐酸,可观察到的现象是
(7)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是 (填“F”或“G”)。
【知识拓展】
(8)生石灰与水反应生成Ca(OH)2并放出热量[化学方程式为CaO+H2O==Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列 物质代替(填序号)。
A.碱石灰(NaOH与CaO的固体混合物) B.NaOH 固体
C.硫酸溶液 D.石灰石(含CaCO3)
【知识应用】
(9)2010年11月9日晚,我省宁德市一冷冻厂发生氨气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救为法?
-
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。A中发生反应的化学方程式:2NH4Cl+Ca(OH)2 2NH3↑+2H2O+CaCl2。
2NH3↑+2H2O+CaCl2。
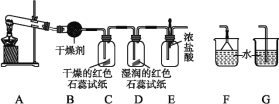
[实验探究]
(1)A中的反应_____(填“是”或“不是”)氧化还原反应。
(2)A装置还可用于制取气体_______(只填一种)。
(3)实验室收集氨气的方法是________________。
(4)若有10.7 g NH4Cl固体,最多可制取NH3(标准状况)的体积是_____ L(NH4Cl的摩尔质量为 53.5 g/mol)。
(5)C、D装置中颜色会发生变化的是_____(填“C”或“D”)。
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是____________________。
(7)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_____(填“F”或“G”)。
(8)生石灰与水反应生成Ca(OH)2并放出热量[化学方程式为CaO+H2O=Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列________(填字母)物质代替。
A.碱石灰(NaOH与CaO的固体混合物) B.NaOH固体
C.硫酸溶液 D.石灰石(含CaCO3)
(9)2010年11月9日晚,福建省宁德市一冷冻厂发生氨气泄漏事件,500多居民深夜大转移。假如你在现场,你会采用什么自救方法?_______________________________________________。
-
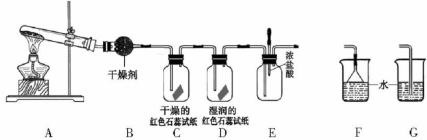
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。A中试管内盛放的物质是Ca(OH)2、NH4Cl固体。
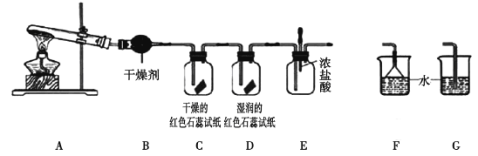
(实验探究)
(1)A中发生反应的化学方程式为________;
(2)B中盛放的干燥剂为_____,干燥氨气能否用浓硫酸_____(填“能”或“不能”) ;
(3)若有10.7gNH4Cl固体,最多可制取NH3(标准状况)的体积是_____L;
(4)实验室收集氨气的方法是________;
(5)C、D装置中颜色会发生变化的是_______(填“C”或“D”),红色石蕊试纸变成____色;
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_______;
(7)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_______(填“F”或“G”)。
-
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。

(实验探究)
(1) A中制备氨气的化学反应方程式_________
(2)A中的反应___________(填“是”或“不是”)氧化还原反应。
(3)A装置还可用于制取气体___________ (只填一种)
(4)若有10.7gNH4Cl固体,最多可制取NH3(标准状况)的体积是_____ L
(5)实验室收集氨气的方法是___________
(6)检验氨气的方法是__________
(7)C、D装置中颜色会发生变化的是___________ (填“C”或“D”)
(8)当实验进行一段时间后,挤压E装置中的胶头滴管,滴人1-2滴浓盐酸,可观察到的现象是___________
(9)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是___________ (填“F”或“G”)。
(知识拓展)
(10)生石灰与水反应生成Ca(OH)2并放出热量化学方程式 [CaO+H2O==Ca(OH)2]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列 ___________ 物质代替(填序号)。
A.碱石灰(NaOH与CaO的固体混合物) B.NaOH 固体
C.硫酸溶液 D.石灰石(含CaCO3)
(知识应用)
(11)2010年11月9日晚,我省宁德市一冷冻厂发生氨气泄漏事件,500多居民深夜大转移。假如你在现场,你会采用什么自救为法? ____________
-
(8分)某中学化学研究性学习小组利用以下装置制取并探究氨气的性质。A中发生反应的化学方程式:2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2H2O
CaCl2 + 2NH3↑+ 2H2O
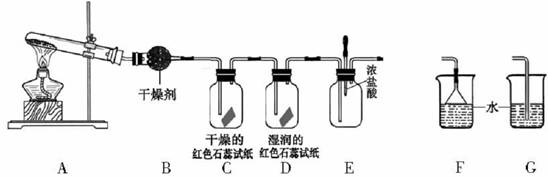
(1)A中的反应________(填“是”或“不是”)氧化还原反应;
(2)A装置还可用于制取气体________(只填一种);
(3)实验室收集氨气的方法是________;
(4)C、D装置中颜色会发生变化的是________(填“C”或“D”);
(5)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是________(填“F”或“G”);
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴人1-2滴浓盐酸,可观察到的现象是________;
(7)2010 年 11月9日晚,我省一冷冻厂发生氨气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救为法?________。
-
某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
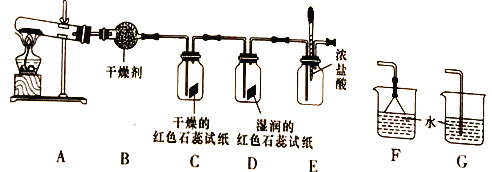
(1)B装置中的干燥剂是_____ (填“碱石灰”或“浓硫酸”)。
(2)C、D 装置中试纸颜色会发生变化的是_____(填”C”或“D”)。
(3)当实验进行段时间后,挤压E装置中的胶头滴管,滴入1- -2滴浓盐酸,可观察到 E装置中的现象是产生______(填” 烟”或“白雾”)。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_____ (填“F”或“G”)。
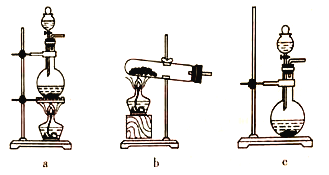
(5)生石灰与水反应生成Ca(OH)2并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是____ (填“a”“b”或“c”)。
-
某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
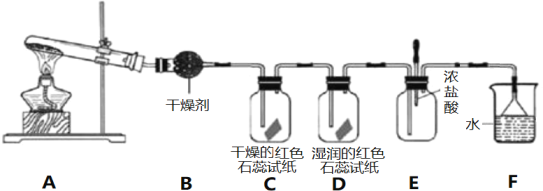
(1)B装置中的干燥剂是_________________(填“碱石灰”或“浓硫酸”)。
(2)C、D 装置中试纸颜色会发生变化的是___________(填”C”或“D”)。
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到 E装置中的现象是产生_____________(填” 白烟”或“白雾”)。
(4)烧杯F中水的作用是________________________。
(5)欲制得标准状况下11.2 LNH3,至少需要Ca(OH)2的质量为____________g。
-
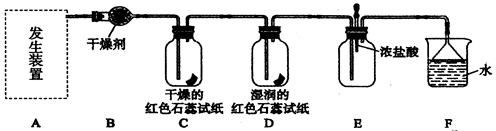
某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。
【实验探究】
(1)实验室制取氨气应选用下图中________发生装置进行实验,反应的化学方程式为
_________________________

(2)B装 置中的干燥剂可选用________(填“碱石灰”或“浓硫酸”)。
置中的干燥剂可选用________(填“碱石灰”或“浓硫酸”)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是____(填“C”或“D”)。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是____________________________________________________________。
(5)F装置中倒置漏斗的作用_______________________ _________________________。
_________________________。
(6)某同学用右图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有________性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(7)氨气的用途很广。如可用氨气处理二氧化氮:8NH3 + 6NO2 ==7N2 + 12H2O
该反应中氨气体现________(填“氧化性”或“还原性”)。请你列举出氨气的另一种用途_____________________________________________。
-
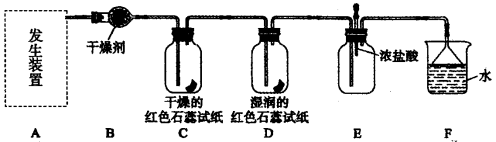
某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。[制取氨气的反应原理:2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O]
【实验探究】
(1)利用上述原理,实验室制取氨气应选用下图中 发生装置进行实验。
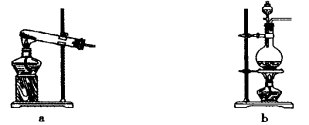
(2)B装置中的干燥剂可选用 (填“碱石灰”或“浓硫酸”)。
(3)用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为 L。(NH4Cl的摩尔质量为53.5 g·mol-1)
(4)气体通过C、D装置时,试纸颜色会发生变化的是 (填“C”或“D”)。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是 。
(6)F装置中倒置漏斗的作用 。
【拓展应用】
(7)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有 性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
(8)氨气的用途很广。如可用氨气处理二氧化氮: 8NH3 + 6NO2 =7N2 + 12H2O
该反应中氨气体现 (填“氧化性”或“还原性”)。
请你列举出氨气的另一种用途 。
-
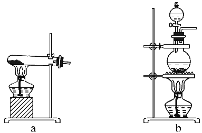
某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。已知:制取氨气的反应原理为2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
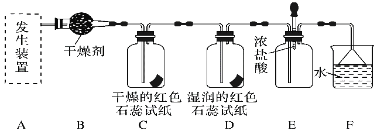
[实验探究]
(1)利用上述原理,实验室制取氨气应选用下图中________(填序号)发生装置进行实验。
(2)B装置中的干燥剂可选用________(填“碱石灰”或“浓硫酸”)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是________(填“C”或“D”)。
(4)F装置中倒置漏斗的作用是___________________________________。
(5)某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有________性质(填序号)。
a.还原性 b.极易溶于水 c.与水反应生成碱性物质
2NH3↑+2H2O+CaCl2。