-
根据核外电子的排布特点推断元素的性质:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为_____,在周期表中位于___区。
(2) B元素基态原子的M层全充满,N层没有成对电子且只有一个未成对电子,B的基态原子的价层电子排布式为_______。
(3)请利用电子排布的相关知识稳定性:Fe3+______Fe2+(填>或< ),原因___________,第一电离能:Mg____Al(填>或< )原因__________。
(4) 有以下物质:①H2 ②N2 ③CO2 ④N2H4⑤H2O2 ⑥HCN(H—C≡N);只有σ键的是______;既有σ键又有π键的是__________;含有由两个原子的s轨道重叠形成的σ键的是_____;含有由一个原子的s轨道与另一个原子的p轨道重叠形成的σ键的是______;
(5) 通过 (3)的解答,请归纳基态原子核外电子排布除了符合构造原理外,泡利原理、洪特规则外,还有哪些结构稳定__________。
高二化学综合题中等难度题查看答案及解析
-
下列说法正确的是( )
A.第ⅥA族元素形成的简单氢化物中,稳定性最好的其沸点也最高
B.除氢元素外最外层都只有一个电子的元素,其化学性质相似
C.根据原子核外电子排布的特点,Cu在元素周期表中位于d区
D.在周期表中,元素F的电负性最大,Li的电负性最小
高二化学单选题简单题查看答案及解析
-
(13分) 四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
元素 A B C D
性质
结构
信息 原子核外有两个电子层,最外层有3个未成对的电子 原子的M层有1对成对的p电子 原子核外电子排布为[Ar]3d104s1,
有+1、+2两种常见化合价 有两种常见氧化物,其中有一种是冶金工业常用的还原剂
⑴写出B原子的电子排布式________。
⑵A元素的氢化物的沸点比同主族相邻元素氢化物沸点________(填“高”或“低”),其是__________________________。
⑶D的最高价氧化物的电子式:________。高温下D的氧化物还原赤铁矿的方程式为可逆反应,写出该反应的化学方程式___________________,该反应的平衡常数表达式K=___________。
⑷往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为________________,简要描述该配合物中化学键的成键情况__________________。
⑸下列分子结构图中的“
”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示氢原子,小黑点“
”表示没有形成共价键的最外层电子,短线表示共价键。
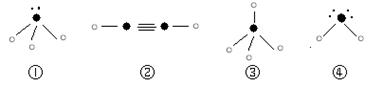
则在以上分子中,中心原子采用sp3杂化形成化学键的且空间构型是角形的是________(填写序号);在②的分子中有________个σ键和________个π键。
⑹已知NH4+、N4H44+的空间构型均为四面体,NH4+的结构式为 \s\up10(∣←N-,\s\up10(∣H(→表示共用电子对由N原子单方面提供)。 请画出N4H44+的结构式_____________________。
高二化学填空题极难题查看答案及解析
-
根据原子结构及元素周期律的知识,下列推断正确的是( )
A. 核外电子排布相同的微粒化学性质也相同
B. Cl与Cl得电子能力相同
C. Cl-、S2-、Ca2+、K+半径逐渐减小
D. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
高二化学单选题中等难度题查看答案及解析
-
根据原子结构及元素周期律的知识,下列推断正确的是
A.
得电子能力相同
B.同主族元素含氧酸的酸性随核电荷数的增加而减弱
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D.核外电子排布相同的微粒化学性质也相同
高二化学选择题中等难度题查看答案及解析
-
根据原子结构及元素周期律的知识,下列推断正确的是
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. Cl-、S2-、Ca2+、K+半径逐渐减小
D.
与
得电子能力相同
高二化学选择题中等难度题查看答案及解析
-
X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如下表
元素
结构或性质信息
X
其原子最外层电子数是内层电子数的2倍
Y
基态原子最外层电子排布为nsnnpn+1
Z
非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰
M
单质在常温、常压下是气体。基态原子的M层上有1个未成对的p电子
Q
其与X形成的合金为目前用量最多的金属材料
(1)Q元素基态原子的电子排布式是________,Y原子的电子排布图是 。
(2)比较Y元素与氧元素的第一电离能____>____;X和Z形成的化合物XZ2为一种液体溶剂,其化学式是 ,分子中的
键和
键数目之比为_____。
(3)写出实验室制备M单质的离子方程式 。
(4)M的气态氢化物和氟化氢相比(写化学式)
稳定性强的是_____________,其原因是_____________________;
沸点高的是_____________,其原因是_____________________。
高二化学填空题困难题查看答案及解析
-
X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如下表:
元素
结构或性质信息
X
其原子最外层电子数是内层电子数的2倍
Y
基态原子最外层电子排布为nsnnpn+1
Z
非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰
M
单质在常温、常压下是气体。基态原子的M层上有1个未成对的p电子
Q
其与X形成的合金为目前用量最多的金属材料
(1)Q元素基态原子的电子排布式是:____________。比Q元素原子序数大3的元素的原子结构示意图为 。
(2)比较Y元素与氧元素的第一电离能大小顺序 ;X和Z形成的化合物XZ2为一种液体溶剂,其电子式为 。
(3)写出实验室制备M单质的离子方程式:_____________。
(4)M的气态氢化物和氟化氢相比稳定性强的是___________(写化学式)。
高二化学填空题困难题查看答案及解析
-
已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A.某元素原子的第二电子层电子排布图为

B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层上电子数为6
D.某元素的外围电子排布式为5s25p1
高二化学单选题中等难度题查看答案及解析
-
已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A.某元素原子的第二电子层电子排布图为

B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层上电子数为6
D.某元素的外围电子排布式为5s25p1
高二化学单选题中等难度题查看答案及解析