-
已知常温下部分弱酸的电离常数如表,下列说法不正确的是( )
弱酸
电离常数
CH3COOH
Ka=1.76×10-5
H2SO3
Ka1=1.23×10-2、 Ka2=5.6×10-8
HF
Ka=6.8×10-4
A. 在1mol/LNaHA(酸式盐)溶液中不一定存在:c(Na+)=c(H2A)+c(HA-)+c(A2-)
B. 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C. 常温下,相同物质的量浓度的CH3COONa、NaF、Na2SO3、NaHSO3水溶液,溶液中离子总数由小到大的顺序是Na2SO3>CH3COONa>NaF>NaHSO3
D. 常温下,pH均等于3的醋酸溶液与盐酸等体积混合后,溶液的pH不变
高二化学单选题中等难度题查看答案及解析
-
已知常温下部分弱酸的电离常数如表,下列说法不正确的是
弱酸
电离常数
CH3COOH
Ka=1.76×10-5
H2SO3
Ka1=1.23×10-2、 Ka2=5.6×10-8
HF
Ka=6.8×10-4
A. 在1mol/LNaHA(酸式盐)溶液中不一定存在:c(Na+)=c(H2A)+c(HA-)+c(A2-)
B. 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C. 常温下,pH均等于3的醋酸溶液与盐酸等体积混合后,溶液的pH变小
D. 常温下,相同体积、相同物质的量浓度的NaF、Na2SO3、NaHSO3水溶液,溶液中离子总数由大到小的顺序是:Na2SO3 > NaHSO3 > NaF
高二化学单选题中等难度题查看答案及解析
-
常温下,部分弱酸的电离平衡常数如下表:
弱酸
CH3COOH
HCN
H2CO3
电离平衡常数(25℃)
K1=1.76×10-5
K1=4.9×10-10
K1=4.3×10-7
K2=5.6×10-11
下列选项错误的是
A.中和等体积、等pH的CH3COOH溶液和HCN溶液消耗NaOH的量前者大于后者
B.可发生反应:2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑
C.Na+、CN-、CH3COO-、HCO3-等离子能大量共存
D.等浓度的CH3COONa和NaCN溶液pH前者小于后者
高二化学选择题简单题查看答案及解析
-
下表是几种常见弱酸的电离平衡常数Ka(25℃).
回答下列问题:酸 电离方程式 电离平衡常数Ka CH3COOH CH3COOH⇌CH3COO-+H+ 1.76×10-5 H2S H2S⇌H++HS-
HS-⇌H++S2-Ka1=9.1×10-8
Ka2=1.1×10-12H3PO4 H3PO4⇌H++H2PO4-
H2PO4-⇌H++HPO42-
HPO42-⇌H++PO43-Ka1=7.52×10-3
Ka2=6.23×10-8
Ka3=2.20×10-13
(1)一般情况下,当温度升高时,Ka______ (填“增大”、“减小”或“不变”).
(2)同一温度下,各弱酸Ka的大小与酸性的相对强弱关系为______.
(3)若把CH3COOH、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是______,最弱的是______.
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸,Ka1、Ka2、Ka3在数值上相差甚大,如磷酸:Ka1:Ka2:Ka3≈1:10-5:10-10,造成这种差异的原因可能是______.高二化学解答题中等难度题查看答案及解析
-
已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸
CH3COOH
H2CO3
电离平衡常数(常温)
Ka=1.8×10-5
Ka1=4.3×10-7;
Ka2=5.6×10-11
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则c(CH3COOH)/c(CH3COO-)=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
高二化学单选题困难题查看答案及解析
-
已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸
CH3COOH
H2CO3
电离平衡
常数(常温)
Ka=1.8×10-5
Ka1=4.3×10-7
Ka2=5.6×10-11
下列判断正确的是( )
A. 向Na2CO3溶液中滴入酚酞,溶液变红,原因是CO32-+2H2O
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则
=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4mol·L-1的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5mol·L-1
高二化学单选题困难题查看答案及解析
-
已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸
CH3COOH
H2CO3
电离平衡常数(常温)
Ka=1.8×10-5
Ka1=4.3×10-7;
Ka2=5.6×10-11
下列判断正确的是
A.向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O
H2CO3+2OH-
B.常温时,CH3COOH与CH3COONa混合溶液的pH=6,则c(CH3COOH)/c(CH3COO-)=18
C.NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D.2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
高二化学单选题困难题查看答案及解析
-
已知Ksp(CaCO3)=2.8×10-9及表中有关信息:
弱酸
CH3COOH
H2CO3
电离平衡常数(常温)
Ka=1.8×10-5
Ka1=4.3×10-7;
Ka2=5.6×10-11
下列判断正确的是
A. 向Na2CO3溶液中滴入酚酞,溶液变红,主要原因是CO32-+2H2O
H2CO3+2OH-
B. 常温时,CH3COOH与CH3COONa混合溶液的pH=6,则
=18
C. NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-)
D. 2×10-4 mol/L的Na2CO3溶液与CaCl2溶液等体积混合出现沉淀,则CaCl2溶液的浓度一定是5.6×10-5 mol/L
高二化学单选题困难题查看答案及解析
-
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸
CH3COOH
HCN
H2CO3
电离常数(25℃)
Ka = 1.8×10-5
Ka=4.3×l0-10
Ka1=5.0×l0-7 Ka2=5.6×l0-11
①0.1 moI/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______c(HCO3 -)(填“>”、“<”或“=”)。②常温下,pH相同的三种溶液A.CH3COONa B.NaCN C.Na2CO3,其物质的量浓度由大到小的顺序是________(填编号)。
③已知25℃时,CH3COOH(aq)+OH -( aq)=CH3COO-(aq) +H2O(1) △H=-akJ/mol,H+(aq) +OH-(aq) =H2O(1) △H=-b kJ/mol,醋酸电离的热化学方程式为________________________________________。
④将少量CO2通入NaCN溶液,反应的离子方程式是______________________________。
⑤室温下,—定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是________________,溶液中c(CH3COO—)/c(CH3COOH)___________。
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示。
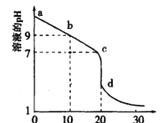
①d点所示的溶液中离子浓度由大到小的顺序依次为_______________。
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=__________(用溶液中的其它离子浓度表示)。
③pH =10的氨水与pH =4的NH4C1溶液中,由水电离出的c(H+)之比为____。
高二化学填空题中等难度题查看答案及解析
-
电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸
CH3COOH
HCN
H2CO3
电离常数(25℃)
Ka = 1.8×10-5
Ka=4.3×l0-10
Ka1=5.0×l0-7 Ka2=5.6×l0-11
① 0.1 moI/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______c(HCO3-)(填“>”、“<”或“=”)。
②常温下,pH相同的三种溶液:A.CH3COONa B.NaCN C.Na2CO3,其物质的量浓度由大到小的顺序是________(填编号)。
③已知25℃时,CH3COOH(aq)+OH-( aq)=CH3COO-(aq) +H2O △H=-akJ/mol,H+(aq) +OH-(aq) =H2O △H=-b kJ/mol,醋酸电离的热化学方程式为________________。
④将少量CO2通入NaCN溶液,反应的离子方程式是____________________________。
⑤室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是______________,溶液中c(CH3COO-)/c(CH3COOH) =___________。
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。
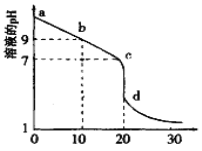
① d点所示的溶液中离子浓度由大到小的顺序依次为____________。
② b点所示的溶液中c(NH3·H2O)-c(NH4+)=_________(用溶液中的其它离子浓度表示)。
高二化学填空题中等难度题查看答案及解析