-
某温度时,Kw=1.0×10-12,若在该温度时,某溶液的c(H+)=1.0×10-7mol•L-1,则该溶液
A. 呈酸性 B. 呈碱性 C. 呈中性 D. 
-
(1)某温度(t℃)时,水的Kw=1×10-12,则该温度下,c(H+)=1×10-7mol/L的溶液呈___(填“酸性”、“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=___mol•L-1
(2)25℃时,0.1mol/L的6种溶液,水电离出来的c(H+)由大到小的关系是___(填序号)
①盐酸 ②H2SO4 ③CH3COOH(Ka=1.7×10-5) ④氨水(Kb=1.7×10-5) ⑤NaOH ⑥Ba(OH)2
(3)已知常温时,0.1mol/L醋酸在水中有1%发生电离,则该溶液的pH=_________,醋酸的电离平衡常数Ka=_______________。
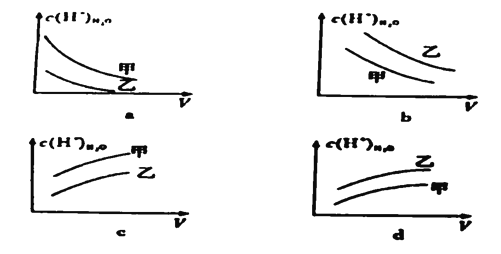
(4)下列曲线中,可以描述0.1mol/L乙酸(甲,Ka=1.8×10-5)和0.1mol/LHF(乙,Ka=3.5×10-4)的水溶液中,水电离出来的c(H+)与加入水体积V的关系是__________(填字母代号)
-
(12分) (1)某温度下,Kw=10-12。
①若保持温度不变,某溶液中c(H+)为1×10-7mol·L-1,则该溶液显________性(填“酸”、“碱”或“中”)。
②若保持温度不变,向水中通入的HCl气体恰好使溶液中c(H+)/c(OH-)=1010,则此时水电离的c(H+)=________mol·L-1。
(2)常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
①混合溶液的pH=8的原因(用离子方程式表示):________。
②混合溶液中离子浓度由大到小的顺序是:________。
③混合溶液中由水电离出的c(H+)________同浓度NaOH溶液中由水电离出的c(H+)
(填“>”、“<”或“=”)。
④求出混合溶液中下列算式的精确计算结果(填具体数据):
c(Na+)-c(A-)=________mol/L。
-
已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
(1)某温度时,Kw=1.0×10-12,若在该温度时,某溶液的c(H+)=1.0×10-7mol/L,则该溶液呈 性。
(2)常温下,浓度均为0.1 mol·L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.0 |
①上述盐溶液中的阴离子,结合质子(H+)能力最强的是
②根据表中数据判断,浓度均为0.01 mol·L-1的下列五种物质的溶液中,酸性最强的是 ;
将各溶液分别稀释100倍,pH变化最小的是 (填编号)。
A.HCN B.HClO C.C6H5OH D.CH3COOH
③据上表数据,请计算0.1mol/L的NaCN溶液中水电离出的氢氧根离子浓度 。
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,请用平衡移动原理解释其原因 (写离子方程式并用必要的文字说明)。
(3)在0.1mol/L的NaClO溶液中,写出离子浓度的大小关系 。
-
某温度时水的离子积为1×10-12,若该温度下某溶液中的H+浓度为1×10-7mol·L-1,则该溶液是
A. 酸性 B. 碱性 C. 中性 D. 无法判断
-
1 00℃时,水的离子积为1×10-12,若该温度下某溶液中的H+ 浓度为1×10-7mol/L则该溶液是
00℃时,水的离子积为1×10-12,若该温度下某溶液中的H+ 浓度为1×10-7mol/L则该溶液是
A.酸性 B.碱性 C.中性 D. 无法判断
无法判断
-
100℃时,水的离子积为1×10-12,该温度下某溶液中的c(H+)为10-7mol.L-1,则该溶液
A.呈碱性 B.呈酸性 C.呈中性 D.无法判断
-
在100 ℃时,水的离子积为1×10-12,若该温度下某溶液中的H+浓度为1×10-7mol·L-1,则该溶液( )
A.呈碱性 B.呈酸性 C.呈中性 D.c(OH-)=100c(H+)
-
在100 ℃时,水的离子积为1×10-12,若该温度下某溶液中的H+浓度为1×10-7mol·L-1,则该溶液( )
A. 呈碱性 B. 呈酸性 C. 呈中性 D. c(OH-)=100c(H+)
-
40 ℃时水的离子积Kw=2.9×10-14,则在40 ℃时,c(H+)=1×10-7mol·L-1的溶液( )
A. 呈酸性 B. 呈碱性 C. 呈中性 D. 无法判断
