-
钴、镍与铁是同族元素,它们的单质及化合物的性质有很多相似之处。
(1) 为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下甲、乙、丙三个实验装置。丙装置中X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。

①甲池Fe电极反应式为_________。由现象可知三种金属的活动性由强到弱的顺序是__________(填元素符号) 。
②写出丙装置中反应的离子方程式____________________。
(2)Na2FeO4具有广泛用途,可通过电解法制取得到,工作原理图丁所示。通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。已知: Na2FeO4只在强碱性条件下稳定,易被H2还原。
①Fe电极反应式为________。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______________。
③当阴极产生112mL(标准状况)的气体时,通过阴离子交换膜的离子有_______mol。
-
钴、镍与铁是同族元素,它们的单质及化合物的性质有很多相似之处。
(1) 为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下甲、乙、丙三个实验装置。丙装置中X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。
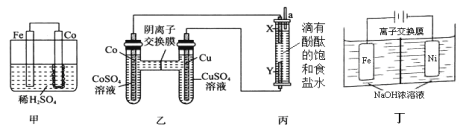
①甲池Fe电极反应式为_________。由现象可知三种金属的活动性由强到弱的顺序是__________(填元素符号) 。
②写出丙装置中反应的离子方程式____________________。
(2)Na2FeO4具有广泛用途,可通过电解法制取得到,工作原理图丁所示。通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。已知: Na2FeO4只在强碱性条件下稳定,易被H2还原。
①Fe电极反应式为________。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______________。
③当阴极产生112mL(标准状况)的气体时,通过阴离子交换膜的离子有_______mol。
-
钴、镍与铁是同族元素,主要化合价均为+2、+3价,它们的单质及化合物的性质有很多相似之处。试回答下列问题:
(1) 氯化铁溶液呈__________ (填“酸”“中”或“碱”)性,原因是___________ (用离子方程式表示)。
(2) 将Co3O4与浓盐酸混合,可生成黄绿色气体。写出该反应的化学方程式: ________。
(3) Co2+和Fe3+均可与KSCN溶液发生相似的反应,向CoCl2溶液中加入KSCN溶液,生成某种蓝色离子,该离子中钴元素的质量分数约为20%。则该离子的化学式为___________。
(4) 为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下实验装置。

丙装置中充入滴有酚酞的氯化钠溶液,X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。可知三种金属的活动性由强到弱的顺序是__________(填元素符号) 若起始时装置丙中有1 L 1.5 mol·L−1氯化钠溶液,一段时间后,a处收集到1.12 L H2(标准状况),忽略溶液体积的变化,装置丙中所有离子的浓度由大到小的顺序为___________。
-
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等
(1)编号为⑤的元素的符号为______,其在周期表中位于______.
(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:______.
(3)己知AlCl3的熔点为190℃(2.5×105Pa),沸点为182.7℃,试推测:
①BeCl2是______化合物(填“离子”或“共价”),②Be(OH)2的碱性比LiOH______.
(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为______(用化学式表示).

-
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;下图是元素周期表的一部分,编号为③的元素最外层与最内层电子数等

(1)编号为⑤的元素的符号为________,其在周期表中位于________。
(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:________。
(3)己知AlCl3的熔点为190 ℃(2.5×105Pa),沸点为182.7℃,
试推测:
①BeCl2是化合物(填“离子”或“共价”),
②Be(OH)2的碱性比LiOH ________。
(4)根据Mg在空气中的燃烧情况, Li在空气中燃烧生成的产物为__(用化学式表示)。
-
砹(At)是原子序数最大的ⅦA元素,试根据同族元素性质的相似性和递变性分析,下列各个推论,其中错误的是( )
A.HAt很稳定
B.AgAt既不溶于水也不溶于硝酸
C.砹单质易溶于有机溶剂
D.砹单质在常温、常压下是固体
-
下列说法不正确的是( )
A.同族元素在性质上的相似性,取决于原子价电子排布的相似性
B.电离能越小,表示气态时该原子越易失去电子
C.元素的电负性越大,表示其原子在化合物中吸引电子能力越强
D.电负性大的元素易呈现正价,电负性小的元素易呈现负价
-
下列有关物质性质的比较正确的是 ( )
①同主族元素的单质从上到下,非金属性减弱,熔点增高
②元素的最高正化合价在数值上等于它所在的族序数
③同周期主族元素的原子半径越小,越难失去电子
④元素的非金属性越强,它的气态氢化物水溶液的酸性越强.
⑤还原性:S2->Se2->Br->Cl-⑥酸性:HClO4>H2SO4>H3PO4>H2SiO3
A.①③ B.②④ C.③⑥ D.⑤⑥
-
周期表中同族元素单质及其化合物在许多性质上都存在着递变规律,随着原子序数的递增,下列有关说法正确的是
A.IA族,单质的熔点逐渐降低 B.ⅥA族,对气态氢化物还原性逐渐增强
C.VA族氢化物的沸点逐渐升高 D.ⅣA族最高氧化物对应水化物的酸性逐渐增强
-
同族元素所形成的同一类型的化合物,其结构和性质往往相似。化合物PH4I是一种白色晶体,下列对它的描述中正确的是( )
A.它是一种共价化合物 B.它受热时,可能会分解产生有色气体
C.这种化合物不能跟碱反应 D.它只含共价键,不含离子键




