-
钴、镍与铁是同族元素,主要化合价均为+2、+3价,它们的单质及化合物的性质有很多相似之处。试回答下列问题:
(1) 氯化铁溶液呈__________ (填“酸”“中”或“碱”)性,原因是___________ (用离子方程式表示)。
(2) 将Co3O4与浓盐酸混合,可生成黄绿色气体。写出该反应的化学方程式: ________。
(3) Co2+和Fe3+均可与KSCN溶液发生相似的反应,向CoCl2溶液中加入KSCN溶液,生成某种蓝色离子,该离子中钴元素的质量分数约为20%。则该离子的化学式为___________。
(4) 为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下实验装置。

丙装置中充入滴有酚酞的氯化钠溶液,X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。可知三种金属的活动性由强到弱的顺序是__________(填元素符号) 若起始时装置丙中有1 L 1.5 mol·L−1氯化钠溶液,一段时间后,a处收集到1.12 L H2(标准状况),忽略溶液体积的变化,装置丙中所有离子的浓度由大到小的顺序为___________。
-
钴、镍与铁是同族元素,它们的单质及化合物的性质有很多相似之处。
(1) 为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下甲、乙、丙三个实验装置。丙装置中X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。

①甲池Fe电极反应式为_________。由现象可知三种金属的活动性由强到弱的顺序是__________(填元素符号) 。
②写出丙装置中反应的离子方程式____________________。
(2)Na2FeO4具有广泛用途,可通过电解法制取得到,工作原理图丁所示。通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。已知: Na2FeO4只在强碱性条件下稳定,易被H2还原。
①Fe电极反应式为________。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______________。
③当阴极产生112mL(标准状况)的气体时,通过阴离子交换膜的离子有_______mol。
-
钴、镍与铁是同族元素,它们的单质及化合物的性质有很多相似之处。
(1) 为了比较Fe、Co、Cu三种金属的活动性,某实验小组设计如下甲、乙、丙三个实验装置。丙装置中X、Y均为石墨电极。反应一段时间后,可观察到甲装置中Co电极附近产生气泡,丙装置中X极附近溶液变红。
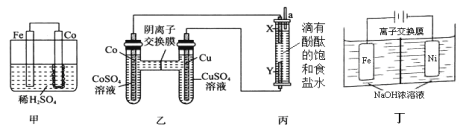
①甲池Fe电极反应式为_________。由现象可知三种金属的活动性由强到弱的顺序是__________(填元素符号) 。
②写出丙装置中反应的离子方程式____________________。
(2)Na2FeO4具有广泛用途,可通过电解法制取得到,工作原理图丁所示。通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。已知: Na2FeO4只在强碱性条件下稳定,易被H2还原。
①Fe电极反应式为________。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______________。
③当阴极产生112mL(标准状况)的气体时,通过阴离子交换膜的离子有_______mol。
-
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;如图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等
(1)编号为⑤的元素的符号为______,其在周期表中位于______.
(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:______.
(3)己知AlCl3的熔点为190℃(2.5×105Pa),沸点为182.7℃,试推测:
①BeCl2是______化合物(填“离子”或“共价”),②Be(OH)2的碱性比LiOH______.
(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为______(用化学式表示).

-
短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;下图是元素周期表的一部分,编号为③的元素最外层与最内层电子数等

(1)编号为⑤的元素的符号为________,其在周期表中位于________。
(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:________。
(3)己知AlCl3的熔点为190 ℃(2.5×105Pa),沸点为182.7℃,
试推测:
①BeCl2是化合物(填“离子”或“共价”),
②Be(OH)2的碱性比LiOH ________。
(4)根据Mg在空气中的燃烧情况, Li在空气中燃烧生成的产物为__(用化学式表示)。
-
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用.请回答下列问题:
(1)32号元素Ge的原子核外电子排布式为______.
(2)C、Si、Sn三种元素的单质中,能够形成金属晶体的是______.
(3)已知SnO2是离子晶体,写出其主要物理性质______(写出2条即可).
(4)已知:
| CH4 | SiH4 | NH3 | PH3 |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是______.
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是______.
结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时______先液化.
-
钛被称为继铁、铝之后的第三金属,其单质及化合物在航天、军事、航海、医疗等领域都有着重要的应用。请回答下列问题:
(1)在元素周期表中,锆元素与钛元素同族,则锆元素位于__区。
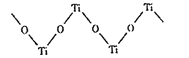
(2)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形成存在的钛酰阳离子,其结构如图所示,若阳离子所带电荷为+n,则该离子中钛原子数为__。
(3)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个Al原子与__个N原子相连,与同一个N原子相连的Al原子构成的立体构型为___,氮化铝晶体属于___晶体。
(4)Ti3+可形成配位数为6的两种配合物晶体(一种是紫色,一种是绿色),组成皆为TiCl3•6H2O。向含有0.01mol绿色配合物晶体的水溶液中加入过量硝酸银溶液,产生0.02molAgCl沉淀,则绿色配合物晶体的化学式为__。
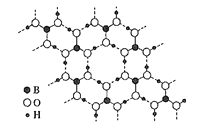
(5)硼与铝同族,硼酸晶体是片层结构,其中一层的结构如图所示,层内的分子以氢键相连。含1mol硼酸的晶体中有__mol氢键。图中所示最外层已达8原子结构的原子是__(填元素符号),H3BO3晶体中B原子个数与极性键个数比为__。
-
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。请回答下列问题。
(1)氮与元素周期表同周期的相邻元素的第一电离能由小到大的顺序为_____________
(2)与阴离子(CN-)互为等电子体的两种分子有______________、____________________
(3)氨水溶液中存在多种氢键,任表示出其中两种_________________、_________________.
(4)H3PO4的K1、K2、K3分别为7.6×10-3、6.3×10-8、4.4×10-13。硝酸完全电离,而亚硝酸K=5.1×10-4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因是______________
②硝酸比亚硝酸酸性强的原因是______________
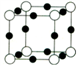
(5)X+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示。X的核外电子排布式为_________________与同一个N3-相连的X+有_____ 个。
(6)X的高价阳离子(X2+)在水溶液中存在离子[X(H2O)4]2+,则X2+与H2O之间的键型为________________该化学键能形成的原因是___________________请画出[X(H2O)4]2+离子的结构式(用元素符号写结构式)__________________。
-
碳族元素的单质及其化合物是一类重要物质。请回答下列问题:
(1)锗(Ge)是用途很广的半导体材料,基态Ge原子的核外电子中,有_____个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是________________________________________。
(3)GeCl4可水解生成一种氧化物和一种无氧酸,其化学反应方程式为:_______________。
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是____________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为______,微粒之间存在的作用力是_______。
(6)合成氮化碳是一种硬度比金刚石还大的晶体,氮化碳的晶体类型为________,该晶体中微粒间的作用力是____________。
(7)COCl2俗称光气,分子中C原子采取sp2杂化成键,光气分子的结构式为____________,其中碳氧原子之间共价键是________(填序号)。
a.2个σ键b.2个π键c.1个σ键,1个π键
(8) CaC2中C22−与O22+互为等电子体,O22+的电子式可表示为________。
-
下列说法不正确的是( )
A.同族元素在性质上的相似性,取决于原子价电子排布的相似性
B.电离能越小,表示气态时该原子越易失去电子
C.元素的电负性越大,表示其原子在化合物中吸引电子能力越强
D.电负性大的元素易呈现正价,电负性小的元素易呈现负价







