-
A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)A在元素周期表中的位置是____________。
(2)下列事实能用元素周期律解释的是(填字母序号)________。
a. D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是____________。
(4)①工业上用电解法制备D的单质,反应的化学方程式为____________。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为________。
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理。上述反应的离子方程式为____________。
高三化学填空题中等难度题查看答案及解析
-
A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)A在元素周期表中的位置是____________。
(2)下列事实能用元素周期律解释的是(填字母序号)________。
a. D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是____________。
(4)①工业上用电解法制备D的单质,反应的化学方程式为____________。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为________。
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理。上述反应的离子方程式为____________。
高三化学填空题中等难度题查看答案及解析
-
A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)E在元素周期表中的位置是____________。A与E组成的化合物是常用的溶剂,写出其电子式__________________
(2)下列事实能用元素周期表相应规律解释的是(填字母序号)____________。
a.D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b.E的气态氢化物的稳定性小于HF
c.A的单质能与二氧化硅高温下制得粗品硅单质
(3)WE3的溶液可用于刻蚀铜制的印刷电路板,反应的离子方程式为______。
(4)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理,上述反应的离子方程式为______________。上述W的氧化物X能与D的单质反应,写出该反应的化学方程式为____________________。
高三化学综合题中等难度题查看答案及解析
-
已知X、Y、Z、W是中学常见的四种元素,原子序数依次增大。X的原子最外层电子数是次外层的2倍,Y 的氧化物属于两性氧化物,Y、Z 位于同周期,X、Y、Z的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)X在元素周期表中的位置是_________________。
(2)下列事实能用元素周期律解释的是_____________________________________(填字母序号)。
A.Y 的最高价氧化物对应水化物的碱性弱于Mg(OH)2
B.Z的气态氢化物的稳定性小于HF
C.WZ3的溶液可用于刻蚀铜制的印刷电路板
(3)Z的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是______________________。
(4)工业上用电解法制备Y单质,化学方程式为___________________________。
(5)家用“管道通”的有效成分是烧碱和Y 的单质,使用时需加入一定量的水,此时发生反应的化学方程式为______________________________。
(6)W的单质可用于处理酸性废水中的NO3-,使其转化成为铵根离子,同时生成磁性的W的氧化物H,再进行后续处理。相应离子方程式为____________。Y 的单质与H在高温下反应的化学方程式为_________。
高三化学推断题中等难度题查看答案及解析
-
X、Y、Z、W是中学常见的四种短周期元素,其原子序数依次增大,且原子核外最外层电子数都不少于2 ,X族序数与最外层电子数相等。四种元素的单质均能在氧气中燃烧,生成四种相对分子质量都大于26的氧化物,其中有两种氧化物能溶于稀硫酸,三种能溶于烧碱溶液。四种元素单质的混合物有如下性质:
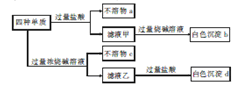
下列说法正确的是
A. 原子半径:X>Y>Z>W
B. 简单气态氢化物的热稳定性:W>X
C. 最高价氧化物对应的水化物的碱性:Z>Y
D. X和W组成的化合物常作砂纸、砂轮的磨料
高三化学选择题困难题查看答案及解析
-
X、Y、Z、W是中学常见的四种短周期元素,其原子序数依次增大,且原子核外最外层电子数都不少于2,X与W的最外层电子数相等。四种元素的单质均能在氧气中燃烧,生成四种相对分子质量都大于26的氧化物,其中有两种氧化物能溶于稀硫酸,三种氧化物能溶于烧碱溶液。四种元素的单质所形成的混合物有如下性质:

下列说法正确的是
A.原子半径:X>Y>Z>W
B.简单的气态氢化物的热稳定性:W>X
C.最高价氧化物对应水化物的碱性:Z>Y
D.X和W组成的化合物常作砂纸、砂轮的磨料
高三化学单选题中等难度题查看答案及解析
-
a、b、c、d是四种原子序数依次增大的短周期元素。a原子的电子层数为n,核内质子数是2n2—1,最外层电子数为2n+l;b、d同主族,能形成两种中学常见的化合物;c与b组成的化合物是一种两性氧化物,工业上通过电解该化合物可冶炼c单质;e原子有四个能层,其未成对电子数在同周期是最多的。回答下列问题:
(1)a在周期表中的位置 ;e的基态原子价电子排布式为 。
(2)b、c、d原子的第一电离能由大到小的顺序是 。
(3)a和b形成的离子W呈平面正三角形,其中心原子的杂化类型为 ;a、b、d 气态氢化物最稳定的是 (写化学式)。
(4)元素c与Fe构成合金的晶胞如图,该合金的化学式为 。
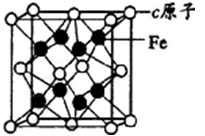
(5)将b、d组成的极性分子通人含少量W离子的BaCl2水溶液中,有NO气体生成。发生反应的离子方程式为
高三化学填空题困难题查看答案及解析
-
a、b、c、d是四种原子序数依次增大的短周期元素。a原子的电子层数为n,核内质子数是2n 2—1,最外层电子数为2n+l;b、d同主族,能形成两种中学常见的化合物;c与b组成的化合物是一种两性氧化物,工业上通过电解该化合物可冶炼c单质;e原子有四个能层,其未成对电子数在同周期是最多的。回答下列问题:
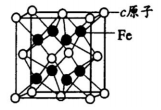
(l)a在周期表中的位置 ;e的基态原子价电子排布式为 。
(2)b、c、d原子的第一电离能由大到小的顺序是 (用元素符号回答)。
(3)a和b形成的离子W呈平面正三角形,其中心原子的杂化类
型为 ;a、b、d气态氢化物最稳定的是 (写化学式)。
(4)元素c与Fe构成合金的晶胞如图,该合金的化学式为 。
(5)将b、d组成的极性分子通入含少量W离子的BaCl2水溶液中,有NO气体生成。发生反应的离子方程式为 .。
高三化学填空题困难题查看答案及解析
-
短周期主族元素甲、乙、丙、丁、戊的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,甲和丙同主族,丁原子最外层电子数与电子层数相等,在中学常见的酸中戊的最髙价氧化物对应的水化物的酸性最强。下列叙述错误的是( )
A. 氧元素与甲、乙、丙形成的二元化合物均只有两种
B. 简单离子半径:戊 >乙>丙>丁
C. 甲、乙、戊三种元素可形成含有共价键的离子化合物
D. 丙、丁、戊三种元素的最高价氧化物对应的水化物两两之间均能发生反应
高三化学选择题困难题查看答案及解析
-
短周期元素A、B、C、D、E的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,A和C同主族,D原子最外层电子数与电子层数相等,在中学常见的酸中E的最高价氧化物对应的水化物的酸性最强。下列叙述正确的是( )
A. 氧元素与A、B、C形成的二元化合物均只有两种
B. 简单离子半径:E>C>D>B
C. 由A、B、E三种元素只能形成含有共价键的共价化合物
D. C、D、E三种元素的最高价氧化物对应的水化物两两之间均能发生反应
高三化学单选题中等难度题查看答案及解析