-
氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.001 mol·L-1KMnO4酸性溶液滴定未知浓度的无色NaHSO3溶液。反应的离子方程式是:2MnO4-+5HSO3-+H+=2Mn2++5SO42-+3H2O
回答下列问题:
(1)用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液;
(2)该滴定实验选用何种指示剂,说明理由____________________(如无需加入指示剂也请说明理由);
(3)滴定前平视KMnO4溶液液面,刻度为a mL,滴定后俯视液面刻度为b mL,则根据(b-a)mL计算得到的待测浓度,比实际浓度________(填“大”或“小”)。
-
氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.001 mol·L-1 KMnO4酸性溶液滴定未知浓度的无色NaHSO3溶液。反应的离子方程式是2MnO4-+5HSO3-+H+=2Mn2++5SO42-+3H2O
填空完成问题:
(1)该滴定实验所需仪器有下列中的____________。
A酸式滴定管(50 mL) B碱式滴定管(50 mL) C量筒(10 mL) D锥形瓶 E铁架台 F滴定管夹 G烧杯 H白纸 I胶头滴管 J漏斗
(2)不能用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因________________。
(3)选何种指示剂,说明理由_____________________。
-
氧化还原滴定同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.001 mol·L−1酸性KMnO4溶液滴定未知浓度的无色NaHSO3溶液。反应的离子方程式为2 +5
+5 +H+
+H+ 2Mn2++5
2Mn2++5 +3H2O。
+3H2O。
请完成下列问题:
(1)该滴定实验所需仪器和用品是____________。
A 酸式滴定管(50 mL)B 碱式滴定管(50 mL) C 量筒(10 mL) D 锥形瓶 E 铁架台 F 滴定管夹 G 烧杯 H 白纸 I 胶头滴管 J 漏斗
(2)实验中用_____(填“酸”或“碱”)式滴定管盛装酸性KMnO4溶液,原因是_______。
(3)本实验_______(填“需要”或“不需要”)使用指示剂,滴定终点的现象是__________。
(4)①滴定前平视液面,刻度为a mL,滴定后俯视刻度为b mL,则(b−a) mL比实际消耗KMnO4溶液的体积_____(填“大”或“小”),根据(b−a) mL计算得到的待测液浓度比实际浓度_____(填“高”或“低”)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测液浓度值会____(填“偏小”“偏大”或“不变”)。
-
氧化还原滴定同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.001mol·L-1酸性KMnO4溶液滴定未知浓度的无色NaHSO3溶液。反应的离子方程式为2MnO4-+5HSO3-+H+=2Mn2++5SO42-+3H2O
请完成下列问题:
(1)实验中用___(填“酸”或“碱”)式滴定管盛装酸性KMnO4溶液;
(2)本实验___(填“需要”或“不需要”)使用指示剂,滴定终点的现象是___;
(3)①滴定前平视液面,刻度为amL,滴定后俯视刻度为bmL,则根据(b−a)mL计算得到的待测液浓度值会___(填“偏小”“偏大”或“不变”);
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测液浓度值会___(填“偏小”“偏大”或“不变”)。
-
氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.001 mol·L-1 KMnO4酸性溶液滴定未知浓度的无色NaHSO3溶液。反应离子方程式是2MnO4﹣+5HSO3﹣+H+===2Mn2++5SO42﹣+3H2O填空完成问题:
(1)该滴定实验所需仪器有下列中的____________。
A.酸式滴定管(50 mL)
B.碱式滴定管(50 mL)
C.量筒(10mL)
D.锥形瓶
E.铁架台
F.滴定管夹
G.烧杯
H.白纸
I.胶头滴管
J.漏斗
(2)不能用______(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因_______________。
(3)指示剂 _______ (填“需要”或“不需要”)选用,说明理由_______________________________。
(4)滴定前平视KMnO4溶液液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积________(填“多”或“少”)。根据(b-a)mL计算得到的待测浓度,比实际浓度________(填“大”或“小”)。
-
(8分)氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之).现有0.001mol/L酸性KMnO4和未知浓度的无色NaHSO3溶液,反应离子方程式是2MnO4- + 5HSO3- + H+ ==2Mn2+ + 5SO42- + 3H2O 填空回答问题:
(1)该滴定实验所需仪器有下列中的______________________________(填序号)
A.酸式滴定管 B.碱式滴定管 C.量筒 D.锥形瓶 E.铁架台 F.滴定管夹 G.烧杯 H.白纸 I.胶头滴管 J.漏斗
(2)滴定前平视KMnO4溶液,刻度为a mL,若滴定后(终点)俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积_________( 多、少)。根据(b-a)mL计算得到的待测液浓度比实际的浓度_________(大、小)。
-
氧化还原滴定同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.0010 mol·L−1酸性KMnO4溶液滴定未知浓度的无色NaHSO3溶液,反应的离子方程式为2 +5
+5 +H+=2Mn2++5
+H+=2Mn2++5 +3H2O。请完成下列问题:
+3H2O。请完成下列问题:
(1)该实验除了滴定管(50 mL)、铁架台、滴定管夹、烧杯 、白纸等仪器和用品外,还必须使用的仪器是____________。
(2)实验中用_____(填“酸”或“碱”)式滴定管盛装酸性KMnO4溶液,原因是_______。
(3)本实验_______(填“需要”或“不需要”)使用指示剂,滴定终点的现象是__________。
(4)①滴定前平视液面,刻度为a mL,滴定后俯视刻度为b mL,根据(b−a) mL计算得到的待测液浓度比实际浓度_____(填“高”或“低”)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测液浓度值会____(填“偏小”“偏大”或“不变”)。
-
氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.1000 mol·L-1KMnO4酸性溶液滴定未知浓度的无色H2C2O4溶液,反应离子方程式是:2MnO4-+5H2C2O4+6H+===2Mn2++CO2↑+8H2O。
填空完成问题:
(1)该滴定实验所需的玻璃仪器有______________。
A酸式滴定管(50 mL) B碱式滴定管(50 mL) C量筒(50 mL) D锥形瓶 E烧杯
(2)不用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因________________。
(3)滴定终点的现象为__________________________。
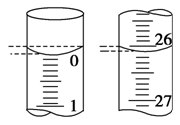
(4)若滴定开始和结束时,滴定管中的液面下图所示,则起始读数为________mL,终点读数为________mL。
(5)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测H2C2O4溶液的体积/mL | 0.1000 mol·L-1 KMnO4的体积/mL |
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL |
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
| | | | |
依据上表数据列式计算该H2C2O4溶液的物质的量浓度_________。
(6) 下列操作中可能使测定结果偏低的是________(填字母)。
A.酸式滴定管未用标准液润洗就直接注入KMnO4标准液
B.滴定前盛放草酸溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴部分在滴定前没有气泡,滴定后有气泡
D.读取KMnO4标准液时,开始仰视读数,滴定结束时俯视读数
-
氧化还原滴定实验同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现有0.01 mol·L-1KMnO4酸性溶液和未知浓度的无色NaHSO3溶液。反应离子方程式是2MnO4-+5HSO3-+H+ 2Mn2++5SO42-+3H2O。填空回答问题:
2Mn2++5SO42-+3H2O。填空回答问题:
(1)滴定过程中用到的玻璃仪器除了酸式滴定管、碱式滴定管外还缺少_____________________
(2)不用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因:
(3)选何种指示剂,说明理由 ,到达终点时颜色变化
(4)当用酸滴定碱时,下列操作使测定结果(碱的浓度)偏高的是
① 酸式滴定管滴至终点,俯视读数
② 碱液移入锥形瓶后,加入10mL蒸馏水
③ 酸式滴定管注入酸溶液后,尖嘴有气泡时便开始滴定,滴定后无气泡
④ 酸式滴定管用蒸馏水润洗后,未用标准液润洗
(5)有关数据记录如下:
| 实验序号 | 待测液体积(mL) | 所消耗KMnO4酸性溶液的体积(mL) |
| 滴定前 | 滴定后 |
| 1 | 20.00 | 0.50 | 20.60 |
| 2 | 20.00 | 6.00 | 25.90 |
| 3 | 20.00 | 1.40 | 24.20 |
| | | |
则NaHSO3溶液的物质的量浓度为______________mol/L。
-
氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO3溶液的浓度,现用0.1000mol/L的酸性KMnO4溶液进行滴定,回答下列问题:
(1)配平离子方程式:________MnO4-+________HSO3-+________H+--________Mn2++________SO42-+________H2O
(2)滴定过程中,NaHSO3溶液的体积是20.00mL,消耗0.100mol/L的酸性KMnO4溶液16.00mL,则NaHSO3溶液的物质的量浓度是________ mol/L.
+5
+H+
2Mn2++5
+3H2O。
