-
乙炔、乙烯均是重要的化工原料。回答下列问题:
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)═C2H4(g)△H1=-174.3kJ·mol—1
K1(300K)=3.37×1024
C2H2(g)+2H2(g)=C2H6(g)△H2═-311.0kJ·mol一l
K2(300K)═1.19×1042
则反应C2H4(g)+H2(g)═C2H6(g)的△H=___kJ·mol一1,K(300K)=__(保留三位有效数字)。
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。
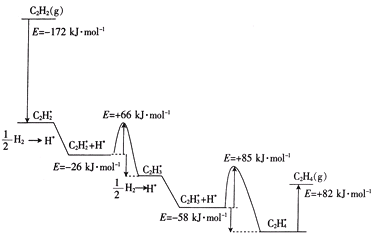
上述吸附反应为____(填“放热”或“吸热”)反应,该历程中最大能垒(活化能)为____kJ·mol-1,该步骤的化学方程式为____。
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g)⇌C2H2(g)+H2(g)。乙烯的离解率为a,平衡时容器内气体总压强为P总,则分压p(C2H4)═___(用p总和a表示)。
(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。
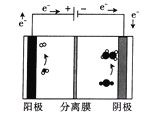
该分离膜为___(填“阳”或“阴”)离子选择性交换膜;生成乙烯的电极反应式为___。
-
乙炔、乙烯均是重要的化工原料。回答下列问题:
(1)1902年,Sabatier首次发现,常压下过渡金属可以催化含有双键或叁键的气态烃的加氢反应。
①已知:C2H2(g)+H2(g)═C2H4(g)△H1=-174.3kJ·mol—1
K1(300K)=3.37×1024
C2H2(g)+2H2(g)=C2H6(g)△H2═-311.0kJ·mol一l
K2(300K)═1.19×1042
则反应C2H4(g)+H2(g)═C2H6(g)的△H=___kJ·mol一1,K(300K)=__(保留三位有效数字)。
②2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图)。其中吸附在Pd表面上的物种用*标注。
上述吸附反应为____(填“放热”或“吸热”)反应,该历程中最大能垒(活化能)为____kJ·mol-1,该步骤的化学方程式为____。
(2)在恒容密闭容器中充入乙烯,一定条件下发生反应C2H4(g)⇌C2H2(g)+H2(g)。乙烯的离解率为a,平衡时容器内气体总压强为P总,则分压p(C2H4)═___(用p总和a表示)。
(3)用如图装置电解含CO2的某酸性废水溶液,阴极产物中含有乙烯。

该分离膜为___(填“阳”或“阴”)离子选择性交换膜;生成乙烯的电极反应式为___。
-
乙炔加氢是乙烯工业中的重要精制反应,利用这一反应可以将乙烯产品中的乙炔含量降低,以避免后续乙烯聚合催化剂的中毒,工业上称为碳二加氢过程。
已知:I. 
 ;
;
II. 
 ;
;
回答下列问题:
(1)已知几种化学键的键能如表所示:
| 化学键 | 
| 
| 
| 
|
| 键能/ | 436 | 413.4 | 615 | 812 |
 =____________
=____________ 。
。
(2)400K时,在密闭容器中将等物质的量的 和
和 混合,采用适当的催化剂进行反应,生成
混合,采用适当的催化剂进行反应,生成 ,达到平衡时测得
,达到平衡时测得 ,则平衡时
,则平衡时 _____
_____ 。
。
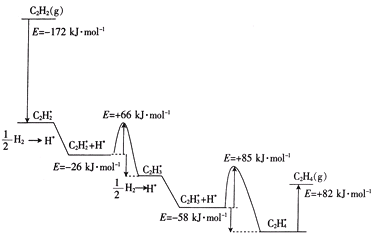
(3)据前人研究发现乙炔在 团簇表面催化加氢反应的部分历程如图所示,其中吸附在
团簇表面催化加氢反应的部分历程如图所示,其中吸附在 表面上的物种用*标注。
表面上的物种用*标注。

推测乙烯在 表面上的吸附为__________(填“放热”或“吸热”)过程。图中历程中最大能垒(活化能)E正=______
表面上的吸附为__________(填“放热”或“吸热”)过程。图中历程中最大能垒(活化能)E正=______ ,该步骤的化学方程式为___________。
,该步骤的化学方程式为___________。
(4) 时,将体积比为1:2的
时,将体积比为1:2的 和
和 充入刚性密闭容器中,加入催化剂发生反应Ⅱ,起始体系总压强为
充入刚性密闭容器中,加入催化剂发生反应Ⅱ,起始体系总压强为 ,实验测得
,实验测得 的分压
的分压 与反应时间
与反应时间 的关系如图所示:
的关系如图所示:
① 时,
时, 内,平均反应速率
内,平均反应速率 ______
______ (用含
(用含 的代数式表示,下同)。
的代数式表示,下同)。
② 时,该反应的化学平衡常数
时,该反应的化学平衡常数 _____
_____ (
( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
③ 时,
时, 内,
内, 的减小量______(填“>”“<”或“=”)
的减小量______(填“>”“<”或“=”)  内
内 的减小量,理由为__________。
的减小量,理由为__________。
-
乙炔和乙烯都是基本的重要有机化工原料。由它们和常见的有机物可合成一种醚类香料和制备聚乙烯醇缩丁醛。具体合成路线如图所示(部分反应条件和产物略去):
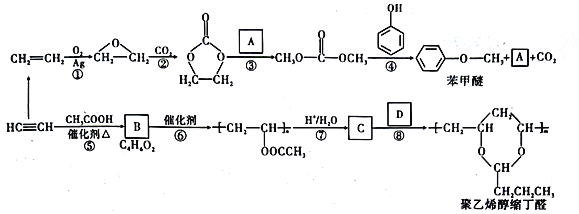
已知以下信息:
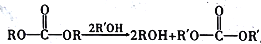 。
。
回答下列问题:
(1)A的名称是_________________,D中含有的官能团名称是________________________。
(2)B的结构简式为__________________。聚乙烯醇缩丁醛的分子式为_________________________。
(3)⑦的反应类型是__________________________。
(4)写出反应③的化学方程式:_____________________________________。
(5)M 与碳酸二甲酯( )互为同系物,满足下列条件的M 的同分异构体共有______种。其中核磁共振氢谱有3组峰,峰面积之比为3 :2 :3,该同分异构体的结构简式为________________。
)互为同系物,满足下列条件的M 的同分异构体共有______种。其中核磁共振氢谱有3组峰,峰面积之比为3 :2 :3,该同分异构体的结构简式为________________。
①相对分子质量比碳酸二甲酯多14;
②酸性条件下能发生水解,且水解后的产物不含 结构;
结构;
③分子中不含醚键结构( )。
)。
(6)参照上述合成路线,设计一条由2-氯丁烷和必要的无机试剂制备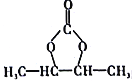 的合成路线(注明必要的反应条件)。___________________
的合成路线(注明必要的反应条件)。___________________
-
以有机物A为原料合成聚合物PMA和聚碳酸酯PC的路线如下:

回答下列问题:
(1)下列关于高分子化合物的说法中正确的是________。(填标号)
a.聚乙烯分子中含有碳碳双键
b.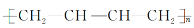 的单体是2-丁炔
的单体是2-丁炔
c.棉花、羊毛和蚕丝是天然纤维
d.CuSO4溶液可使蛋白质变性
(2)A的化学名称是________,C中的官能团名称为_________。
(3)①的反应类型为________,③的反应类型为________。
(4)反应②的化学方程式为_____________________。
(5)B的同系物C5H8O2共有____________种同分异构体(不含立体异构),写出其中核磁共振氢谱为三组峰的物质的结构简式:______________。
(6)参照上述合成路线,以CH3CHO为原料(无机试剂任选),设计制备 的合成路线________________。
的合成路线________________。
-
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:
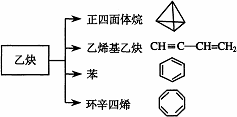
(1)正四面体烷的分子式为 ,其二氯取代产物有________种;
(2)关于乙烯基乙炔分子的说法错误的是:( );
A.能使酸性KMnO4溶液褪色
B.1摩尔乙烯基乙炔能与3摩尔H2发生加成反应
C.乙烯基乙炔分子内含有两种官能团
D.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)① 写出与环辛四烯互为同分异构体,且能使溴水褪色,又属于芳香烃的分子的结构简式:________________________________________;
② 该物质与溴水反应的反应类型是: 。
-
乙炔加氢是乙烯工业中的重要精制反应,利用这一反应可以将乙烯产品中的乙炔含量降低,以避免后续乙烯聚合催化剂的中毒,工业上称为碳二加氢过程。
已知:Ⅰ.CH CH(g)+H2(g)→CH2=CH2(g) ΔH1 K1(400K)=4.2×1022
CH(g)+H2(g)→CH2=CH2(g) ΔH1 K1(400K)=4.2×1022
Ⅱ.CH CH(g)+2H2(g)→CH3CH3(g) ΔH2=-311.4kJ·mol-1 K2(400K)=1.4×1038
CH(g)+2H2(g)→CH3CH3(g) ΔH2=-311.4kJ·mol-1 K2(400K)=1.4×1038
回答下列问题:
(1)已知几种化学键的键能如下表所示:

△H1=___kJ•mol-1。
(2)400K时,在密闭容器中将等物质的量的CH2=CH2(g)和H2(g)混合,采用适当的催化剂进行反应,生成CH3CH3(g),达到平衡时测得 =1016,则平衡时c(H2)=___mol•L-1。
=1016,则平衡时c(H2)=___mol•L-1。
(3)据前人研究发现乙炔在PV团簇表面催化加氢反应的部分历程如图1所示,其中吸附在PV表面上的物种用*标注。
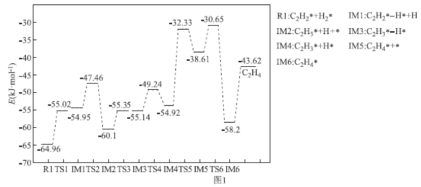
推测乙烯在PV表面上的吸附为___(填“放热”或“吸热”)过程。图1历程中最大能金(活化能)E正=___kJ·mol-1,该步骤的化学方程式为___。
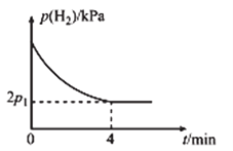
(4)T1℃时,将体积比为1:2的CH≡CH(g)和H2(g)充入刚性密闭容器中,加入催化剂发生反应Ⅱ,起始体系总压强为P0 kPa,实验测得H2的分压(p)与反应时间(t)的关系如图2所示。
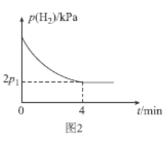
①T1℃时,0~4min内,平均反应速率v(HC≡CH)=___kPa•min-1(用含p0、p1的代数式表示,下同)。
②T1℃时,该反应的化学平衡常数Kp=___kPa-2(Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
③T1℃时,0~2min内p(H2)的减小量___(填“>”“<”或“=”)2~4min内p(H2)的减小量,理由为___。
-
以烃A为原料合成有机化合物M和N的路线如下:
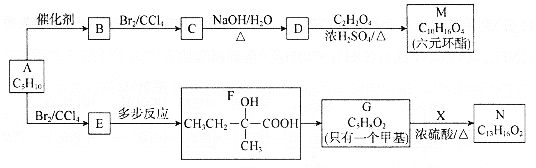
已知:a.在催化剂作用下,烯烃分子间的双键碳原子可以互换而发生烯烃复分解反应: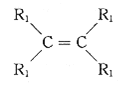 +
+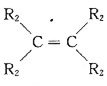
 2
2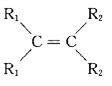
b.X的苯环上有2种等效氢,且只含1个甲基。
回答下列问题:
(1)根据系统命名法,B的名称是________。N中含氧官能团的名称为________。
(2)M的结构简式是________。
(3)F→G的反应类型是________。
(4)写出C→D的化学方程式________。
(5)同时满足下列两个条件的N的同分异构体共有________种;
①能够发生银镜反应且该物质与生成Ag的物质的量之比为1:4;
②苯环上连接—C5H11。
上述同分异构体中,核磁共振氢谱有5组峰且峰面积之比为9:2:2:2:1的有________和________(写结构简式)
(6)写出以CH2=CH(CH2)4CH=CH2为原料制备 的合成路线________(其他试剂任选)
的合成路线________(其他试剂任选)
-
醋酸乙烯(CH3COOCH=CH2)是一种重要的有机化工原料,以二甲醚(CH3OCH3)与合成气(CO、H2)为原料,醋酸锂、碘甲烷等为催化剂,在高压反应釜中一步合成醋酸乙烯及醋酸。回答下列问题:
(1)常温下,将浓度均为a mol/L的醋酸锂溶液和醋酸溶液等体积混合,测得混合液的pH=b,则混合液中c(CH3COO-)=______mol/L( 列出计算式即可)。
(2)合成二甲醚:Ⅰ.2H2(g)+CO(g)=CH3OH(g) ΔH1=-91.8kJ/mol;
Ⅱ.2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ/mol;
Ⅲ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.3 kJ/mol.
已知:H-H 的键能为436kJ/mol,C=O的键能为803kJ/mol,H-O的键能为464kJ/mol,则C≡O的键能为_____kJ/mol.
(3)二甲醚(DME)与合成气一步法合成醋酸乙烯(VAC)的反应方程式为2CH3OCH3(g)+4CO(g)+H2(g)  CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2 molCH3OCH3、0.4 molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2 molCH3OCH3、0.4 molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
①0~10min内,用CO浓度变化表示的平均反应速率v(CO)=______;该温度下,该反应的平衡常数K=__________。
②下列能说明该反应达到平衡状态的是______(填选项字母)。
A、V正(DME)=v逆(H2)≠0 B、混合气体的密度不再变化
C、混合气体的平均相对分子质量不再变化 D、c(CO):c(VAC)=4:1
③如图是反应温度对二甲醚(DME)的转化率和醋酸乙烯(VAC)选择性(醋酸乙烯的选择性Svac= )的影响,该反应的ΔH______0(填“>”“<”或“=”);控制的最佳温度是___________.
)的影响,该反应的ΔH______0(填“>”“<”或“=”);控制的最佳温度是___________.
④保持温度不变,向反应釜中通入氩气增大压强,则化学平衡______(填“向正反应方向”“向逆反应方向"或“不”)移动。

-
醋酸乙烯(CH3COOCH=CH2)是一种重要的有机化工原料,以二甲醚(CH3OCH3)与合成气(CO、H2)为原料,醋酸锂、碘甲烷等为催化剂,在高压反应釜中一步合成醋酸乙烯及醋酸。
回答下列问题:
(1)合成二甲醚:
Ⅰ.2H2(g)+CO(g)=CH3OH(g)ΔH1=-91.8kJ/mol;
Ⅱ.2CH3OH(g)=CH3OCH3(g)+H2O(g)ΔH2=-23.5kJ/mol;
Ⅲ.CO(g)+H2O(g)=CO2(g)+H2(g)ΔH3=-41.3kJ/mol.
已知:H-H的键能为436kJ/mol,C=O的键能为803kJ/mol,H-O的键能为464kJ/mol,则C≡O的键能为_____kJ/mol;
(2)二甲醚(DME)与合成气一步法合成醋酸乙烯(VAC)的反应方程式为2CH3OCH3(g)+4CO(g)+H2(g) CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2molCH3OCH3、0.4molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2molCH3OCH3、0.4molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
①0~10min内,用CO浓度变化表示的平均反应速率v(CO)=______;该温度下,该反应的平衡常数K=__________。
②下列能说明该反应达到平衡状态的是______(填选项字母)。
A.v正(DME)=v逆(H2)≠0
B.混合气体的密度不再变化
C.混合气体的平均相对分子质量不再变化
D.c(CO):c(VAC)=4:1
③保持温度不变,向反应釜中通入氩气增大压强,则化学平衡______(填“向正反应方向”“向逆反应方向"或“不”)移动。
(3)常温下,将浓度均为2.0mol/L的醋酸锂溶液和醋酸溶液等体积混合,测得混合液的pH=8,则混合液中c(CH3COO-)=______mol/L。







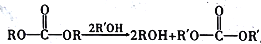 。
。 的合成路线(注明必要的反应条件)。___________________
的合成路线(注明必要的反应条件)。___________________
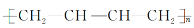 的单体是2-丁炔
的单体是2-丁炔 的合成路线________________。
的合成路线________________。




 +
+

