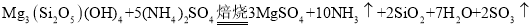-
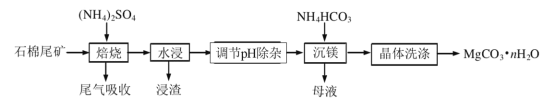
石棉尾矿主要含有Mg3(Si2O5)(OH)和少量的Fe2O3、Al2O3。以石棉尾矿为镁源制备碳酸镁晶体(MgCO3·nH2O)的工艺如图:
已知“焙烧”过程中的主反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
(1)写出焙烧产物NH3的电子式__。
(2)为提高水浸速率,可采取的措施为__(任写一条即可),“浸渣”的主要成分为___。
(3)①“调节pH除杂”时,除去的杂质离子是__,室温下,若要将溶液中的c(Fe3+)降低至4.0×10-11mol/L,则应控制溶液的pH=___(Ksp[Fe(OH)3]=4.0×10-38)。
②“调节pH除杂”时,可以选用的试剂是___。
A.MgO B.NaOH C.MgCO3 D.HNO3
(4)“沉镁”过程中反应的离子方程式为___。“沉镁”时若温度超过60℃,将产生较多的碱式碳酸镁[Mg2(OH)2CO3]杂质,原因是__。
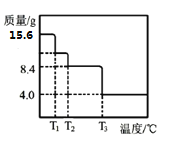
(5)某小组同学称取15.6gMgCO3·nH2O进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则n=__。
-
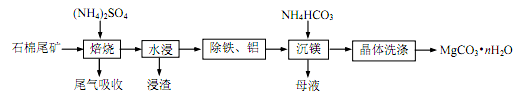
石棉尾矿主要含有 Mg3(Si2O5)(OH)4 和少量的 Fe2O3、Al2O3。以石棉尾矿为镁源制备碳酸镁晶须(MgCO3•nH2O)的工艺如下:
已知“焙烧”过程中的主反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑。
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑。
(1)写出焙烧产物 NH3 的电子式___________。
(2)为提高水浸速率,可采取的措施为________________(任写一条)。“浸渣”的主要成分为_________________。
(3)“除铁、铝”时,需将 pH 调至 8.0 左右,适宜作调节剂的是____(填字母代号)。
a.NaOH b.Mg(OH)2 c.NH3•H2O
(4)“沉镁”过程中反应的离子方程式为______________。“沉镁”时若温度超过 60℃,将产生较多的碱式碳酸镁杂质,原因是_______。
(5)流程中可以循环利用的物质是______(填化学式)。
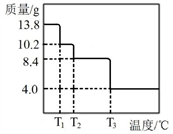
(6)某小组同学称取 13.8 g MgCO3•nH2O 进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则 n=________。
-
石棉尾矿主要含有 和少量的
和少量的 、
、 以石棉尾矿为镁源制备碳酸镁晶体
以石棉尾矿为镁源制备碳酸镁晶体 的工艺如下:
的工艺如下:
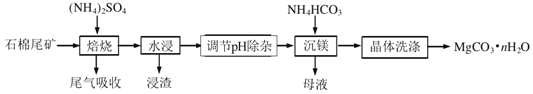
已知“焙烧”过程中的主反应为: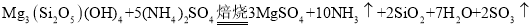
 写出焙烧产物
写出焙烧产物 的电子式______。
的电子式______。
 为提高水浸速率,可采取的措施为______
为提高水浸速率,可采取的措施为______ 任写一条
任写一条 ,“浸渣”的主要成分为____。
,“浸渣”的主要成分为____。
 “调节pH除杂”时,需将pH调至
“调节pH除杂”时,需将pH调至 ,则除去的杂质离子是______,此时溶液中的
,则除去的杂质离子是______,此时溶液中的 ______
______ 已知
已知 。
。
 “沉镁”过程中反应的离子方程式为______。
“沉镁”过程中反应的离子方程式为______。
“沉镁”时若温度超过 ,将产生较多的碱式碳酸镁杂质,原因是______
,将产生较多的碱式碳酸镁杂质,原因是______
 流程中可以循环利用的物质是______
流程中可以循环利用的物质是______ 填化学式
填化学式 。
。
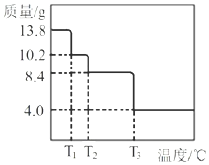
 某小组同学称取
某小组同学称取
 进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则
进行热重分析,并绘制剩余固体质量随温度变化的曲线如图所示,则 ______。
______。
-
氧化镁在易燃材料中常被用作阻燃剂,碳酸镁高温分解法是工业上制备轻质氧化镁的常用方法。镁硅矿主要成分为Mg3(Si2O5)(OH)4和还有少量的Fe2O3、Al2O3等。以镁硅矿为原料制备碳酸镁晶体(MgCO3•nH2O)的生产流程如下:
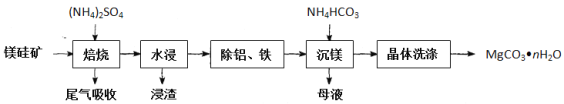
已知“焙烧”过程中的主要反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
(1)Mg3(Si2O5)(OH)4用氧化物的形式表示为___,焙烧产物NH3的电子式为__。
(2)为提高水浸速率,可采取的措施为__(任写一种)。“浸渣”的主要成分为__。
(3)“除铝、铁”时,需将溶液pH调至8.0左右,适宜作调节剂的是__(填字母代号)。
a.Ca(OH)2 b.Mg(OH)2 c.NH3•H2O
(4)“沉镁”过程中反应的离子方程式为__。“沉镁”时若温度超过60℃,将会产生较多的碱式碳酸镁杂质,原因是___。
(5)流程中可以循环利用的物质是___(填化学式)。
(6)为测定产品MgCO3•nH2O中的n值,称取15.6g产品进行充分加热至恒重,冷却,称得固体质量为4g,则n=__。
-
某兴趣小组以一种工业废渣(主要成分为MgCO3、MgSiO3和少量SiO2、Fe的氧化物)为原料制备碳酸镁晶体(MgCO3•3H2O)。实验过程如下:
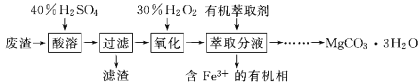
下列说法不正确的是( )
A.为了加快酸溶速率,可将原料进行研磨并适当提高反应温度
B.滤渣的主要成分是H2SiO3和SiO2
C.萃取后,可用KSCN溶液检验水相中是否含有Fe3+
D.萃取后,往水溶液中加入适量的Na2CO3,经过加热蒸发,可得到碳酸镁晶体
-
磷尾矿难溶于水,主要含Ca5(PO4)3F和CaCO3·MgCO3。某研究小组提出了用磷尾矿制备CaCO3、Mg(OH)2、P4和CO的方案,其工艺流程图如下:
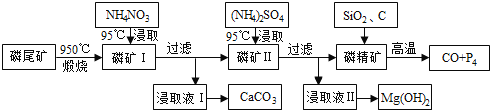
请回答下列问题:
(1)磷精矿[Ca5(PO4)3F]分解温度_______________(填“高于”、“低于” )950℃;
(2)NH4NO3溶液能从磷矿I中浸取出Ca2+的原因是________________,第一次浸取液用NH4NO3而不用的(NH4)2SO4原因是__________________________。
(3)磷精矿与SiO2、C发生反应时被还原的物质是_______________。
(4)其产物CO在工业上有重要的综合应用,现以CO、H2O、熔融Na2O组成的电池装置如图所示。
写出石墨Ⅰ电极上发生反应的电极反应式_______________,Na+向________(填写“石墨Ⅰ”或“石墨Ⅱ”)移动。
(5)CO也可由甲酸(HCOOH)制取,甲酸是易溶于水的一元弱酸。
①常温下关于1 L 0.1 mol·L-1 HCOONa溶液,下列关系不正确的是____________。
a.c(H+)·c(OH-)=1×10-14
b.c(H+)+c(HCOOH)=c(OH-)
c.c(Na+)=c(HCOOH)+c(HCOO-)
d.c(Na+)>c(H+)>c(HCOO-)>c(OH-)
②向1 L 0.1 mol·L-1 HCOONa溶液中加水稀释后,c(HCOOH)·c(OH-)的数值________(填写“增大”“减小”或“不变”)。
-
磷尾矿难溶于水,主要含Ca5(PO4)3F和CaCO3·MgCO3。某研究小组提出了用磷尾矿制备CaCO3、Mg(OH)2、P4和CO的方案,其工艺流程图如下:
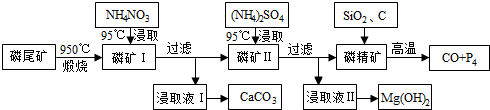
请回答下列问题:
(1)磷精矿[Ca5(PO4)3F]分解温度_______________(填“高于”、“低于” )950℃;
(2)NH4NO3溶液能从磷矿I中浸取出Ca2+的原因是________________,第一次浸取液用NH4NO3而不用的(NH4)2SO4原因是__________________________。
(3)磷精矿与SiO2、C发生反应时被还原的物质是_______________。
(4)其产物CO在工业上有重要的综合应用,现以CO、H2O、熔融Na2O组成的电池装置如图所示。
写出石墨Ⅰ电极上发生反应的电极反应式_______________,Na+向________(填写“石墨Ⅰ”或“石墨Ⅱ”)移动。
(5)CO也可由甲酸(HCOOH)制取,甲酸是易溶于水的一元弱酸。
①常温下关于1 L 0.1 mol·L-1  HCOONa溶液,下列关系不正确的是____________。
HCOONa溶液,下列关系不正确的是____________。
a.c(H+)·c(OH-)=1×10-14
b.c(H+)+c(HCOOH)=c(OH-)
c.c(Na+)=c(HCOOH)+c(HCOO -)
-)
d.c(Na+)>c(H+)>c(HCOO-)>c(OH-)
②向1 L 0.1 mol·L-1 HCOONa溶液中加水稀释后,c(HCOOH)·c(OH-)的数值________(填写“增大”“减 小”或“不变”)。
小”或“不变”)。
-
某工厂废金属屑中主要成分为Cu、Fe和Al(含有少量Al2O3和Fe2O3),某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
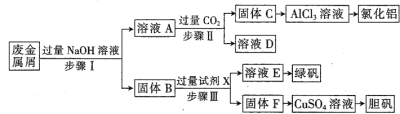
请回答:
(1)胆矾的化学式为___________________。
(2)溶液E为绿色溶液,则试剂X是______________。
(3)步骤I,首先加入温热NaOH溶液,作用是_________;-段时间后,再分批加入常温NaOH溶液,原因是___________。
(4)在步骤II时,用如图装置制取CO2并通入溶液A中。-段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可在a和b间加-个盛有饱和_________溶液的洗气瓶。
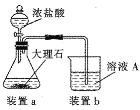
(5)保存FeSO4溶液时,需要滴加少量硫酸溶液,再加入适量_______(填化学式),防止变质。
-
某矿石主要成分有磁铁矿(Fe3O4)、锰矿(MnO2和MnCO3)、氧化铝(Al2O3)、石棉Mg3Si3O7(OH)4等。其中锰矿含量大于磁铁矿含量。工业上将该矿石处理后提取铝的工业流程如下:
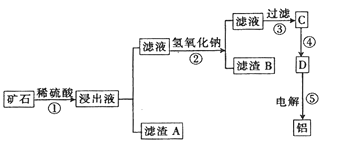
已知:二氧化锰难溶于水、稀硫酸,溶于热浓盐酸。碳酸锰不溶于水,溶于稀硫酸。
(1)MnO2和MnCO3中,Mn元素的化合价分别是_________。
(2)石棉化学式为Mg3Si3O7(OH)4,它与硫酸反应的化学方程式为_________。
(3)滤渣A为____________(填化学式)
(4)步骤②中加入氢氧化钠的作用是_________。
(5)已知不同金属离子生成氢氧化物沉淀所需的pH如表:
| 离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ | Mn2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 9.3 | 7.8 |
| 完全沉淀的pH | 3.7 | 4.7 | 9.6 | 10.8 | 9.8 |
步骤②中加入氢氧化钠调节溶液的pH等于11,则滤渣B的成份是________。
(6)步骤③是往滤液中加入一种物质后过滤,这种物质是__________,过滤操作中使用的玻璃仪器有漏斗、_________;由D电解制备铝的化学方程式为_____________。
-
金属及其化合物在生产中用途广泛。
I.利用生产硼砂的废渣一硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO、CaO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
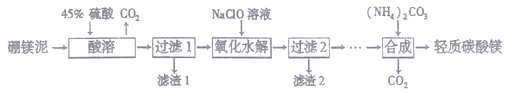
(1)写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式________________________。
(2)滤渣2的主要成分有MnO2和______________,写出生成MnO2的离子方程式___________________。
(3)“合成”时需通蒸汽至80℃,边加热边搅拌,温度不能超80℃的原因是______________。
II.从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
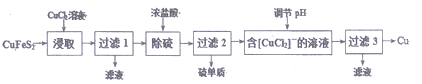
已知:①CuFeS2+3CuCl2=4CuCl↓+FeCl2+2S↓ ②+1价的Cu在酸性条件下易歧化
(4)浸取时,若改用FeCl3溶液,也能生成CuCl和S,该反应化学方程式为_________________。
(5)若过滤1所得滤液中只含FeCl2,则将其在空气中加热蒸干、灼烧后,所得固体的化学式为____________________。
(6)调节溶液的pH后,除生成Cu外,还能产生一种金属离子,此金属离子是______________。(填离子符号)
(7)过滤3所得滤液中的CuCl2可循环使用,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为_______。

3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑