-
氮的氧化物和硫的氧化物是主要的大气污染物,烟气脱硫脱硝是环境治理的热点问题。回答下列问题:
(1)目前柴油汽车都用尿素水解液消除汽车尾气中的NO,水解液中的NH3将NO还原为无害的物质。该反应中氧化剂与还原剂物质的量之比为___。
(2)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO42-。
①KMnO4脱硫(SO2)的离子方程式为___。
②加入CaCO3的作用是___。
③KMnO4/CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为___。
(3)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液pH对脱硫脱硝的影响如图所示:
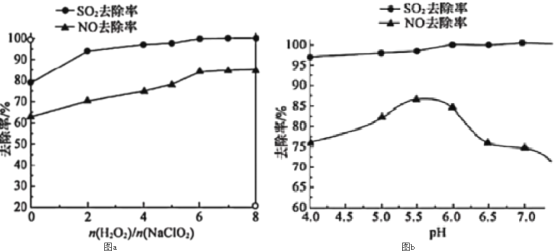
图a和图b中可知脱硫脱硝最佳条件是___。图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因是___。
-
工业废气中的二氧化硫和氮氧化物是大气主要污染物,脱硫脱氮是环境治理的热点问题。回答下列问题:
(1)已知氮及其化合物发生如下反应:
N2(g)+O2(g) 2NO(g) ΔH=+180kJ·mol-1
2NO(g) ΔH=+180kJ·mol-1
N2(g)+2O2(g) 2NO2(g) ΔH=+68kJ·mol-1
2NO2(g) ΔH=+68kJ·mol-1
则2NO(g)+O2(g) 2NO2(g)ΔH___kJ·mol-1。
2NO2(g)ΔH___kJ·mol-1。
(2)利用KMnO4脱除二氧化硫的离子方程式为:___
①□MnO +□SO2+□H2O
+□SO2+□H2O □MnO
□MnO +□ +□ 。(在“□”里填入系数,在“__”上填入微粒符号)
+□ +□ 。(在“□”里填入系数,在“__”上填入微粒符号)
②在上述反应中加入CaCO3可以提高SO2去除率,原因是___。
(3)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
I.CaSO3(s)+SO (aq)
(aq) CaSO4(s)+SO
CaSO4(s)+SO (aq)
(aq)
II.SO (aq)+2NO2(g)+H2O(l)
(aq)+2NO2(g)+H2O(l) SO
SO (aq)+2NO
(aq)+2NO (aq)+2H+(aq)
(aq)+2H+(aq)
浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图所示。
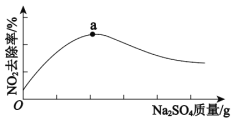
a点后NO2去除率降低的原因是___。
(4)检测烟道气中NOx含量的步骤如下:
I.将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO ;
;
II.加水稀释至100.00mL,量取20.00mL该溶液,与V1mLc1mol·L-1FeSO4标准溶液(过量)充分混合;
III.用c2mol·L-1KMnO4标准溶液滴定剩余的Fe2+,终点时消耗V2mL。
①NO被H2O2氧化为NO 的离子方程式为___。
的离子方程式为___。
②滴定过程中主要使用的玻璃仪器有___和锥形瓶等。
③滴定过程中发生下列反应:
3Fe2++NO +4H+=NO↑+3Fe3++2H2O
+4H+=NO↑+3Fe3++2H2O
MnO +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O
烟气气样中NOx折合成NO2的含量为__mg·m-3。
-
空气质量评价的主要污染物为PM 10、PM2.5、SO2、NO2、O3、CO等物质。烟气的脱硝(除NOx)
技术和脱硫(除SO2)技术都是环境科学研究的热点,选择性催化还原法(SCR)是目前最成熟的烟气脱硝技术,即在催化剂的作用下,用还原剂选择性地与NOx反应生成N2和H2O。
(1)在催化剂存在的条件下,用H2将NO还原为N2。已知:

则氢气和一氧化氮反应生成氮气和水蒸气的热化学方程式是_____________。
(2)用热炭还原NO的反应为2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为T1℃、T1℃、T2℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为T1℃、T1℃、T2℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 | 200 |
| n(NO) /mol(甲容器/T1℃) | 2.00 | 1.50 | 1. 10 | 0.80 | 0.80 | 0. 80 |
| n(NO) /mol(乙容器/T1℃) | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 | 0.40 |
| n(NO) /mol(丙容器/T2℃) | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 | 1.00 |
①该反应T1_________T2,∆H________0 (填“<”或“>”)。
②若乙容器在200min达到平衡状态,则0~ 200min内用CO2的浓度变化表示的平均反应速率v(CO2)=____。
(3)用焦炭还原NO2的反应为2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,lmolNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图18所示:
N2(g)+2CO2(g),在恒温条件下,lmolNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图18所示:
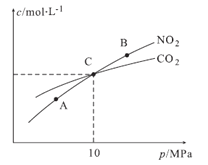
①A、B两点的浓度平衡常数关系:Kc(A)__________ (填“<” 、“>” 或“=”)
②A、B、C三点中NO2的转化率最低的是________(填“A” 、“B” 或“C”)点。
③计算C点时该反应的压强平衡常数Kp(c)=___________(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)在催化剂的作用下,尿素可以与NO2反应生成N2、H2O和CO2。写出CO(NH2)2与NO2反应的化学方程式:___________。
(5)氮的化合物应用广泛。氯胺(NH2Cl)是常用的饮用水二级消毒剂,可作长效缓释消毒剂,已知NH2Cl易水解生成强氧化性的物质,写出NH2Cl与水反应的化学方程式:_______________。
-
空气质量评价的主要污染物为PM10、PM2.5、SO2、NO2、O3和CO等物质。
(1)烟气的脱硝(除NOx)技术和脱硫(除SO2)技术都是环境科学研究的热点。
选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,即在催化剂作用下,用还原剂(如NH3)选择性地与NOx反应生成N2和H2O。
①已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=﹣905.5kJ/mol
N2(g)+O2(g)=2NO(g) △H= +180kJ/mol
则4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H=________
②在催化剂作用下,尿素[CO(NH2)2]也可以将NOx反应生成N2和H2O。写出CO(NH2)2与NO2反应的化学方程式_____________________。
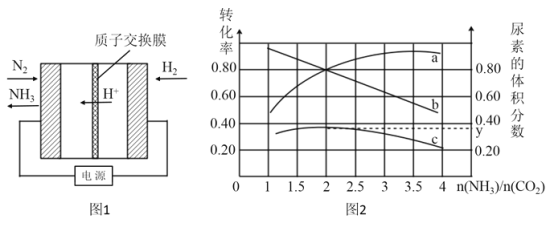
(2)电化学法是合成氨的一种新方法,其原理如图1所示,阴极的电极反应是_____________。
(3)氨碳比[n(NH3)/n(CO2)]对合成尿素[2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(g)]有影响,恒温恒容时,将总物质的量3 mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示。a、b线分别表示CO2或NH3的转化率变化,c线表示平衡体系中尿素的体积分数变化。[n(NH3)/ n(CO2)]=___________时,尿素产量最大;经计算,图中y=____________(精确到0.01)。
CO(NH2)2(g)+H2O(g)]有影响,恒温恒容时,将总物质的量3 mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示。a、b线分别表示CO2或NH3的转化率变化,c线表示平衡体系中尿素的体积分数变化。[n(NH3)/ n(CO2)]=___________时,尿素产量最大;经计算,图中y=____________(精确到0.01)。
(4)废水中含氮化合物的处理方法有多种。
①用次氯酸钠氧化氨气,可以得到N2H4的稀溶液,该反应的化学方程式是__________。
②用H2催化还原法可降低水中NO3-的浓度,得到的产物能参与大气循环,则反应后溶液的pH_________(填“升高”、“降低”或“不变”)。
-
空气质量评价的主要污染物为PM10、PM2.5、SO2、NO2、O3和CO等物质。
(1)烟气的脱硝(除NOx)技术和脱硫(除SO2)技术都是环境科学研究的热点。
选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,即在催化剂作用下,用还原剂(如NH3)选择性地与NOx反应生成N2和H2O。
①已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=﹣905.5kJ/mol
N2(g)+O2(g)=2NO(g) △H= +180kJ/mol
则4NH3(g)+4NO(g)+O2(g)=4N2(g)+6H2O(g) △H=
②在催化剂作用下,尿素[CO(NH2)2]也可以将NOx反应生成N2和H2O。写出CO(NH2)2与NO2反应的化学方程式 。
(2)电化学法是合成氨的一种新方法,其原理如图1所示,阴极的电极反应是 。
(3)氨碳比[n(NH3)/n(CO2)]对合成尿素[2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(g)]有影响,恒温恒容时,将总物质的量3 mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示。a、b线分别表示CO2或NH3的转化率变化,c线表示平衡体系中尿素的体积分数变化。[n(NH3)/ n(CO2)]= 时,尿素产量最大;经计算,图中y= (精确到0.01)。
CO(NH2)2(g)+H2O(g)]有影响,恒温恒容时,将总物质的量3 mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示。a、b线分别表示CO2或NH3的转化率变化,c线表示平衡体系中尿素的体积分数变化。[n(NH3)/ n(CO2)]= 时,尿素产量最大;经计算,图中y= (精确到0.01)。
(4)废水中含氮化合物的处理方法有多种。
①用次氯酸钠氧化氨气,可以得到N2H4的稀溶液,该反应的化学方程式是__________。
②用H2催化还原法可降低水中NO 的浓度,得到的产物能参与大气循环,则反应后溶液的pH (填“升高”、“降低”或“不变”)。
的浓度,得到的产物能参与大气循环,则反应后溶液的pH (填“升高”、“降低”或“不变”)。
-
氮氧化物(主要为NO和NO2)是大气污染物,如何有效地消除氮氧化物污染是目前科学家们研究的热点问题之一。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为___________;用尿素溶液也可吸收氮氧化物,研究表明,氮氧化物气体中NO的体积分数越大,总氮被还原率越低,可能的原因是______。
②在一个体积固定的真空密闭容器中充入等物质的量的CO2和NH3,在恒定温度下使其发生反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示:
CO(NH2)2(s)+H2O(g)并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示:

则A点的v正(CO2)___________(填“>”“<”或“=”)B点的v逆(H2O),原因是________________。
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:2NO(g)+O2(g)=2NO2(g)△H1=akJ·mol-1,NO(g)+O3(g)=NO2(g)+O2(g)△H2=bkJ·mol-1,6NO2(g)+O3(g)===3N2 O5(g)△H3=c kJ·mol-1,则反应4NO2(g)+O2(g)=2N2O5(g)的△H=___________kJ·mol-1。
(3)氮氧化物也可用碱溶液吸收。若NO和NO2混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为_______;已知常温下,Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq) NaNO2(ag)+H2O(1)的平衡常数K=___________,相同物质的量浓度的HNO2、NaNO2混合溶液中,各离子的物质的量浓度由大到小的顺序为___________。
NaNO2(ag)+H2O(1)的平衡常数K=___________,相同物质的量浓度的HNO2、NaNO2混合溶液中,各离子的物质的量浓度由大到小的顺序为___________。
-
氮氧化物(主要为NO和NO2)是大气污染物,如何有效地消除氮氧化物污染是目前科学家们研究的热点问题之一。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为____________;用尿素溶液也可吸收氮氧化物,研究表明,氮氧化物气体中NO的体积分数越大,总氮还原率越低,可能的原因是______________________。
②在一个体积固定的真空密闭容器中充入等物质的量的CO2和NH3,在恒定温度下使其发生反应2NH3(g)+CO2(g)  CO(NH2)2(s)+H2O(g)并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示:
CO(NH2)2(s)+H2O(g)并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示:

则A点的v正(CO2)______________(填“>”“<”或“=”)B点的v逆(H2O),原因是___________________。
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:
2NO(g)+O3(g)=2NO2(g) ΔH1=a kJ·mol-1
NO(g)+O3(g)=NO2(g)+O2(g) △H2=b kJ·mol-1
6NO2(g)+O3(g)=3N2O2(g) ΔH3=c kJ·mol-1
则反应4NO2(g)+O2(g)=2N2O5(g)的ΔH=_____________kJ·mol-1
(3)氮氧化物也可用碱溶液吸收。若NO和NO2混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为____________;已知常温下,Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq)  NaNO2(aq)+H2O(l)的平衡常数K=_______________。
NaNO2(aq)+H2O(l)的平衡常数K=_______________。
-
氮氧化物(主要为NO和NO2)是大气污染物,如何有效地消除氮氧化物污染是目前科学家们研究的热点问题之一。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为___________;用尿素溶液也可吸收氮氧化物,研究表明,氮氧化物气体中NO的体积分数越大,总氮被还原率越低,可能的原因是______。
②在一个体积固定的真空密闭容器中充入等物质的量的CO2和NH3,在恒定温度下使其发生反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示:
CO(NH2)2(s)+H2O(g)并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示:
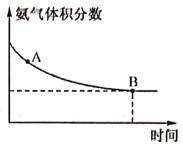
则A点的v正(CO2)___________(填“>”“<”或“=”)B点的v逆(H2O),原因是________________。
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:2NO(g)+O2(g)=2NO2(g)△H1=akJ·mol-1,NO(g)+O3(g)=NO2(g)+O2(g)△H2=bkJ·mol-1,6NO2(g)+O3(g)===3N2 O5(g)△H3=c kJ·mol-1,则反应4NO2(g)+O2(g)=2N2O5(g)的△H=___________kJ·mol-1。
(3)氮氧化物也可用碱溶液吸收。若NO和NO2混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为_______;已知常温下,Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq) NaNO2(ag)+H2O(1)的平衡常数K=___________,相同物质的量浓度的HNO2、NaNO2混合溶液中,各离子的物质的量浓度由大到小的顺序为___________。
NaNO2(ag)+H2O(1)的平衡常数K=___________,相同物质的量浓度的HNO2、NaNO2混合溶液中,各离子的物质的量浓度由大到小的顺序为___________。
-
(13分)SO2是主要大气污染物之一。工业上烟气脱硫的方法如下:

请回答下列问题:
(1)石灰—石膏法的流程如图: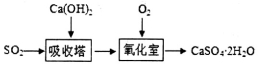 。
。
该法原料便宜,产物有利用价值。写出氧化室中发生反应的化学方程式_______________。
(2)碱法的流程如图: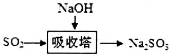 。该法吸收快,效率高。若在操作中持续通入含SO2的烟气,则最终产物X为________。操作过程中测得吸收塔内溶液pH=7,则溶液中含硫微粒的浓度由大到小的顺序为_______________。(已知:
。该法吸收快,效率高。若在操作中持续通入含SO2的烟气,则最终产物X为________。操作过程中测得吸收塔内溶液pH=7,则溶液中含硫微粒的浓度由大到小的顺序为_______________。(已知: )。
)。
(3)工业上在石灰—石膏法和碱法的基础上,结合两种方法的优点,设计出新的脱硫方案如下:


其中物质Y的化学式为_______,转化塔中反应的化学方程式是__________。
(4)最近利用碱法得到产物X的溶液电解制硫酸的工艺己被某些工厂采用。其装置如右图所示(电极为惰性电极)。阴极的电极反应式是__________,透过阴离子交换膜的离子主要为_________。该装置使X转化为硫酸的转化率不会超过________。
-
煤燃烧排放的烟气含有SO2和NOx,大量排放烟气形成酸雨、污染大气,因此对烟气进行脱硫、脱硝,对环境保护有重要意义。回答下列问题:
Ⅰ.利用CO脱硫
(1)工业生产可利用CO气体从燃煤烟气中脱硫,则25℃时CO从燃煤烟气中脱硫的热化学方程式2CO(g)+SO2(g)⇌2CO2(g)+S(s)的焓变△H=_____________。25℃,100kPa时,由元素最稳定的单质生成1mol纯化合物时的反应热称为标准摩尔生成焓,已知一些物质的“标准摩尔生成焓”如下表所示:
| 物质 | CO(g) | CO2(g) | SO2(g) |
| 标准摩尔生成焓∆fHm(25℃)/kJ∙mol-1 | -110.5 | -393.5 | -296.8 |
(2)在模拟脱硫的实验中,向多个相同的体积恒为2L的密闭容器中分别通入2.2mol CO和1mol SO2气体,在不同条件下进行反应,体系总压强随时间的变化如图所示。
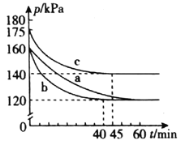
①在实验b中,40 min达到平衡,则0~40 min用SO2表示的平均反应速率v(SO2)=_______。
②与实验a相比,实验b可能改变的条件为_______________,实验c可能改变的条件为_________________。
Ⅱ.利用NH3脱硝
(3)在一定条件下,用NH3消除NO污染的反应原理为:4NH3(g)+6NO(g)⇌5N2(g)+6H2O(l)△H=-1807.98kJ·mol-1。在刚性容器中,NH3与NO的物质的量之比分别为X、Y、Z(其中X<Y<Z),在不同温度条件下,得到NO脱除率(即NO转化率)曲线如图所示。
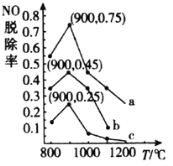
①NH3与NO的物质的量之比为X时对应的曲线为_____________(填“a”“b”或“c”)。
②各曲线中NO脱除率均先升高后降低的原因为__________。
③900℃条件下,设Z= ,初始压强p0,则4NH3(g)+6NO(g)⇌5N2(g)+6H2O(l)的平衡常数Kp=_____________(列出计算式即可)。
,初始压强p0,则4NH3(g)+6NO(g)⇌5N2(g)+6H2O(l)的平衡常数Kp=_____________(列出计算式即可)。
Ⅲ.利用NaCIO2脱硫脱硝
(4)利用NaClO2的碱性溶液可吸收SO2和NO2(物质的量之比为1:1)的混合气体,自身转化为NaCl,则反应的离子方程式为________________。









 。
。 。该法吸收快,效率高。若在操作中持续通入含SO2的烟气,则最终产物X为________。操作过程中测得吸收塔内溶液pH=7,则溶液中含硫微粒的浓度由大到小的顺序为_______________。(已知:
。该法吸收快,效率高。若在操作中持续通入含SO2的烟气,则最终产物X为________。操作过程中测得吸收塔内溶液pH=7,则溶液中含硫微粒的浓度由大到小的顺序为_______________。(已知:


