-
盐X由三种元素组成,其具有良好的热电性能,在热电转换领域具有广阔的应用前景。为研究它的组成和性质,现取12.30g化合物X进行如下实验:
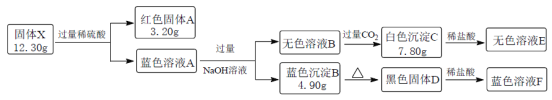
试根据以上内容回答下列问题:
(1)X的化学式为_____________。
(2)无色溶液B中通入过量CO2产生白色沉淀的离子方程式为______________。
(3)蓝色溶液F中通入中SO2气体会产生白色沉淀,该沉淀中氯元素质量分数为35.7%,其离子方程式为____________。
(4)白色沉淀C煅烧的固体产物与D高温反应可生成化合物X,其化学方程式为__________。
-
钛金属重量轻、强度高、有良好的抗腐蚀能力,其单质及其化合物在航空航天、武器装备、能源、化工、冶金、建筑和交通等领域应用前景广阔。回答下列问题:
(1)三氟化钛可用于制取钛氟玻璃,基态 F 原子核外有_____个未成对电子,Ti 原子形成Ti3+时价层电子层排布式为_____。
(2)TiO2 的熔点为 1800℃,TiCl4 的熔点为-25℃,则 TiO2 的晶体类型为_____,TiCl4 熔点低的原因为_____。
(3)钛某配合物可用于催化环烯烃聚合,其结如图所示:
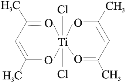
①钛的配位数为_____,该化合物中电负性最大元素是_____(填元素符号)。
②该配合物中不含有的化学键有_____(填字母标号)。
a.离子键 b.σ键 c.金属键 d.π键
(4)已知 TiO2 与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为_____,阳离子中 O 的杂化方式为_____,阴离子的空间构型为_____。
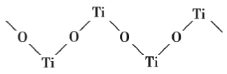
(5)氮化钛可以用于制作电池的材料,其晶胞如图,该晶胞的密度为ρ g·cm-3,与氮原子最近的且距离相等的钛原子有_____个,氮原子与钛原子最近的距离为_____cm。

-
GaN凭借其出色的功率性能、频率性能以及散热性能,在光电领域和高频微波器件应用等方面有广阔的前景。
(1) Johnson等人首次在1100℃下用镓与氨气制得氮化镓,该可逆反应每生成1 mol H2放出10.3 kJ热量。该反应的热化学方程式是_____。(己知金属镓的熔点是29.8℃,沸点是2403℃;氮化镓的熔点为1700℃)
(2)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示(已知图中T1和T2的温度均小于1700℃)。

①下列说法正确的是________(填标号)。
a.相同条件下,Ga(OH)3 的碱性比Al(OH)3强
b.当c(NH3)=c(H2)时,一定达到了化学平衡状态
c. A点和C点化学平衡常数的关系是:KA< KC
d.温度一定时,达平衡后再充入氦气(氦气不参与反应),NH3的转化率增大.
②气相平衡中用组分的平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp),已知在T1℃时体系的压强初始压强为a Pa,则B点的Kp=____(用含a表示且保留2位有效数字)。
(3)电解精炼法提纯镓是工业上常用的方法。具体原理如图所示:

已知:金属的活动性Zn>Ga>Fe>Cu;镓化学性质与铝相似。
①M为电源的_______极,电解精炼镓时产生阳极泥的主要成分是________。
②电解过程中阳极产生的离子迁移到达阴极并在阴极析出高纯镓。请写出电解过程的阴极的电极反应__________。
③电解过程中需控制合适的电压,若电压太高时阴极会产生H2导致电解效率下降。若外电路通过0.2mole时,阴极得到3.5g的镓。则该电解装置的电解效率η=_________(η=生成目标产物消耗的电子数+转移的电子总数)。
-
GaN凭借其出色的功率性能、频率性能以及散热性能,在光电领域和高频微波器件应用等方面有广阔的前景。
(1) Johnson等人首次在1100℃下用镓与氨气制得氮化镓,该可逆反应每生成1 mol H2放出10.3 kJ热量。该反应的热化学方程式是_____。(己知金属镓的熔点是29.8℃,沸点是2403℃;氮化镓的熔点为1700℃)
(2)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示(已知图中T1和T2的温度均小于1700℃)。
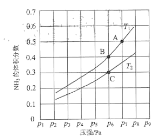
①下列说法正确的是________(填标号)。
a.相同条件下,Ga(OH)3 的碱性比Al(OH)3强
b.当c(NH3)=c(H2)时,一定达到了化学平衡状态
c. A点和C点化学平衡常数的关系是:KA< KC
d.温度一定时,达平衡后再充入氦气(氦气不参与反应),NH3的转化率增大.
②气相平衡中用组分的平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp),已知在T1℃时体系的压强初始压强为a Pa,则B点的Kp=____(用含a表示且保留2位有效数字)。
(3)电解精炼法提纯镓是工业上常用的方法。具体原理如图所示:
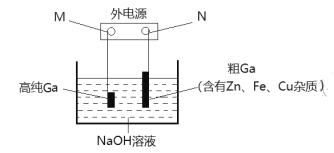
已知:金属的活动性Zn>Ga>Fe>Cu;镓化学性质与铝相似。
①M为电源的_______极,电解精炼镓时产生阳极泥的主要成分是________。
②电解过程中阳极产生的离子迁移到达阴极并在阴极析出高纯镓。请写出电解过程的阴极的电极反应__________。
③电解过程中需控制合适的电压,若电压太高时阴极会产生H2导致电解效率下降。若外电路通过0.2mole时,阴极得到3.5g的镓。则该电解装置的电解效率η=_________(η=生成目标产物消耗的电子数+转移的电子总数)。
-
Fe@Fe2O3纳米线是一种新型铁基材料,在催化、生物医药、环境科学等领域具有广阔应用前景。某研究小组以赤泥(铝土矿提取氧化铝过程中产生的固体废弃物,含SiO2、Fe2O3、Al2O3)为原料,设计下列流程制备Fe@Fe2O3纳米线并探究其在水处理中的应用。
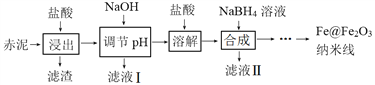
回答下列问题:
(1)“浸出”实验中,盐酸起始浓度对铁、铝浸出率的影响如图所示:
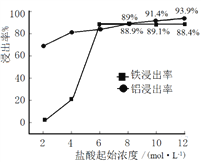
①盐酸的合适浓度为______________。
②盐酸起始浓度为2 mol·L﹣1时,铁的浸出率很低,原因是______________。
(2)已知:25℃时,Al(OH)3(s) AlO2-+ H+ + H2O K=4×10-13。若浸出液c(Al3+) = 0.04 mol·L-1,“调节pH”时,pH最小应为______________(设调节pH过程中溶液体积不变)。
AlO2-+ H+ + H2O K=4×10-13。若浸出液c(Al3+) = 0.04 mol·L-1,“调节pH”时,pH最小应为______________(设调节pH过程中溶液体积不变)。
(3)Fe@Fe2O3纳米线为壳层结构(核是Fe、壳是Fe2O3),壳是由中心铁核在合成过程中被氧化而形成。
①“合成”时滴加NaBH4溶液过程中伴有气泡产生,滤液Ⅱ中含B(OH)3,合成铁核的离子方程式为____________________________。
②“合成”后,经过滤、______________、______________获得Fe@Fe2O3纳米线。
(4)Fe@Fe2O3纳米线去除水体中Cr2O72-的机理是,纳米线将Cr2O72-吸附在表面并还原。在“无氧”和“有氧”条件下将纳米线分别置于两份相同的水体中,80 min后回收该纳米线,测得其表面元素的原子个数比如下表:

①在水体中Fe@Fe2O3纳米线形成的分散系是____________________________。
②样本2的实验条件是______________(填“有氧”或“无氧”)。
③已知水体中检测不到Cr(Ⅲ),样本1中Fe@Fe2O3纳米线的表面Cr(Ⅵ)的去除率为____________________________。
-
氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理,欲在实验室制备氮化铝并检验其纯度。
查阅资料:①实验室用饱和NaNO2与NH4Cl溶液共热制N2:NaNO2+NH4Cl NaCl+N2↑+2H2O。
NaCl+N2↑+2H2O。
②工业制氮化铝:Al2O3+3C+N2 2AlN+3CO,氮化铝在高温下能水解。
2AlN+3CO,氮化铝在高温下能水解。
③AlN与NaOH饱和溶液反应:AlN+NaOH+H2O NaAlO2+NH3↑。
NaAlO2+NH3↑。
Ⅰ.氮化铝的制备

(1)实验中使用的装置如上图所示,请按照氮气气流方向将各仪器接口连接:e→c→d→____________(根据实验需要,上述装置可使用多次)。
(2)B装置内的X液体可能是____;E装置内氯化钯溶液的作用可能是_______。
Ⅱ.氮化铝纯度的测定
【方案ⅰ】甲同学用下图装置测定AlN的纯度(部分夹持装置已略去)。
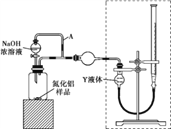
(3)为准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是____。
a.CCl4 b.H2O c.NH4Cl饱和溶液 d.植物油
(4)若装置中分液漏斗与导气管之间没有导管A连通,对所测AlN纯度的影响是____ (填“偏大”“偏小”或“不变”)。
【方案ⅱ】乙同学按以下步骤测定样品中AlN的纯度。

(5)步骤②的操作是_________。
(6)实验室里煅烧滤渣使其分解,除了必要的热源和三脚架以外,还需要的仪器有______等。
(7) 样品中AlN的纯度是__________(用m1、m2、m3表示)。
-
氮化铝(AIN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理,欲在实验室制备氮化铝并检验其纯度。
查阅资料:①实验室用饱和NaNO2与NH4Cl溶液共热制N2: NaNO2+NH4Cl NaCl+N2↑+2H2O。
NaCl+N2↑+2H2O。
②工业制氮化铝:A12O3+3C+N2 2AlN+3CO氮化铝在高温下能水解。
2AlN+3CO氮化铝在高温下能水解。
③ AlN与NaOH饱和溶液反应:AlN+Na0H+H2O=NaAlO2+NH3↑。
一、氮化铝的制备

(1)实验室中使用的装置如上图所示,请按照氮气气流方向将各个衣器接口连接完整:
e→c→d→___________。(根据实验需要,上述装置可使用多次)。
(2)B装置内的X液体可能是_______;E装置内氯化钯溶液的作用可能是________。
二、氮化铝纯度的测定
【方案ⅰ】甲同学用右图装置测定AlN的纯度(部分夹持装置已略去)。
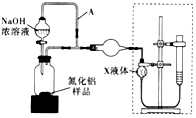
(3)为准确测定生成气体的体积,量气装置(虚线框内)中的X液体可以是____。
a.CC14 b.H2O c.NH4Cl饱和溶液 d.植物油
(4)若装置中分液漏斗与导气管之间没有导管A连通,对所测AIN纯度的影响是______(填“偏大”、“偏小”或“不变”)。
(5)用下列仪器也能组装一套量气装置,其中必选的仪器有_____(选下列仪器的编号)。
a.单孔塞 b.双孔塞 c.广口瓶 d.容量瓶 e.量筒 f.烧杯
【方案ⅱ】 乙同学按以下步骤测定样品中AIN的纯度。

(6)步骤②的操作是__________。
(7)实验室里煅烧滤渣使其分解,除了必要的热源和三脚架以外,还需要的仪器有_____等。
(8)样品中AIN的纯度是_______(用m1、m2、m3 表示)
-
氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理欲在实验室制备氮化铝并检验其纯度。查阅资料:
①实验室用饱和NaNO2溶液与NH4Cl溶液共热制N2:NaNO2+NH4Cl NaCl+N2↑+2H2O。
NaCl+N2↑+2H2O。
②工业制氮化铝:Al2O3+3C+N2高温,2AlN+3CO,氮化铝在高温下能水解。
③AlN与NaOH饱和溶液反应:AlN+NaOH+H2O===NaAlO2+NH3↑。
Ⅰ.氮化铝的制备
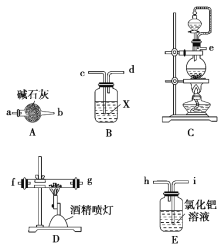
(1)实验中使用的装置如上图所示,请按照氮气气流方向将各仪器接口连接:e→c→d→a→b→____________________(根据实验需要,上述装置可使用多次)。
(2)B装置内的X液体可能是_____________,E装置内氯化钯溶液的作用可能是_____。
Ⅱ.氮化铝纯度的测定
(方案ⅰ)甲同学用如图装置测定AlN的纯度(部分夹持装置已略去)。
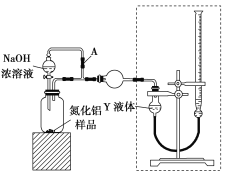
(3)为准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是________。
a.CCl4 b.H2O
c.NH4Cl饱和溶液 d.植物油
(4)若装置中分液漏斗与导气管之间没有导管A连通,对所测AlN纯度的影响是________(填“偏大”“偏小”或“不变”)。
(方案ⅱ)乙同学按以下步骤测定样品中AlN的纯度。
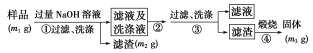
(5)步骤②通入过量________气体。
(6)步骤③过滤所需要的主要玻璃仪器有____________。
-
氮化铝(AlN)是一种性能优异的新型材料,在许多领域有广泛应用,前景广阔。某化学小组模拟工业制氮化铝原理欲在实验室制备氮化铝并检验其纯度。
查阅资料:
①实验室用饱和NaNO2溶液与NH4C1溶液共热制N2:
NaNO2+NH4C1 NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
②工业制氮化铝:Al2O3+3C+N2 2AlN+3CO,氮化铝在高温下能水解。
2AlN+3CO,氮化铝在高温下能水解。
③AlN与NaOH饱和溶液反应:AlN+NaOH+H2O=NaAlO2+NH3↑。
Ⅰ.氮化铝的制备
(1)实验中使用的装置如图所示,请按照氮气气流方向将各仪器接口连接:e→c→d→a→b→__(根据实验需要,上述装置可使用多次)。
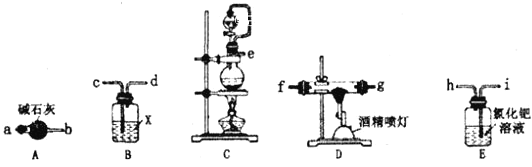
(2)B装置内的X液体可能是__,E装置内氯化钯溶液的作用可能是__。
Ⅱ.氮化铝纯度的测定
方案i:甲同学用如图装置测定AlN的纯度(部分夹持装置已略去)。
(1)为准确测定生成气体的体积,量气装置(虚线框内)中的Y液体可以是__。
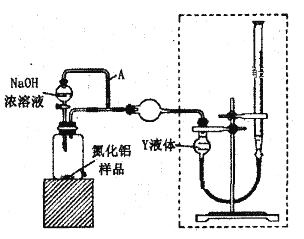
a.CCl4 b.H2O c.NH4Cl饱和溶液 d.植物油
(2)若装置中分液漏斗与导气管之间没有导管A连通,对所测AlN纯度的影响是__(填“偏大”“偏小”或“不变”)
方案ii:乙同学按以下步骤测定样品中AlN的纯度。
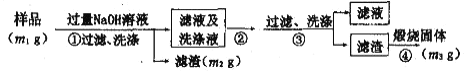
(3)步骤②通入过量__气体。
(4)步骤③过滤所需要的主要玻璃仪器有__。
(5)样品中AlN的纯度是___(用含m1、m2、m3的表达式表示)。
-
选考[有机化学基础](15分)双酚A型环氧树脂是由双酚A、环氧氯丙烷在碱性条件下缩合而成的高分子化合物。具有良好的物理化学性能,被广泛应用于涂料、胶粘剂等领域。根据该树脂的合成路线图示,回答以下问题:
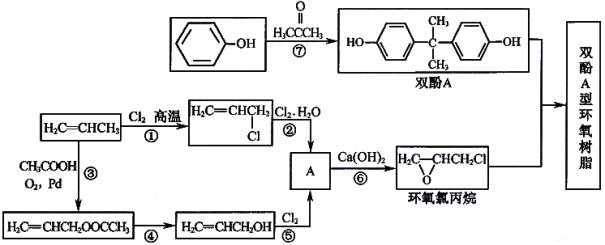
(1)写出上图中②⑥两步的反应方程式:②_________________⑥_________________
(2)乙酸丙烯酯(H2C=CHCH2OOCCH3)有多种同分异构体,其中能发生银镜反应,且核磁共振氢谱上只有两种峰,强度比为3:1的同分异构体的结构简式为__________________;其中既可以和NaHCO3溶液又能与溴水反应的物质有_____种(不考虑立体异构)。
(3)双酚A的另一重要用途是和光气( )合成Lexan聚碳酸酯(一种高强材料,可用于制作防弹窗户)。写出此合成反应的化学方程式:_________________________。
)合成Lexan聚碳酸酯(一种高强材料,可用于制作防弹窗户)。写出此合成反应的化学方程式:_________________________。























