-
实验室制备肉桂酸的化学方程式为:

副反应: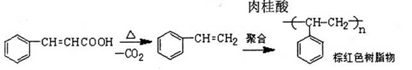
药品物理常数
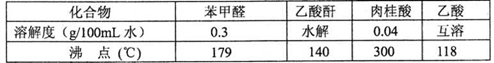
主要实验装置和步骤如下:
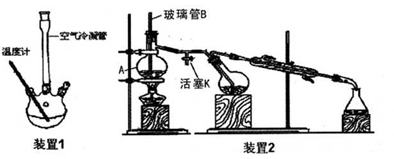
(I) 合成:
向装置1的三颈烧瓶中先后加入3g新熔融并研细的无水醋酸钠、3mL新蒸馏过的苯甲醛和 5.5mL乙酸酐,振荡使之混合均匀。在150~170℃加热回流40min,反应过程中体系的颜色会逐 渐加深,并伴有棕红色树脂物出现。
(II)分离与提纯:
①向反应液中加30mL沸水,加固体碳酸钠至反应混合物呈弱碱性。
②按装置2进行水蒸气蒸馏,在冷凝管中出现有机物和水的混合物,直到馏出液无油珠。
③剩余反应液体中加入少许活性炭,加热煮沸,趁热过滤,得无色透明液体。
④滤液用浓盐酸酸化、冷水浴冷却、结晶、抽滤、洗涤、重结晶,得肉桂酸无色晶体。 回答下列问题:
(1)合成过程中要求无水操作,理由是______。将含结晶水的醋酸钠加热制无水醋酸钠,观察到盐由固体→液体→固体→液体。第一次变成液体的原因是_____。
(2)合成过程的加热回流,要控制皮应呈微沸状态,如果剧烈沸腾,可能导致()
A. 使肉桂酸蒸出影响产率
B. 使乙酸酐蒸出影响产率
C. 肉桂酸脱羧成苯乙烯,进而生成苯乙烯低聚物,甚至生成树脂状物
D. 反应变缓慢
(3)仪器A的名称_____:玻璃管B的作用_____。
(4)分离和提纯操作中,步骤①加Na2CO3目的是_____。
(5)水蒸气蒸馏就是将水蒸气通入不溶或难溶于水但有一定挥发性的有机物中,使该有机物在 ,低于1000C的温度下,与水共沸而随着水蒸气一起蒸馏出来。步骤②的目的____,蒸馏结束后先____,再____,以防倒吸。
(6)步骤③加活性炭目的是____:若趁热过滤在抽滤装置中进行,下列操作错误的是()
A.布氏漏斗和滤纸要事先用沸水预热
B.各步操作的动作一定要快
C.为防止滤纸破损,混和液必须用玻璃棒引流至布氏漏斗
D.吸滤瓶内的溶液可直接从支管口倒出
-
(14分)实验室以苯、乙醛为原料,三氯化铝为催化剂来制备1,1—二苯乙烷,其反应原理为:
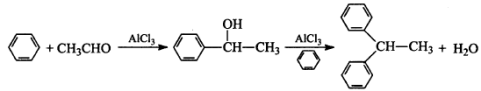
制备过程中其他产物会与AlCl3发生副反应。主要实验装置和步骤如下:
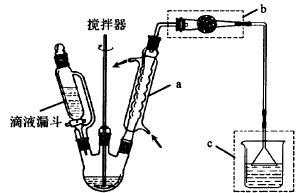
I.合成:
在250 mL三口烧瓶中加入140mL苯(密度0.88g/mL)、19gA1C13和5.5g乙醛,在20℃时充分反应。
Ⅱ.分离与提纯:
将反应混合物倒入装有150 mL,冰水和少量盐酸的烧杯中,充分搅拌,用分液漏斗分离出有机层,依次用水、2%碳酸钠溶液、水洗涤,在分离出的粗产品中加入少量无水硫酸镁固体,过滤后先常压蒸馏除去过量苯再改用减压蒸馏收集170~172℃/6.67kPa的馏分,得12.5g 1,l—二苯乙烷。
(1)仪器a的名称: ;其他产物与A1C13发生副反应的化学方程式为: ;装置C的作用: 。
(2)连接装置b的作用是 。
(3)在洗涤操作中,第二次水洗的主要目的是 。实验中加入少量无水硫酸镁的目的是 。
(4)粗产品常压蒸馏提纯时,下列装置中温度计位置正确的是 ,可能会导致收集到的产品中混有低沸点杂质的装置是 。
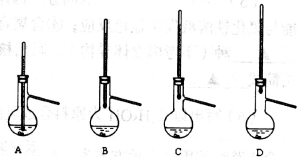
(5)本实验所得到的1,1—二苯乙烷产率约为 (填正确答案的序号)。
A.41% B.48% C.55% D.65%
-
高纯 是制备高性能磁性材料的主要原料。实验室以
是制备高性能磁性材料的主要原料。实验室以 为原料制备少量高纯
为原料制备少量高纯 的操作步骤如下:
的操作步骤如下:
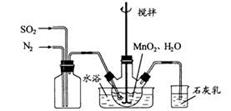 (1)制备
(1)制备 溶液:在烧瓶中(装置见右图)加入
溶液:在烧瓶中(装置见右图)加入
一定量 和水,搅拌,通入
和水,搅拌,通入 和
和 混合
混合
气体,反应3h。停止通入 ,继续反应片刻,
,继续反应片刻,
过滤(已知 )
)
①石灰乳参与反应的化学方程式为_____________。
②反应过程中,为使 尽可能转化完全,在通入
尽可能转化完全,在通入 和
和 比例一定、不改变固液投料的条件下,可采取的合理措施有__________________________、_________________。
比例一定、不改变固液投料的条件下,可采取的合理措施有__________________________、_________________。
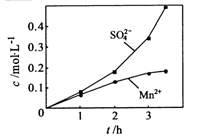 ③若实验中将
③若实验中将 换成空气,测得反应液中
换成空气,测得反应液中
 、
、 的浓度随反应时间t的浓度变化如右图。
的浓度随反应时间t的浓度变化如右图。
导致溶液中 、
、 浓度变化产生明显差异的
浓度变化产生明显差异的
原因是_____________。
(2)制备高纯 固体:已知
固体:已知 难溶于水、乙醇,潮湿时易被空气氧化,
难溶于水、乙醇,潮湿时易被空气氧化, 开始分解;
开始分解; 开始沉淀时
开始沉淀时 。请补充由(1)时制得的
。请补充由(1)时制得的 制备高纯
制备高纯 的操作步骤【实验中可选用的试剂:
的操作步骤【实验中可选用的试剂:  、
、 、
、  、
、 】。
】。
①________;②________;③________;④________;⑤低于 。
。
-
实验室以苯、乙醛为原料,三氯化铝为催化剂来制备1,1—二苯乙烷,其反应原理为: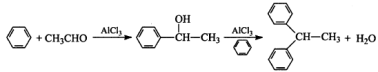
制备过程中的无机产物会与AlCl3发生反应。主要实验装置和步骤如下:
I.合成:
在250 mL三口烧瓶中加入140mL苯(密度0.88g/mL)、19gAlCl3和5.5g乙醛,在20℃时充分反应。
Ⅱ.分离与提纯:
将反应混合物倒入装有150 mL冰水和少量盐酸的烧杯中,充分搅拌,用分液漏斗分离出有机层,依次用水、2%碳酸钠溶液、水洗涤,在分离出的粗产品中加入少量无水硫酸镁固体,过滤后先常压蒸馏除去过量苯再改用减压蒸馏收集170~172℃/6.67kPa的馏分,得12.5g 1,1—二苯乙烷。
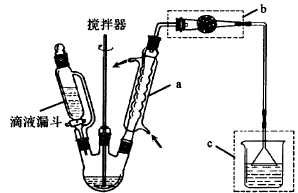
(1)仪器a的名称: ;无机产物与AlCl3发生反应的化学方程式为: ;装置c的作用: 。
(2)连接装置b的作用是 。
(3)在洗涤操作中,第二次水洗的主要目的是 ,实验中加入少量无水硫酸镁的目的是 。
(4)粗产品常压蒸馏提纯时,下列装置中温度计位置正确的是 ,可能会导致收集到的产品中混有低沸点杂质的装置是 。
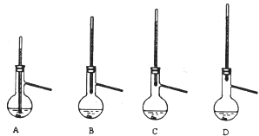
(5)本实验所得到的1,1—二苯乙烷产率约为 (填正确答案的序号)。
A.41% B.48% C.55% D.65%
-
 (12分)高纯
(12分)高纯 是制备高性能磁性材料的主要原料。实验室以
是制备高性能磁性材料的主要原料。实验室以 为原料制备少量高纯
为原料制备少量高纯 的操作步骤如下:
的操作步骤如下:
(1)制备 溶液:
溶液:
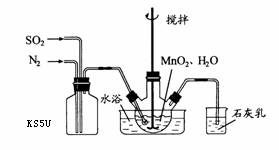
 在烧瓶中(装置见右图)加入一定量
在烧瓶中(装置见右图)加入一定量 和水,搅拌,
和水,搅拌,
通入 和
和 混合气体,反应3h。停止通入
混合气体,反应3h。停止通入 ,
,
继续反应片刻,过滤(已知 )。
)。
①石灰乳参与反应的化学方程式为________。
②反应过程中,为使 尽可能转化完全,在通入
尽可能转化完全,在通入 和
和 比例一定、不改变固液投料的条件下,可采取的合理措施有________、________。
比例一定、不改变固液投料的条件下,可采取的合理措施有________、________。
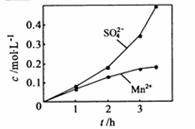
③若实验中将 换成空气,测得反应液中
换成空气,测得反应液中 、
、 的浓度随反应时间t变化如右图。导致溶液中
的浓度随反应时间t变化如右图。导致溶液中 、
、 浓度变化产生明显差异的原因是________。
浓度变化产生明显差异的原因是________。
(2)制备高纯 固体:已知
固体:已知 难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;
难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解; 开始沉淀时
开始沉淀时 。请补充由(1)制得的
。请补充由(1)制得的 溶液制备高纯
溶液制备高纯 的操作步骤[实验中可选用的试剂:
的操作步骤[实验中可选用的试剂:  、
、 、
、  、
、 ]。
]。
①________;②________;③________;④________;⑤低于100℃干燥。
-
肉桂酸为微有桂皮香气的无色针状晶体,能抑制黑色酪氨酸酶的形成,是高级防晒霜中不可少的成分之一。实验室制取肉桂酸的原理如下:

实验步骤:
步骤1 在图1所示装置(夹持与加热仪器未画出,下同)的三颈烧瓶内加入K2CO3、苯甲醛(油状物)和乙酸酐,混合均匀后,在170 ℃~180 ℃加热反应1 h,冷却。
 图1
图1 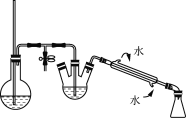 图2
图2 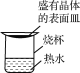 图3
图3
步骤2 向三颈烧瓶内分批加入20 mL水和Na2CO3固体,调节溶液pH约为8。
步骤3 在三颈烧瓶中加入活性炭,用图2所示水蒸气蒸馏装置蒸馏除去未反应的苯甲醛。
步骤4 将三颈烧瓶内反应混合物趁热过滤,滤液冷却至室温,用浓盐酸酸化至pH=3,析出大量晶体,抽滤。并用少量冷水洗涤晶体。
步骤5 将晶体在图3所示热水浴上加热干燥。
(1)图1中仪器A的作用是____________。
(2)步骤2中Na2CO3需分批加入的原因是_________________________________________________。
(3)水蒸气蒸馏时,判断蒸馏结束的方法是________。
(4)步骤4中,“趁热过滤”的目的是_____________。
(5)抽滤时所需主要仪器有____、安全瓶及抽气泵等。
(6)与使用烘箱烘干相比,热水浴干燥的优点是___________________________________。
-
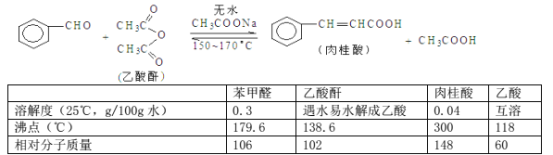
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料。实验室可用苯甲醛和乙酸酐、醋酸钠等原料经下列反应制取肉桂酸,其中苯甲醛为无色油状液体。已知:
填空:
Ⅰ.合成:反应装置如图所示。向三颈烧瓶中先后加入研细的无水醋酸钠、4.8g苯甲醛和5.6g乙酸酐,振荡使之混合均匀。在150~170℃加热1小时,保持微沸状态。
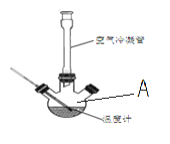
(1)仪器A的名称为___。
(2)空气冷凝管的作用是__,该装置加热要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是__。
(3)不能把无水CH3COONa换成CH3COONa·3H2O的原因是__。
Ⅱ.粗品精制:已知水蒸气蒸馏是分离提纯有机化合物的重要方法之一,可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯的目的。
将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
a.在搅拌下,向反应液中加入20mL水
b.再慢慢加入碳酸钠溶液
c.然后进行水蒸气蒸馏
d.待烧瓶内溶液冷却至室温,在搅拌下用加入盐酸酸化,析出大量晶体,过滤,洗涤,干燥。
(4)饱和Na2CO3溶液的作用有__。水蒸气蒸馏可除去的杂质是__;如何判断蒸馏终点___。
(5)若得到的肉桂酸晶体产品不纯,应采用__可得到纯度更高的产品。
(6)若最后得到纯净的肉桂酸5.0g,则该反应中的产率是__(保留两位有效数字)。
-
芳香羧酸通常用芳香烃的氧化来制备,某同学用甲苯的氧化反应制备苯甲酸。已知: +2KMnO4
+2KMnO4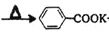 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
反应试剂、产物的物理常数:

主要实验装置和流程如下:
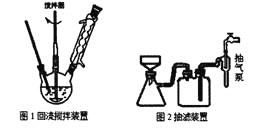
实验方法:向图1装置中依次加入2.8mL甲苯、200mL水和8.6g高锰酸钾,通冷凝水,加热至沸腾,在反应过程中,甲苯不断的被冷凝回流,反应结束后,按以下步骤操作,得到苯甲酸粗产品。

(1)图1装置中反应结束的标志是__,趁热抽滤的目的是__。
(2)写出浓盐酸酸化时的所有离子反应方程式__。
(3)下列说法正确的是__。
A.图1装置中的反应混合物抽滤时应用玻璃砂漏斗替代布氏漏斗
B.在冷却抽滤时,若有产品黏在瓶壁上,可用滤液淋洗,直到所有晶体收集到布氏漏斗中,再次抽滤
C.苯甲酸粗产品的杂质除KCl外还可能含有甲苯,均可用蒸馏水洗涤除去
D.抽滤结束,为防止倒吸,应先关闭水龙头,再拆掉抽气泵和吸滤瓶之间的橡皮管
(4)苯甲酸纯度测定:用__(填仪器名称)称取1.220g产品,加合适溶剂溶解,再用蒸馏水稀释配成100mL溶液,取25.00mL溶液,滴加几滴指示剂,用0.1000mol•L-1NaOH标准液进行滴定,平行滴定3次,平均消耗标准液体积为21.00mL
①“合适溶剂”和“指示剂”分别为__。
A.蒸馏水和酚酞 B.乙醇和甲基橙 C.四氯化碳和酚酞 D.乙醇和酚酞
②苯甲酸产品的纯度为__。
-
硫代硫酸钠是一种重要的化工产品。某兴趣小组制备硫代硫酸钠晶体 的实验装置如下图所示(省略夹持装置):
的实验装置如下图所示(省略夹持装置):
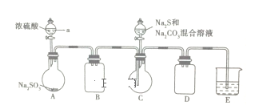
主要实验步骤为:①检查装置气密性,按图示加入试剂;②先向C中烧瓶加入 和
和 混合溶液,再向A中烧瓶滴加浓硫酸;③待
混合溶液,再向A中烧瓶滴加浓硫酸;③待 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经一系列实验操作后得到产品。
完全消耗后,结束反应。过滤C中混合物,滤液经一系列实验操作后得到产品。
已知:i 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成;ii向
溶液混合无沉淀生成;ii向 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 所得产品常含有少量
所得产品常含有少量 和
和 。
。
回答下列问题:
(1)仪器a的名称是____________;B、D装置的作用是_____________。
(2)上述实验步骤③中的操作主要有_______________、冷却结晶、过滤、洗涤、干燥;E中的试剂是_____________。
(3)为检验产品中是否含有 和
和 ,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:
,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:
取适量产品配成稀溶液,滴加足量 溶液,有白色深沉生成,向沉淀中滴加足量的_________,若____________(填实验现象),则可以确定产品中含有
溶液,有白色深沉生成,向沉淀中滴加足量的_________,若____________(填实验现象),则可以确定产品中含有 和
和 。
。
(4)为减少装置C中生成 的量,在不改变原有装置的基础上对实验步骤②需进行改进,具体操作是_________________;写出制备
的量,在不改变原有装置的基础上对实验步骤②需进行改进,具体操作是_________________;写出制备 的总反应的化学方程式:___________________________。
的总反应的化学方程式:___________________________。
-
2-苯基-2-丁醇是重要的有机合成中间体,以溴苯为原料合成该中间体的反应原理如下:
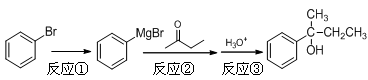
【实验装置】


装置Ⅰ 装置Ⅱ
【实验步骤】
步骤1:将镁条置于装置Ⅰ的三颈烧瓶中,加入100 mL乙醚(ρ=0.71g·cm-3),在冷却条件下缓缓滴入溴苯,微热并加入一小块碘引发反应①。
步骤2:滴加14.2 mL丁酮和30 mL乙醚混合物,发生反应②;滴加入20%的NH4Cl水溶液,发生反应③。
步骤3:分出油层,用水洗涤至中性,用无水CaCl2干燥。
步骤4:用装置Ⅱ先蒸出乙醚,再蒸馏出产品。
⑴步骤1中加入碘的作用是 。
⑵装置Ⅰ中滴加液体所用的仪器的名称是 ,反应②需将三颈烧瓶置于冰水中,且逐滴加入丁酮和乙醚,其目的是 。
⑶步骤三中分离出油层的具体实验操作是 。
⑷装置Ⅱ采用的是减压蒸馏,实验时需将吸滤瓶需连接 ;采用这种蒸馏方式的原因是 。







 (1)制备
(1)制备 ③若实验中将
③若实验中将


 (12分)高纯
(12分)高纯 在烧瓶中(装置见右图)加入一定量
在烧瓶中(装置见右图)加入一定量
 图1
图1  图2
图2  图3
图3

 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O





