-
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
己知:Ksp[Fe(OH)3]= 4.0×10-38
回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为______________________________:
(2)过程I 加入铁屑的主要作用是___________,分离得到固体的主要成分是______,从固体中分离出铜需采用的方法是___________________;
(3)过程II中发生反应的化学方程式为_________________________;
(4)过程II中调节溶液的pH为5,金属离子浓度为__________________。(列式计算)
高二化学工业流程中等难度题查看答案及解析
-
电子工业上使用
溶液蚀刻铜箔制造印刷电路板。在该制备工艺中,为了实现资源再生,减少污染,某兴趣小组提出废液处理和资源回收的过程如下:
Ⅰ.向废液中投入过量铁屑,充分反应后分离出固体和滤液;
Ⅱ.向滤液中加入一定量石灰水,调节溶液
,同时鼓入足量的空气。
已知:Ksp[Fe(OH)3]=4×10-38,回答下列问题:
(1)
蚀刻铜箔反应的离子方程式为______;过程Ⅰ加入铁屑的主要作用是______
(2)过程Ⅱ中鼓入足量的空气发生反应的化学方程式为______
(3)过程Ⅱ中调节溶液的
为5,金属离子浓度为______。(列式计算)
(4)另一兴趣小组将制造印刷电路板
蚀刻铜箔的反应设计成一个原电池。请将方框中实验装置图补充完整,并作相应标注(标出电极材料、电解质溶液)。限选材料:
,
,
,
:铜片,铁片,锌片,石墨和导线。
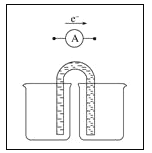
(5)废旧印刷电路板经粉碎分离能得到非金属粉末和金属粉末,也可回收利用实现资源再生,减少污染。印刷电路板的金属粉末用
和
的混合溶液处理,溶出印刷电路板金属粉末中的铜。控制其他条件相同时,测得不同温下铜的平均溶解速率(见下表)。
温度
20
30
40
50
60
70
80
铜平均溶解速率
①当温度高于
时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是______。
②在提纯后的
溶液中加入一定量的
和
溶液,加热,生成
沉淀。制备
的离子方程式是______。
高二化学综合题中等难度题查看答案及解析
-
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(含有Fe2+、Fe3+、Cu
2+)处理和资源回收很有意义,下列是回收金属铜和刻蚀液再生的流程图,回答下列问题:
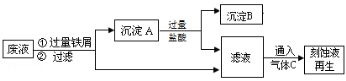
(1)沉淀A中含有的单质是 。
(2)通入的气体C的化学式是 。
(3)滤液与气体C反应生成刻蚀液的离子方程式: 。
高二化学填空题中等难度题查看答案及解析
-
电子工业中,可用FeCl3—HCl溶液作为印刷电路铜板蚀刻液。
某探究小组设计如下线路处理废液和资源回收:
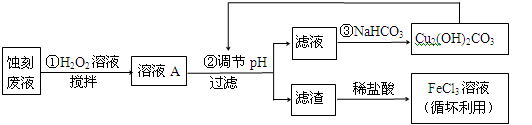
请回答:
(1)FeCl3—HCl溶液蚀刻铜板后的废液中含有的金属阳离是 。
(2)FeCl3蚀刻液中加入盐酸的目的:可以 。
(3)步骤①中加入H2O2溶液的目的是 。
(4)已知:生成氢氧化物沉淀的pH
Cu(OH)2
Fe(OH)2
Fe(OH)3
开始沉淀时
4.7
7.0
1.9
沉淀完全时
6.7
9.0
3.2
根据表中数据推测调节pH的范围是 。
(5)写出步骤②中生成CO2的一个离子方程式 (已知Cu2(OH)2CO3不易溶于水)
(6)写出步骤③生成Cu2(OH)2CO3的离子方程式 。
高二化学填空题困难题查看答案及解析
-
(14分)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的印刷电路板铜箔.某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列流程:
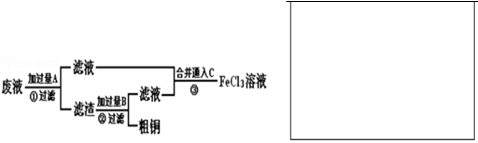
(1)写出流程①中回收金属铜时发生反应的离子方程式 .
请根据上述反应设计一个原电池,在方框中画出简易装置图(标出相应电极名称、电极材料、电解质溶液).
(2)写出图流程③相关反应的化学方程式: .
(3)如下图为相互串联的甲、乙两个电解池(电极都是惰性电)
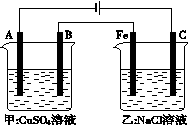
请回答:
①写出两电解池中的电解反应方程式:
甲________________ _
乙
②若甲槽阴极增重12.8 g,则乙槽阳极放出气体在标准状况下的体积为______ __。
③若乙槽剩余液体为400 mL,则电解后得到碱液的物质的量浓度为____ __。
高二化学填空题困难题查看答案及解析
-
FeCl3溶液可以蚀刻印刷电路板上的Cu。某实验兴趣小组模拟该过程,并回收Cu和蚀刻液的流程如下:
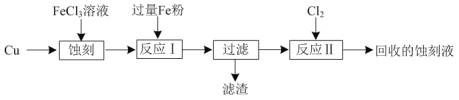
(1)“蚀刻”时的化学反应方程式为____。
(2) 滤渣的成分为____。
(3)“反应Ⅱ”的离子方程式为____。
高二化学工业流程简单题查看答案及解析
-
Fe2(SO4)3溶液可用于腐蚀绝缘板上的铜箔,制造印刷电路板。现设计了一个方案如下,从腐蚀后的废液(主要含Fe3+、Fe2+、Cu2+)中回收铜,并重新获得Fe2(SO4)3溶液。
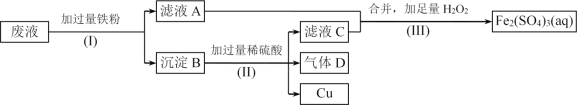
(1)步骤(I)中分离操作名称为____________________。
(2)沉淀B的主要成分有____________________,气体D的电子式为__________。
(3)写出步骤(III)中发生反应的离子方程式______________________________。
高二化学工业流程中等难度题查看答案及解析
-
(11分)电子工业常用30﹪的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与铜箔发生反应的化学方程式:________;若反应过程中有2 mol电子发生转移,会有________ g Cu溶解。
(2)某工程师为了从使用过的腐蚀废液(不含FeCl3)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
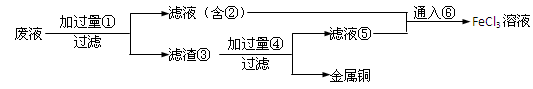
请写出上述试验过程中②⑤的化学式:
②________,⑤________。
请写出①⑥两步反应的离子方程式:________ ;
。
高二化学填空题中等难度题查看答案及解析
-
(11分)电子工业常用30﹪的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)写出FeCl3溶液与铜箔发生反应的化学方程式:________;若反应过程中有2 mol电子发生转移,会有________ g Cu溶解。
(2)某工程师为了从使用过的腐蚀废液(不含FeCl3)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
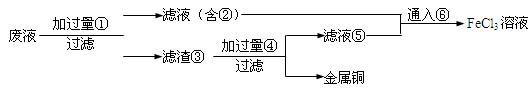 请写出上述试验过程中②⑤的化学式:
请写出上述试验过程中②⑤的化学式:②________,⑤________。
请写出①⑥两步反应的离子方程式:________ ;
________。
高二化学填空题中等难度题查看答案及解析
-
(18分)铁、铜等金属及其化合物在日常生活中应用广泛,回答下列问题。
(1)电子工业常用30%的FeCl3溶液腐蚀附在绝缘板上的铜箔制造印刷电路板,取其腐蚀后的废液,加 入一定量的铁粉后,若无固体剩余,则反应后的溶液中肯定有的离子是______________;若有红色固体,则反应后的溶液中肯定没有的离子是________,检验该离子的试剂为________。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃-60℃,加入H2O2,反应一段时间后可制得硫酸铜,发生反应的化学方程式为:_____________________,
(3)实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾(FeSO4.7H2O),测定产品中绿矾含量的实验步骤:
a.称取5.7 g产品,溶解,配成250 mL溶液;
b.量取25 mL待测液于锥形瓶中;
c.用硫酸酸化的0.01 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液的体积为40 mL。
根据上述步骤回答下列问题:
①滴定时发生反应的离子方程式为(完成并配平离子反应方程式)
②用硫酸酸化的KMnO4溶液滴定至终点的标志是 _____。
③上述产品中FeSO4·7H2O的质量分数为 。
(4)铁氰化钾 K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6] 的混合溶液可用于太阳能电池的电解液,该太阳能电池的工作原理示意图如图所示,其中催化剂a为________极,电极反应式为_______________;

高二化学填空题困难题查看答案及解析