-
氨碱法(索氏)和联合制碱法(侯氏)是两大重要的工业制碱法,下列表达不正确的是
氨碱法 联合制碱法
A 原料 食盐、氨气、生石灰 食盐、氨气、二氧化碳
B 可能的副产物 氯化钙 氯化铵
C 循环物质 氨气、二氧化碳 氯化钠
D 评价 原料易得;设备复杂;能耗高 原料利用率高;废弃物少
高三化学选择题中等难度题查看答案及解析
-
比较纯碱的两种工业制法,正确的是
选项
项目
氨碱法
联合制碱法
A.
原料
食盐、氨气、生石灰
食盐、氨气、二氧化碳
B.
可能的副产物
氯化钙
氯化铵
C.
循环物质
氨气、二氧化碳
氨气、氯化钠
D.
评价
原料易得、产率高
设备简单、能耗低
A.A B.B C.C D.D
高三化学单选题中等难度题查看答案及解析
-
对氨碱法(索氏)和联合制碱法(侯氏)对比分析,错误的是
A.产品完全相同 B.生产NaHCO3的反应原理相同
C.食盐利用率不同 D.都循环利用了CO2
高三化学单选题简单题查看答案及解析
-
(10分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4C1等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料制得NaHCO3,进而生产出纯碱。以下A、B、C、D四个装置可组装成实验室模拟 “侯氏制碱法”制取NaHCO3的实验装置。装置中分别盛有以下试剂:B:稀硫酸;C:盐酸、碳酸钙;D:含氨的饱和食盐水、水

四种盐在不同温度下的溶解度(g/100g水)表
0℃
10℃
20℃
30℃
40℃
50℃
60℃
100℃
NaCl
35.7
35.8
36.0
36_3
36.6
37.0
37.3
39.8
NH4HCO3
11.9
15.8
21.0
27.0
—①
—
—
—
NaHCO3
6.9
8.1
9.6
11.1
12.7
14.5
16.4
NH4Cl
29.4
33.3
37.2
41.4
45.8
50.4
55.3
77.3
(说明:①>35℃NH4HCO3会有分解)
请回答以下问题:
(1)装置的连接顺序应是________(填字母)。
(2)A装置中盛放的试剂是________,其作用是________。
(3)在实验过程中,需要控制D温度在30℃~35℃,原因是________。
(4)反应结束后,将锥形瓶浸在冷水中,析出NaHCO3晶体。用蒸馏水洗涤NaHCO3晶体的目的是除去________杂质(以化学式表示)
(5)将锥形瓶中的产物过滤后,所得的母液中含有________(以化学式表示),加入氯化氢,并进行________操作,使NaCl溶液循环使用,同时可回收NH4C1。
高三化学实验题中等难度题查看答案及解析
-
我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、氨气和二氧化碳为原料制得NaHCO3,进而生产出纯碱。
Ⅰ.某研究性学习小组的同学,模拟“侯氏制碱法”提出下列一种制备NaHCO3 的实验方案,经过讨论,大家一致认为方案2较合理,请说明方案3的不足之处是__________。
方案1:分别将二氧化碳和氨气通入NaCl饱和溶液中;
方案2:将二氧化碳通入含氨的NaCl饱和溶液中;
方案3:将氨气通入含二氧化碳的NaCl饱和溶液中。
Ⅱ.根据方案2,某同学设计了如下实验步骤和装置图:
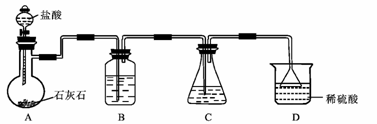
步骤1:配制含氨的饱和食盐水。在100mL的锥形瓶中加人20mL氨水(体积比 1︰ 1),再加入 8g 食盐, 塞紧橡皮塞, 振荡几分钟, 过滤除去不溶物, 得到含氨的饱和食盐水。
步骤2: 制备碳酸氢钠。 按图组装实验装置,先检查装置的气密性,再向各仪器中加入相应的试剂,开始制备碳酸氢钠。 实验过程中,需要控制温度在30℃~35℃(大于35℃时NH4HCO3会分解) 和二氧化碳的通入速度(以出现能数得清的连续气泡为好)。反应结束后,把锥形瓶浸入冷水中,使较多的晶体析出,过滤、洗涤。
请回答下列问题:
(1)D烧杯中稀硫酸的作用是_________。
(2)装置B中试剂是_______, 它的作用为________。
(3)装置C中的化学方程式为______。
(4)检验步骤2中所得晶体是碳酸氢钠而不是氯化钠的的实验方法和现象是_____。 (5)为了检验某含有NaHCO3,杂质的Na2CO3样品的纯度,现将m1 g 样品加热,其质量变为m2 g,则样品的纯度是_________.
高三化学实验题中等难度题查看答案及解析
-
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料先制得NaHCO3,进而生产出纯碱。下面是在实验室中模拟“侯氏制碱法”制取NaHCO3的实验步骤:
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4Cl晶体析出。
请回答下列问题:
(1)装置的连接顺序是:(a)接(____)(____)接(____)(b)接(_____)

(2)A中常选用的固体反应物为___________;D中应选用的液体为__________;B中发生反应的化学方程式为____________________________________。
(3)第二步骤中必须先让________装置先发生反应。
(4)C中用球形干燥管而不用直导管,其作用是__________________________,C中广口瓶内产生固体的总化学方程式为____________________________。
(5)第四步中分离出NH4Cl晶体的操作是_____________;其所得的NH4Cl晶体中常含有少量的NaCl和NaHCO3约占5%—8%),请设计一个简单的实验证明所得固体的成分大部分是NH4Cl。简要写出操作和现象_______________________。
高三化学实验题中等难度题查看答案及解析
-
(14分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料先制得NaHCO3,进而生产出纯碱。下面是在实验室中模拟“侯氏制碱法”制取NaHCO3的实验步骤:
第一步:连接好装置,检验气密性,在仪器内装入药品。
第二步:先让一装置发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体,片刻后,C中出现固体。继续向C中通入两种气体,直到不再有固体产生。
第三步:过滤C中所得的混合物,得到NaHCO3固体。
第四步:向滤液中加入适量的NaCl粉末,有NH4Cl晶体析出。……
请回答下列问题:
(1)装置的连接顺序是:(a)接( ) ( )接( );(b)接( )
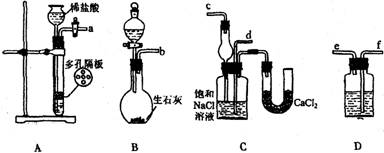
(2)A中常选用的固体反应物为____________;D中应选用的液体为___________ (填化学式)
(3)第二步骤中必须先让________装置先发生反应。
(4)C中用球形干燥管而不用直导管,其作用是____________________________,C中广口瓶内产生固体的总化学方程式为________。
(5)在第四步中分离NH4Cl晶体的操作是________________(填操作名称);其所得的NH4Cl晶体中常含有少量的NaCl和NaHCO3约占5%—8%),请设计一个简单的实验证明所得固体的成分中含有Na+。简要写出操作和现象________。
高三化学实验题中等难度题查看答案及解析
-
化学与科学、技术、社会、环境密切相关,下列说法正确的是:
A.研制乙醇汽油技术,能够降低机动车尾气中有害气体的排放
B.联合制碱法生产纯碱时,在饱和食盐水中先通入二氧化碳,再通入氨气
C.接触法制备硫酸的过程中,在吸收塔内是用大量的水吸收三氧化硫
D.工业上通过电解熔融氧化铝制备金属铝时,常常加入冰晶石作助熔剂
高三化学选择题简单题查看答案及解析
-
[化学——选修2化学与技术](15分)
(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”(侯氏制碱法)两种工艺。
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式:_________________________________________________;
②写出“联合制碱法”有关反应的化学方程式_________________ __;
。
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?________________________________________;
(2)钢铁工业对促进经济和社会发展起了重要作用。
① 炼钢时,加入硅、锰和铝的目的是_______________________________。
② 不锈钢含有的Cr元素是在炼钢过程的氧吹__ __(填“前”或“后”)加入。
③ 炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_________。
高三化学填空题简单题查看答案及解析
-
[化学一选修2:化学与技术]化学是人类进步的关键,化学为人类的生产、生活提供了物质保证。
(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。
①“氨碱法”产生大量CaCI2副产品,该工艺中生成CaCI2的化学反应方程式为___ _______________ ______
②“联合制碱法”中相关的化学反应方程式为
③C02是制碱工业的重要原料,请阐述“联合制碱法”与“氨碱法”中C02的来源有何不同 。
(2)铀(U)是核反应最重要的燃料,在核反应中有重要的应用。目前已经研制成功一种螫合型离子交换树脂,它专门吸附海水中的U4+,而不吸附其他元素,其反应原理为___ _(用离子方程式表示,树脂用HR代替,下同),发生离子交换后的离子交换膜用酸处理还可再生,并得到含铀的溶液,其反应原理为 。
(3)钢铁工业对促进经济和社会发展起了重要作用。
①不锈钢中含有的铬元素是在炼钢过程的氧吹 (填“前”或“后”)加入。
②炼钢时,加入硅、锰和铝的目的是____ 。
③炼铁和炼钢生产中,尾气均含有的主要污染物是____ ;从环保和经济角度考虑,上述尾气经处理可用作___ 。
高三化学填空题中等难度题查看答案及解析