-
碳及其化合物有广泛应用。
(1)工业冶炼铝,以石墨为阳极。阳极反应式为,可能发生副反应有。
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为。如果理论输出电压为1.50V,能量密度E= 。
(3)向75mL4mol•L-1KOH溶液中缓慢通入4480mLCO2气体(标准状况)恰好完全被吸收。①写出该反应的离子方程式:。
②该吸收溶液中离子浓度大小排序为。
③常温下,amol•L-1KHCO3溶液的pH=8,HCO3的水解常数约等于。(用含a式表示)。
(4)已知:①2H2(g)+O2(g)=2H2O(l)△H1=—571.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H2=—566.0kJ•mol-1
③CO(g)+2H2(g) CH3OH(g)△H3=—90.8kJ•mol-1
CH3OH(g)△H3=—90.8kJ•mol-1
计算甲醇蒸气的燃烧热△H= 。
(5)某温度下,发生可逆反应:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
①向某容器中充入1.0molH2和1.0molCO2(g),在一定条件下发生上述反应。混合气体中CO2的物质的量与时间关系如下列所示:
| 0 | 5min | 10min | 15min | 20min | 25min |
| I(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
| II(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
相对实验I,实验II可能改变的条件可能是,该温度下,平衡常数=。
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应。
下列图像正确且说明可逆反应达到平衡状态的是。(填序号)

-
碳及其化合物有广泛应用。
(1)工业冶炼铝,以石墨为阳极。阳极反应式为 ,可能发生副反应有 。
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为 。
(3)向75 mL 4 mol•L-1KOH溶液中缓慢通入4480 mL CO2气体(标准状况)恰好完全被吸收。①写出该反应的离子方程式: 。(只用一个离子方程式表示)
②该吸收溶液中离子浓度大小排序为 。
(4)已知:① 2H2(g)+O2(g)=2H2O(l) △H1=—571.6kJ•mol-1
② 2CO(g)+O2(g)=2CO2(g) △H2 = —566.0kJ•mol-1
③ CO(g)+2H2(g) CH3OH(g) △H3 = —90.8kJ•mol-1
CH3OH(g) △H3 = —90.8kJ•mol-1
计算甲醇蒸气的燃烧热 = 。
= 。
(5)某温度下,发生可逆反应:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g) 
①向某容器中充入1.0 molH2和1.0 molCO2(g),在一定条件下发生上述反应。混合气体中CO的物质的量与时间关系如下列所示:
| 0 | 5 min | 10 min | 15 min | 20 min | 25 min |
| I(800℃) | 1.0 | 0.80 | 0.70 | 0.65 | 0.50 | 0.50 |
| II(800℃) | 1.0 | 0.7 | 0.60 | 0.50 | 0.50 | 0.50 |
相对实验I,实验II可能改变的条件可能是 ,该温度下,平衡常数= 。
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应。
下列图像正确且说明可逆反应达到平衡状态的是 。(填序号)

-
(17分)铜、铝、硫及其它们的化合物应用广泛,如Cu可用作催化剂、制作印刷电路铜板等。
Ⅰ.铜的冶炼:工业上以辉铜矿为原料,采用火法熔炼工艺生产铜。
火法炼铜的方程式为: ,该工艺的中间过程会发生反应2Cu20+辉铜矿 6Cu+ m↑,若反应每生成5.6 L(标准状况下)m气体.则转移电子的物质的量为 。
6Cu+ m↑,若反应每生成5.6 L(标准状况下)m气体.则转移电子的物质的量为 。
Ⅱ.粗铜精炼:利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是 。
A.电解时以精铜作阳极
B.电解时阴极发生氧化反应
C.粗铜连接电源负极,其电极反应是Cu一2e—=Cu2+
D.电解后.电解槽底部会形成含少量Ag、Pt等金属的阳极泥
E.整个过程溶液中的Cu2+浓度减少
Ⅲ.铜及其化合物的性质探究:
将洁净的铜丝放在火焰上加热.并趁热插入到乙醇中,铜丝表面的现象为 ,
发生的反应为 。
Ⅳ.无水氯化铝是一种重要的化工原料。利用明矾石:K2SO4·A12(SO4)3·2A1203·6H20]制备无水氯化铝的流程如下:
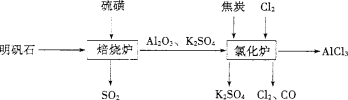
(1)验证焙烧炉产生的气体含有SO2的方法是 。
(2)吸收焙烧炉中产生的S02,下列装置合理的是 (填代号)。
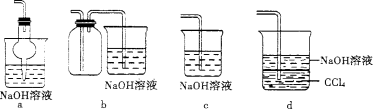
(3)氯化炉中发生反应的化学反应方程式为 。
(4)生产氯化铝的过程中会产生SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。试设计简单实验检验二者是否恰好完全反应。(简要捕述实验步骤、现象和结论) 。
仪器自选;可供选择试剂如下:①滴加酚酞的氢氧化钠溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(5)某实验小组设计了电化学方法进行二氧化硫的回收利用。利用电化学法将尾气中的SO2气体转化为 氮肥硫酸铵,模拟装置如图:
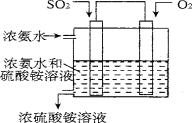
试写出SO2气体发生的电极反应式为 。
-
锑在工业上应用价值广泛,它的一种提取工艺流程如下:
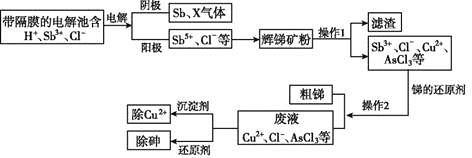
请回答下列问题:
(1)辉锑矿是含锑的重要矿物,其主要成分是 ,其中Sb的化合价是____。
,其中Sb的化合价是____。
(2)写出阳极区产物与辉锑矿粉主要成分发生反应的化学方程式:______________。
(3)电解池所用的“隔膜”宜采用____ 填“阳离子”“阴离子”或“质子”
填“阳离子”“阴离子”或“质子” 交换膜。“电解”中阴极反应的产物之一X是____
交换膜。“电解”中阴极反应的产物之一X是____ 填化学式
填化学式 。
。
(4)为除去操作1所得滤液中的 ,可加入
,可加入 。若滤液中
。若滤液中 ,当溶液中
,当溶液中 完全沉淀时,
完全沉淀时, ____
____ 。
。  已知
已知
(5)除去废液中的 ,是用次磷酸钠
,是用次磷酸钠 还原
还原 ,产生了棕色单质砷沉淀和
,产生了棕色单质砷沉淀和 。该反应中氧化剂和还原剂的物质的量之比为____。
。该反应中氧化剂和还原剂的物质的量之比为____。
(6)若电解池阴极得到 气体,同时电路中转移
气体,同时电路中转移 ,阴极生成的
,阴极生成的 ___g。
___g。
-
锑在工业上应用价值广泛,它的一种提取工艺流程如下,请回答下列问题:
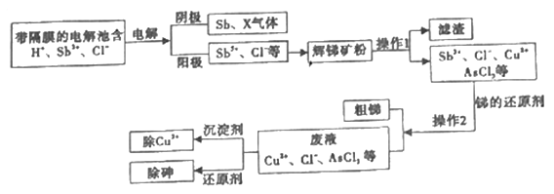
(1)辉锑矿是含锑的重要矿物,其主要成分是Sb2S3其中Sb的化合价是______。
(2)写出阳极区产物与辉锑矿粉主要成分发生反应的化学方程式______。
(3)电解池所用的“隔膜”宜采用______交换膜(填“阳离子”、“阴离子”或“质子”)。为促使Sb3+向阳极迁移加快反应,通常要进行的操作是_________。“电解” 中阴极反应的产物之一X是______。(填化学式)。
(4)为除去操作I所得滤液中的Cu2+,可加入Na2S。若滤液中c(Cu2+)= 0.01mol/L,当溶液中Cu2+恰好完全沉淀时,c(S2-)=______mol/L。 [已知Ksp(CuS)= 8×10-45]
(5)除去废液中的 AsCl3,是用次磷酸钠( NaH2PO2)还原AsCl3,产生了棕色单质砷沉淀和H3PO3。该反应中氧化剂和还原剂的物质的量之比为______,氧化产物是_____________。
(6)若电解池阴极得到1mol X气体,同时电路中转移6mole-,阴极生成的m( Sb)=____ g。
-
铝及其化合物在生活、生产中有广泛应用。
(1) 是冰晶石的主要成分,冰晶石常作工业冶炼铝的助熔剂。工业上,用氢氟酸、
是冰晶石的主要成分,冰晶石常作工业冶炼铝的助熔剂。工业上,用氢氟酸、 和
和 制备冰晶石。化学反应为
制备冰晶石。化学反应为 。稳定性:HF______
。稳定性:HF______ 填“
填“ ”或“
”或“ ”
” ,上述反应不能在玻璃容器中进行,其原因是________________
,上述反应不能在玻璃容器中进行,其原因是________________ 用化学方程式表示
用化学方程式表示 。
。
(2)明矾 常作净水剂。明矾溶液呈______
常作净水剂。明矾溶液呈______ 填“酸”“中”或“碱”
填“酸”“中”或“碱” 性,向明矾溶液中滴加氢氧化钡溶液至
性,向明矾溶液中滴加氢氧化钡溶液至 恰好完全沉淀,写出该反应的离子方程式: ______________。
恰好完全沉淀,写出该反应的离子方程式: ______________。
(3)铝合金材料耐酸、碱等腐蚀,广泛应用于生活、建筑等方面。工业上,常采用氧化法增厚铝合金材料表面的氧化膜,如常温下,用铬酸 作氧化剂可以使氧化膜产生美丽的颜色
作氧化剂可以使氧化膜产生美丽的颜色 还原产物为
还原产物为 ,配平化学方程式:______________
,配平化学方程式:______________ ______
______ ______
______ ______
______ ______
______ 。等质量的铁、铝、硅组成的同种合金分别与足量盐酸、足量烧碱溶液反应,产生氢气体积相等
。等质量的铁、铝、硅组成的同种合金分别与足量盐酸、足量烧碱溶液反应,产生氢气体积相等 同温同压
同温同压 ,则该合金中铁、硅的质量之比为______。
,则该合金中铁、硅的质量之比为______。
-
钛是一种现代工业应用广泛的优良金属,使用量可能会超过金属铁。工业上冶炼金属钛的方法有多种,下列反应原理是比较常见的冶炼钛的一种方法:
①TiO2+2Cl2 +2C TiCl4+2CO;②TiCl4+2Mg
TiCl4+2CO;②TiCl4+2Mg  Ti+2MgCl2。
Ti+2MgCl2。
请回答下列问题:
(1)与钛同周期元素中未成对电子数最多的基态原子的电子排布式为_________________。
(2)反应①中涉及的非金属元素电负性由大到小的顺序为_________(用元素符号表示);与CO互为等电子体的离子为__________(填化学式,写一种即可)。
(3)①TiCl4在常温下是无色液体,分子中4 个氯原子不在一个平面上,TiCl4空间构型为____,该物质能否溶解在苯溶剂中__________(填“能”或“否”) 。
②三氯化钛与酒石酸( )反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。
)反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。
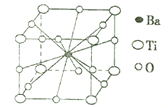
(4)钛酸钡晶体的结构示意图如图所示,若晶胞参数为a pm,则钛酸钡晶体的密度=_____g/cm3(阿伏加德罗常数用NA表示)。
-
铜及其化合物在工业、农业、科技和日常生活中有广泛应用。
(1)工业上利用辉铜矿(主要成分是Cu2S)冶炼铜。为了测定辉铜矿样品的纯度,用酸性高锰酸钾溶液反应,所得溶液加入Ba(NO3)2有白色沉淀生成。写出辉铜矿与高锰酸钾反应的离子方程式 。
(2)工业上利用废铜屑、废酸(含硝酸、硫酸)为主要原料制备硫酸铜晶体。某含有c(HNO3)=2 mol/L,c(H2SO4)=4 mol/L的废酸混合液100 mL(不使用其它酸或氧化剂),最多能制备硫酸铜晶体(CuSO4·5H2O)的质量为 。
(3)现有一块含有铜绿〔Cu2(OH)2CO3〕的铜片(假设不含其它杂质)在空气中灼烧至完全反应,经测定,反应前后固体的质量相同。
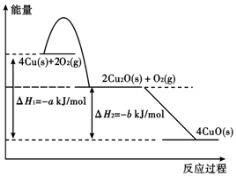
①固态铜与适量氧气反应,能量变化如下图所示,写出固态铜与氧气反应生成1 mol固态氧化亚铜的热化学方程式 。
②上述铜片中铜的生锈率为 (金属生锈率= )。(结果保留到整数)
)。(结果保留到整数)
(4)自然界中各种原生铜的硫化物经氧化、淋滤作用后转化为硫酸铜溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),慢慢地转变为铜蓝(CuS)。
①硫化铜与氧气在淋滤作用下生成硫酸铜等,该过程的化学方程式为 。②写出渗透到地下深层的硫酸铜溶液遇到闪锌矿发生反应的离子方程式 ,请用简短的语言解释该反应发生的原理
-
(14分)铜及其化合物在工业、农业、科技和日常生活中有广泛应用。
(1)工业上利用辉铜矿(主要成分是Cu2S)冶炼铜。为了测定辉铜矿样品的纯度,用酸性高锰酸钾溶液反应,所得溶液加入Ba(NO3)2有白色沉淀生成。写出辉铜矿与高锰酸钾反应的离子方程式 。
(2)工业上利用废铜屑、废酸(含硝酸、硫酸)为主要原料制备硫酸铜晶体。某含有c(HNO3)=2 mol/L,c(H2SO4)=4 mol/L的废酸混合液100 mL(不使用其它酸或氧化剂),最多能制备硫酸铜晶体(CuSO4·5H2O)的质量为 〔M(CuSO4·5H2O)=250〕.
(3)现有一块含有铜绿〔Cu2(OH)2CO3〕的铜片(假设不含其它杂质)在空气中灼烧至完全反应,经测定,反应前后固体的质量相同。
①固态铜与适量氧气反应,能量变化如下图所示,写出固态铜与氧气反应生成1 mol固态氧化亚铜的热化学方程式 。
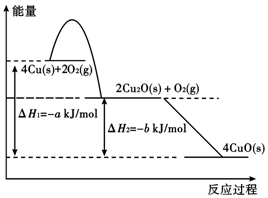
②上述铜片中铜的生锈率为 (金属生锈率= )。(结果保留到整数)
)。(结果保留到整数)
(4)自然界中各种原生铜的硫化物经氧化、淋滤作用后转化为硫酸铜溶液,并向深部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),慢慢地转变为铜蓝(CuS)。
①硫化铜与氧气在淋滤作用下生成硫酸铜等,该过程的化学方程式为 。
②写出渗透到地下深层的硫酸铜溶液遇到闪锌矿发生反应的离子方程式 ,请用简短的语言解释该反应发生的原理 。
-
金属材料有着广泛的应用。下列说法错误的是
A.由于铝具有强还原性,所以可以通过铝热反应冶炼某些高熔点金属
B.利用牺牲阳极保护法保护钢铁时,钢铁作正极
C.少量铁溶于稀硝酸,反应的离子反应为:Fe+4H++NO3-=Fe3++NO↑+2H2O
D.纳米Fe、纳米Cu的化学活性都比原来增强,两者都能与盐酸反应生成氢气
CH3OH(g)△H3=—90.8kJ•mol-1
CO2(g)+H2(g)






 Ti+2MgCl2。
Ti+2MgCl2。 )反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。
)反应,制得新的固态配合物酒石酸羟基钛(III)[Ti(OH)(C4H4O6)·1.5H2O),在酒石酸中,羧基氧原子的轨道杂化类型分别是_______,σ键和π键的数目比为__________,Ti3+能形成配合物的原因为____________。1个酒石酸分子中手性碳原子数有_____________个。

 )。(结果保留到整数)
)。(结果保留到整数)
 )。(结果保留到整数)
)。(结果保留到整数)