一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是
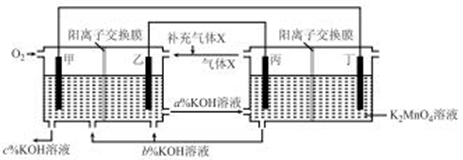
A. 电极丁的反应式为MnO42- -e-= MnO4-
B. 电极乙附近溶液的pH减小
C. KOH溶液的质量分数:c%>a%>b%
D. 导线中流过2 mol电子时,理论上有2molK+移入阴极区
高三化学选择题困难题
一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是

A. 电极丁的反应式为MnO42- -e-= MnO4-
B. 电极乙附近溶液的pH减小
C. KOH溶液的质量分数:c%>a%>b%
D. 导线中流过2 mol电子时,理论上有2molK+移入阴极区
高三化学选择题困难题
一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是
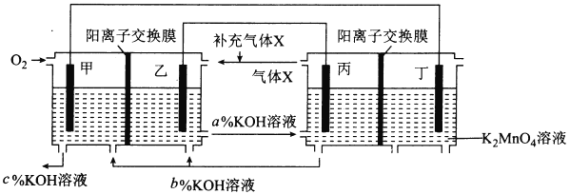
A. 甲为正极,丙为阴极
B. 丁极的电极反应式为MnO42――e-===MnO4-
C. KOH溶液的质量分数:c%>a%>b%
D. 标准状况下,甲电极上每消耗22.4L气体时,理论上有4molK+移入阴极区
高三化学单选题困难题查看答案及解析
一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是
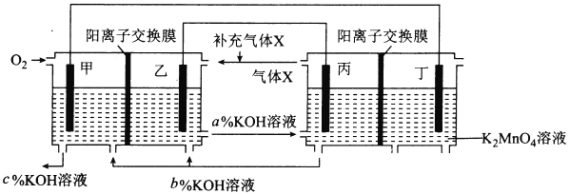
A. 甲为正极,丙为阴极
B. 丁极的电极反应式为MnO42――e-===MnO4-
C. KOH溶液的质量分数:c%>a%>b%
D. 标准状况下,甲电极上每消耗22.4L气体时,理论上有4molK+移入阴极区
高三化学单选题困难题查看答案及解析
一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是

A. 甲为正极,丙为阴极
B. 丁极的电极反应式为MnO42――e-===MnO4-
C. KOH溶液的质量分数:c%>a%>b%
D. 标准状况下,甲电极上每消耗22.4L气体时,理论上有4molK+移入阴极区
高三化学单选题困难题查看答案及解析
一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是

A. 电极丁的反应式为MnO42- -e-= MnO4-
B. 电极乙附近溶液的pH减小
C. KOH溶液的质量分数:c%>a%>b%
D. 导线中流过2 mol电子时,理论上有2molK+移入阴极区
高三化学选择题困难题查看答案及解析
“84”消毒液(主要成分为)广泛应用于杀菌消毒。某化学学习小组用甲烷燃料电池电解饱和食盐水制备“84”消毒液,装置如图所示,
,
,
,
均为惰性电极,下列说法正确的是( )
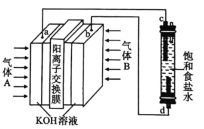
A.气体B为甲烷
B.电解装置中的总反应为NaCl+H2ONaClO+H2↑
C.消耗2.24L(标准状况)甲烷,K+通过交换膜向左室移动0.8mol
D.甲烷发生的电极反应方程式为CH4-8e-+8OH—=CO2↑+6H2O
高三化学单选题中等难度题查看答案及解析
用镁—次氯酸钠燃料电池作电源模拟消除工业酸性废水中的的过程(将
还原为
),装置如图所示。下列说法正确的是
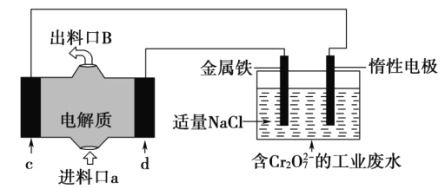
A.燃料电池负极反应式为
B.装置中电子的流动路线是c电极→惰性电极→金属铁电极→d电极
C.装置工作过程中消耗,理论上可消除
D.将处理后的废水比原工业废水的pH小
高三化学单选题中等难度题查看答案及解析
二甲醚(CH3OCH3)直接燃料电池具有启动快、效率高等优点,用二甲醚燃料电池电解甲基肼(CH3—NH—NH2)制氢的装置如图所示,其中X、Y、M、N均为惰性电极。下列说法正确的是( )
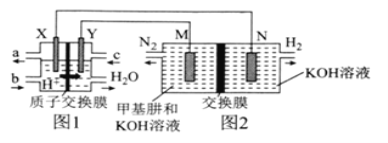
A.M极的电极反应式为CH3—NH—NH2+12OH--10e-=CO+N2↑+9H2O
B.图1中电解质溶液的pH减小,图2中电解质溶液的pH增大
C.图2中的交换膜是阴离子交换膜,OH-透过交换膜向N极移动
D.理论上,当生成6.72LH2时,消耗CH3OCH3的质量为2.3g
高三化学单选题中等难度题查看答案及解析
肼一双氧水燃料电池由于其较高的能量密度而广受关注,其工作原理如图所示。下列有关说法中正确的是
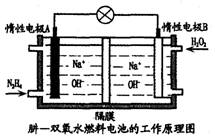
A. 惰性电极A作正极
B. 正极电极反应式为H2O2 +2e-==2OH-
C. 电解质溶液中的Na+从B极区迁移到A极区
D. 电池工作过程中,A极区溶液的pH增大
高三化学选择题困难题查看答案及解析
已知H2O2是一种弱酸,在强碱溶液中主要以HO2-形式存在。现以Al—H2O2燃料电池电解尿素[CO(NH2)2]的碱性溶液制备氢气 (电解池中隔膜仅阻止气体通过,c、d均为惰性电极)。下列说法正确的是
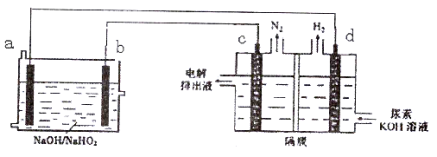
A.燃料电池的总反应为:2Al+3HO2- = 2AlO2- + 2H2O
B.电解时,Al消耗2.7g,则产生氮气的体积为1.12L
C.电极b是负极,且反应后该电极区pH增大
D.电解过程中,电子的流向由a→d,c→b。
高三化学选择题困难题查看答案及解析
已知H2O2是一种弱酸,在强碱溶液中主要以HO2-形式存在。以Al—H2O2燃料电池电解尿素[CO(NH2)2]的碱性溶液制备氢气 (电解池中隔膜仅阻止气体通过,c、d均为惰性电极)。下列说法不正确的是
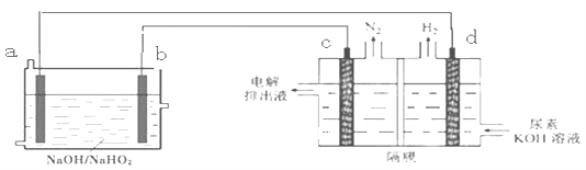
A.燃料电池的总反应为:2Al+3HO2- = 2AlO2- + OH- +H2O
B.电极b是正极,且反应后该电极区pH增大
C.电解过程中,电子的流向由a→b→c→d.
D.电解时,Al消耗2.7g,则产生氮气标准状况下为1.12L
高三化学选择题中等难度题查看答案及解析