-
铁是应用最广泛的金属,铁的卤化物、氧化物、硫酸盐以及高价铁的含氧酸盐均为重要化合物。
(1)在实验室中,FeCl2 可用铁粉和盐酸反应制备,FeCl3可用铁粉和_____反应制备: 现有一含FeCl2和FeCl3的混合物的样品,测得样品中n(Fe):n(Cl) = 1:2.3,则该样品中FeCl3的物质的量分数为____________。
(2)高温下,Fe 与水蒸气反应的化学方程式为____________________。
(3)硫酸亚铁、氯化亚铁溶液存放在实验室均易变质,出现红褐色沉淀,且溶液变棕黄色,则此反应的离子方程式为____________________。
(4)在氯化亚铁溶液中加入等物质的量的过氧化钠,发生反应的总的离子方程式为____________________。
高一化学填空题中等难度题查看答案及解析
-
铁是应用最广泛的金属,铁的氯化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)请写出Fe与水蒸气反应的化学方程式:_____________。
(2)在实验室中,FeCl2可用铁粉和______(填名称)反应制备。
(3)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为______。
(4)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:_________________。
(5)现有一含有FeCl2 和FeCl3的混合物样品,实验测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为_________。
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:____________。
高一化学填空题中等难度题查看答案及解析
-
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要的化合物.
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法.实验中称取0.54g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH﹣的阴离子交换柱,使Cl﹣和OH﹣发生交换.交换完成后,流出溶液的OH﹣用0.40mol/L的盐酸滴定,滴至终点时消耗盐酸25.00mL.则样品中氯的物质的量为________ ,x=________ ;
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则样品中FeCl3的物质的量分数为________ .实验中,FeCl2可用铁粉与_________反应制得,FeCl3可用铁粉与________ 反应制得;
(3)氧化铁与氢碘酸反应的离子方程式为________ ;
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料.FeCl3与KClO在强碱性溶液中反应制取(K2FeO4),其反应的离子方程式为 ________ .
高一化学综合题中等难度题查看答案及解析
-
铁是应用最广泛的金属,铁的卤化物也是一种重要化合物。
(1)在实验室中,FeCl2可用铁粉和___________反应制取,FeCl3可用铁粉和___________反应制取。现有含FeCl2和FeCl3的混合物样品,测得n(Fe):n(Cl)=1:2.4,则该样品中FeCl3的物质的量分数为________________。
(2)FeCl2易被氧化,检验一瓶FeCl2溶液是否被氧化的方法(写出操作步骤、现象及结论)是______________。向FeCl2溶液中加入NaOH溶液,开始时生成白色沉淀,后马上变成灰绿色,最终变成红褐色,沉淀变色发生反应的化学方程式为_________________。
高一化学填空题困难题查看答案及解析
-
铁是应用最广泛的金属,铁的氧化物、卤化物以及硫酸盐均为重要化合物。
(1)氧化铁为红棕色粉末,该物质难溶于水,易溶于盐酸中,请写出该物质与盐酸反应的离子方程式________。
(2)铁在氯气中剧烈燃烧,产生红棕色的烟,将燃烧所得的三氯化铁溶于水,所得溶液的质量分数为16.25%,其密度为6.0g· mL-1,则该溶液中氯离子的物质的量浓度为__________;将上述所配制的溶液稀释为0.15mol/L 的稀溶液480mL,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管之外,还需要___;量取该溶液的体积是_______________mL;在配制过程中如果定容时俯视刻度线,会造成所配溶液浓度____(填“偏高”、“偏低”或“无影响”)。
(3)将饱和FeCl3溶液滴入沸腾的蒸馏水中,可以制得Fe(OH)3胶体,请写出该过程的化学反应方程式______,以下关丁Fe(OH)3胶体的说法中不正确的有_____________(填序号)。
A. Fe(OH)3胶体是一种红褐色、澄清、透明的混合物
B. Fe(OH)3胶体中分散质的微粒直径在10-9m~10-7m 之间
C.用渗析法鉴别Fe(OH)3胶体和FeCl3 溶液,用丁达尔效应分离Fe(OH)3胶体和FeCl3 溶液
D.取少量Fe(OH)3胶体置于试管中,向试管中逐滴滴加稀硫酸,可看到先产生红褐色沉淀,随后沉淀溶解,最终得到黄色的溶液
E.将其装入U 形管内,用石墨作电极,接通直流电,通电一段时间后发现靠近正极区附近的颜色逐渐变深
(4)在硫酸铁溶液中,逐滴加入等浓度的氢氧化钡溶液,其溶液的导电性随氢氧化钡溶液体积增加而变化的图象是_______。

高一化学综合题简单题查看答案及解析
-
二氧化硫是硫的重要化合物,在生产,生活中有广泛应用。二氧化硫有毒,并且是形成酸雨的主要气体。无论是实验室制备还是工业生产,二氧化硫尾气吸收或烟气脱硫都非常重要。完成下列填空:
(1)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
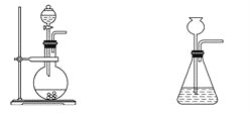
A.装置a B装置b
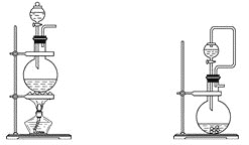
C.装置c D.装置d
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是 _________(填写字母)。
(2)若用硫酸和亚硫酸钠反应制取3.36 L(标准状况)二氧化硫,至少需要称取亚硫酸钠____________________g(保留一位小数);如果已有4.0%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠________g (保留一位小数)。
(3)实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰-石膏法和碱法是常用的烟气脱硫法。石灰-石膏法的吸收反应为SO2+Ca(OH)2=CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O=2CaSO4·2H2O。其流程如下图:
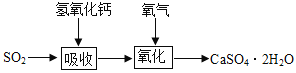
碱法的吸收反应为SO2+2NaOH=Na2SO3+H2O。碱法的特点是氢氧化钠碱性强,吸收快,效率高。其流程如下图:
已知:

石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是 _____________________。和碱法相比,石灰-石膏法的优点是__________________,缺点是__________________。
(4)在石灰-石膏法和碱法的基础上,设计一个改进的,能实现物料循环的烟气脱硫方案(用流程图表示) _______。
高一化学综合题困难题查看答案及解析
-
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
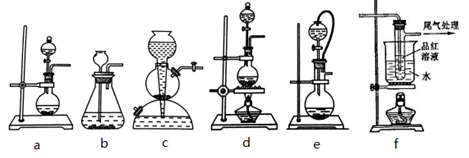
(1)如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装
置是 (填写字母),e装置中的导管作用为 。
(2)工业上制备Na2S2O3反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,某研究小组在实验室制备Na2S2O3·5H2O流程如下:

吸硫装置如图所示:
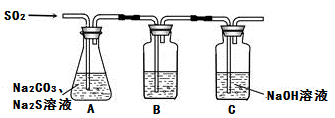
①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ,表明SO2吸收效率低的实验现象是B中溶液 。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是 。
③用双线桥表示下面化学反应的电子转移方向和数目:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。
④Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:准确称取0.214g KIO3固体配成溶液,加入过量KI固体和H2SO4溶液,再向其中加入Na2S2O3与之反应,消耗Na2S2O3 溶液的体积为24mL时恰好完全反应。则c(Na2S2O3)= 。
(已知:IO3-+5I-+6H+=3I2+3H2O 2S2O32-+I2=S4O62-+2I-)
高一化学实验题困难题查看答案及解析
-
铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
(1)生铁含有 C、Si、Mn、S、P 等元素,其中属于金属元素的除 Fe 外,还有_______元 素。
(2)铁元素有三种常见的氧化物,分别是 FeO、Fe2O3、Fe3O4。其中具有磁性的是 ____________,可作为红色颜料的是____________。
(3)某补铁口服液中含有 Fe2+,为检验其是否被氧化变质,可取少量该口服液,向其中 滴加 KSCN 溶液,若溶液变为____________色,则说明其已变质。向该口服液中加入维生素 C 可防止其被氧化变质,此过程中利用了维生素 C 的____________性。
(4)FeCl3可作为铜电路板的腐蚀液,其反应原理为Cu与FeCl3溶液反应生成FeCl2和CuCl2, 该反应的化学方程式为____________。向反应后的溶液中加入____________,可回收 Cu,并得到 FeCl2 溶液。
高一化学填空题中等难度题查看答案及解析
-
下列说法正确的是( )
A.ⅠA族元素的金属性一定比ⅡA族元素的金属性强
B.第三周期中的非金属元素的气态氢化物还原性越强,对应元素的最高价含氧酸酸性越弱
C.非金属元素之间只能形成共价化合物
D.短周期中,同周期元素的离子半径从左到右逐渐减小
高一化学单选题简单题查看答案及解析
-
同周期的X、Y、Z三元素,它们最高价氧化物对应水化物是HXO4、H2YO4、H3ZO4 ,则下列判断正确的是
A.含氧酸的酸性H3ZO4>H2YO4>HXO4
B.非金属性X>Y>Z
C.元素的负化合价的绝对值按X、Y、Z变小
D.气态氢化物的稳定性按X、Y、Z的顺序增强
高一化学选择题中等难度题查看答案及解析