-
氯碱工业中电解饱和食盐水的原理示意图如下图所示:

(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是 ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用 ;
(4)电解所用的盐水需精制。去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42->c(Ca2+)]。精致流程如下(淡盐水和溶液A来自电解池):
①盐泥a除泥沙外,还含有的物质是 。
②过程Ⅰ中将NH4+转化为N2的离子方程式是 。 ③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有 。
-
氯碱工业中电解饱和食盐水的原理示意图如下图所示:
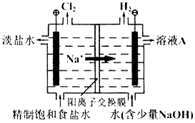
(1)溶液A的溶质是________;
(2)电解饱和食盐水的离子方程式是________;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用________;
(4)电解所用的盐水需精制。去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42->c(Ca2+)]。精致流程如下(淡盐水和溶液A来自电解池):
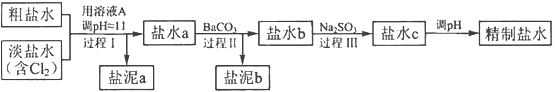
①盐泥a除泥沙外,还含有的物质是________。
②过程Ⅰ中将NH4+转化为N2的离子方程式是________
③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有________
-
氯碱工业中电解饱和食盐水的原理示意图如右图所示.
(1)溶液A的溶质是______.
(2)电解饱和食盐水的离子方程式是______ H2↑+Cl2↑+2OH-

-
氯碱工业中电解饱和食盐水的原理示意图如右图所示

(1)溶液A的溶质是________;
(2)电解饱和食盐水的离子方程式是________
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用________
(4)电解所用的盐水需精制。去除有影响的 、
、 ,NH+3,
,NH+3, ,[
,[ >
> ]。
]。
精致流程如下(淡盐水和溶液A来电解池):

①盐泥a除泥沙外,还含有的物质是________。
②过程Ⅰ中将NH4+转化为N2的离子方程式是________
③ 的溶解度比
的溶解度比 的小,过程Ⅱ中除去的离子有________
的小,过程Ⅱ中除去的离子有________
④经过程Ⅲ处理,要求盐水中c 中剩余 的含量小于5mg /l ,若盐水b中
的含量小于5mg /l ,若盐水b中 的含量是7.45 mg /l ,则处理10m3 盐水b ,至多添加10%
的含量是7.45 mg /l ,则处理10m3 盐水b ,至多添加10%  溶液 ________kg(溶液体积变化忽略不计)。
溶液 ________kg(溶液体积变化忽略不计)。
-
氯碱工业中电解饱和食盐水的原理示意图如下图所示:

(1)溶液A的溶质是________________________________________________________________________________________________________________________________________ ;
(2)电解饱和食盐水的离子方程式是________________________________________________________________________________________________________________________________________________________________________________________________________________________________________ ;
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用________________________ ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________;
(4)电解所用的盐水需精制。去除有影响的Ca2+、Mg2+、NH4+、SO42-[c(SO42->c(Ca2+)]。精制流程如下(淡盐水和溶液A来自电解池):

①盐泥a除泥沙外,还含有的物质是________________________________________________________________________________ 。
②过程Ⅰ中将NH4+转化为N2的离子方程式是________________________________________________________________________________________________ ;
③BaSO4的溶解度比BaCO3的小,过程Ⅱ中除去的离子有________________________________________ 。
-
海洋中有丰富的食品、矿产,能源、药物和水产资源等(如下图所示)
下列有关说法正确的是
A. 氯碱工业中电解饱和食盐水的离子方程式为:2Cl- +2H+  H2↑+ Cl2↑
H2↑+ Cl2↑
B.第②步中结晶出的MgCl2·6H2O可在空气中受热分解得到纯净的无水MgCl2
C.在第③④⑤步中溴元素均被氧化
D.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:BaCl2
-
下列离子方程式正确的是
A. 氯碱工业中电解饱和食盐水:2Cl﹣+2H2O H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
B. 氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+
C. 氢氧化钠溶液吸收少量二氧化硫SO2+OH﹣=HSO3﹣
D. 稀硫酸中加氢氧化钡溶液至中性:Ba2++H++OH﹣+SO42﹣=BaSO4↓+H2O
-
氯碱工业是以电解饱和食盐水为基础的基本化学工业。下图是某氯碱工业生产原理示意图:
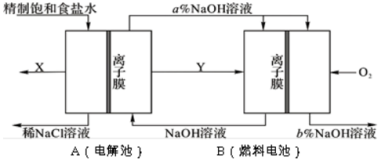
(1)写出装置A在通电条件下反应的化学方程式______________。
(2)A装置所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+和Ca2+,要加入的试剂分别为___________、___________。
(3)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能30%以上,且相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中Y是______________(填化学式);X与稀NaOH溶液反应的离子方程式是:______________。
②分析比较图示中氢氧化钠质量分数a%与b%的大小___________。
③若用B装置作为A装置的辅助电源,每当消耗标准状况下氧气的体积为11.2 L时,则B装置可向A装置提供的电量约为______________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
-
工业上生产氯气常用电解槽中电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分。下图(左图)为电解槽的示意图。
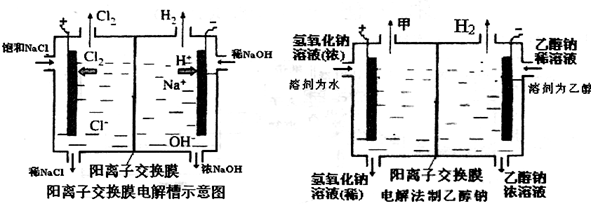
(1)这种阳离子交换膜,只允许溶液中的________通过。(填下列微粒的编号)
①H2 ②Cl2 ③H+ ④Cl- ⑤Na+ ⑥OH-
(2)写出在电解过程中发生的电极方程式阳极:________。
(3)已知某电解槽每小时加入10%的氢氧化钠溶液10kg,每小时能收集到标况下的氢气896L,而且两边的水不能自由流通。则理论上计算,电解后流出的氢氧化钠溶液的质量分数为________。
(4)某化学课外兴趣小组设计了用电解法制取乙醇钠的工业方法,所用的电解槽如上右图所示,设计要求:①所用的交换膜不能让分子自由通过;②电解过程中消耗的原料是氢氧化钠和乙醇。回答下列问题:
①写出在电解过程中发生的电极方程式
阴极:________。
②最后从乙醇钠的乙醇溶液中分离得到纯净乙醇钠固体的方法是:________。
-
工业上电解饱和食盐水能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1) 右图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是 ; NaOH溶液的出口为______ (填字母);精制饱和食盐水的进口为_____ (填字母);干燥塔中使用的液体干燥剂是____(每空2分)。
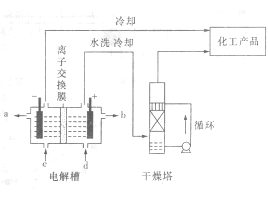
(2) 原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加人的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是 (2分)(填序号)。
(3) 多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 ________(2分)。 也可转化为
也可转化为 而循环使用。一定条件下,在200C恒容密闭容器中发生反应:
而循环使用。一定条件下,在200C恒容密闭容器中发生反应: 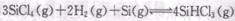 ,达平衡后,H2与SiHCL3物质的量浓度分别为0. 140mol/L和0. 020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的物质的量为_______ (2分)mol。
,达平衡后,H2与SiHCL3物质的量浓度分别为0. 140mol/L和0. 020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的物质的量为_______ (2分)mol。
(4)已知1 g阴极产生的气体在阳极产生的气体中完全燃烧时放出92. 3 kj的热量,则该反应的热化学方程式为: ________________(2分)。












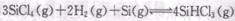 ,达平衡后,H2与SiHCL3物质的量浓度分别为0. 140mol/L和0. 020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的物质的量为_______ (2分)mol。
,达平衡后,H2与SiHCL3物质的量浓度分别为0. 140mol/L和0. 020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的物质的量为_______ (2分)mol。