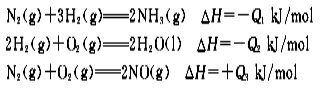-
[物质结构与性质]
将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染。工业 上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)如图是某同学画出CO分子中氧原子的 核外电子排布图:
核外电子排布图: ,请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
,请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
(2)写出与CO互为等电子体(电子总数相等)的一种分子和一种离子的化学式 。
(3)向CuSO4溶液中加入足量氨水可得到深蓝 色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > > (填元素符号)。
色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > > (填元素符号)。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是 ;在甲醇分子中碳原子轨道的杂化类型为 。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:
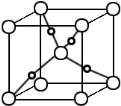
① 在该晶胞中,Cu+ 的配位数是 ,
② 若该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
-
将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)右图是某同学画出CO分子中氧原子的核外电子排布图,

请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
(2)写出两种与CO互为等电子体的离子 。
(3)向CuSO4溶液中加入足量氨水可得到深蓝色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > > (填元素符号)。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是 ;在甲醇分子中碳原子轨道的杂化类型为 。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:
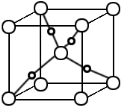
①在该晶胞中,Cu+ 的配位数是 ,
②若 该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
-
将汽车尾气中含有的CO利用不仅能有效利用资源,还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元素形成的催化剂作用下合成甲醇。
(1)右图是某同学画出CO分子中氧原子的核外电子排布图,

请判断该排布图 (填“正确”或“错误”),理由是 (若判断正确,该空不用回答)。
(2)写出两种与CO互为等电子体的离子 。
(3)向CuSO4溶液中加入足量氨水可得到深蓝色[Cu(NH3)4]SO4溶液,[Cu(NH3)4]SO4中 所含配位键是通过配体分子的 给出孤电子对, 接受电子对形成,SO42-的空间构型是 ,该物质中N、O、S三种元素的第一电离能大小顺序为 > > (填元素符号)。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是 ;在甲醇分子中碳原子轨道的杂化类型为 。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图所示:

①在该晶胞中,Cu+ 的配位数是 ,
②若 该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
-
将汽车尾气中含有的CO利用不仅能有效利用资源.还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元索形成的催化剂作用下合成甲醇。
(1)图l是某同学画出CO分子中权原子的核外电子排布图。

请判断该排布图____(填“正确”或“错误”) ,理由是________ (若判断正确,该空不用回答)。
(2)写出两种与CO互为等电子体的离子________。
(3)往硫酸铜溶液中通入过量的NH3,可生成配离子[Cu(NH3 )4]2+,但NF3不易与Cu2+形成配离子,其原因是_________,在配离子[Cu(NH3 )4]2+中所含配位键是通过配体分子的_____给出孤电子对,____接受电子对形成。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是______;在甲醇分子中碳原子轨道的杂化类型为_____。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图2所示。①在该晶胞中,Cu+的配位数是_____。
②若该晶胞的边长为apm,则Cu2O的密度为_____g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
-
大气污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。
(1)汽车尾气中的CO、NOx、碳氢化合物是大气污染物。
①使用稀土等催化剂能将CO、NO 转化成无毒物质。
已知:N2(g)+O2(g)=2NO(g) △H1=+180.5kJ·mol-1
2C(s)+O2(g)=2CO(g) △H2=-221kJ·mol-1
C(s) +O2(g) =CO2(g) △H3=-393.5kJ·mol-1
写出NO(g) 与CO(g)催化转化成N2(g)和CO2(E)的热化学方程式__________________。
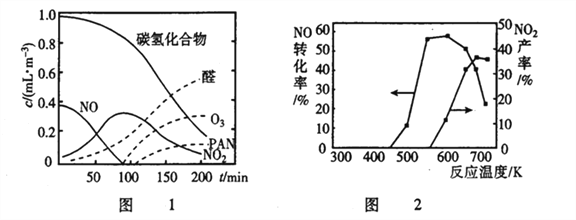
②醛类、O3、PAN( 过氧硝酸乙酰) 等污染物气体和颗粒物所形成的烟雾称为光化学烟雾。某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图 1所示。请你根据光化学烟雾的形成原理,对减少光化学烟雾的发生提出一个合理建议___________________。
(2)利用NH3催化还原氮氧化物(SCR 技术)是目前应用广泛的烟气脱硝技术。
①SCR 技术的主要化学反应之一是2NH3(g)+NO(g)+NO2(g)  2N2(g)+3H2O(g) △H,则该反应的化学平衡常数表达式K=__________。该反应的平衡常数K随温度T的升高而减小,则该反应的△H__________0 (填“>”、“ <”或“”=)。
2N2(g)+3H2O(g) △H,则该反应的化学平衡常数表达式K=__________。该反应的平衡常数K随温度T的升高而减小,则该反应的△H__________0 (填“>”、“ <”或“”=)。
②SCR技术的另一主要反应为4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g)△H=-1627.2kJ·mol-1。NO 和NH3在有氧条件及Ag2O催化作用下,当反应温度升高到550~700℃,NO转化率明显下降,NO2 产率明显上升(见图2)的可能原因是______________。(用化学方程式表达)
4N2(g)+6H2O(g)△H=-1627.2kJ·mol-1。NO 和NH3在有氧条件及Ag2O催化作用下,当反应温度升高到550~700℃,NO转化率明显下降,NO2 产率明显上升(见图2)的可能原因是______________。(用化学方程式表达)
(3)目前,科学家还在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图3,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图4所示。
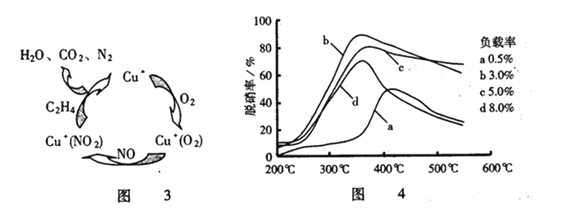
①写出该脱硝原理总反应的化学方程式______________________。
②为达到最佳脱硝效果,应选择的条件是______________________。
-
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。硫、氮氧化物是形成酸雨、雾霾等环境污染的罪魁祸首,采用合适的措施消除其污染是保护环境的重要措施。
Ⅰ.研究发现利用NH3可消除硝酸工业尾气中的NO污染。NH3与NO的物质的量之比分别为1:3、3:l、4:1时,NO脱除率随温度变化的曲线如图所示。
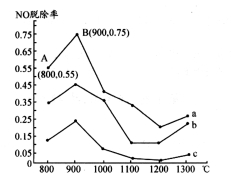
(1)①曲线a中,NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为 mg/(m3·s)。
②曲线b对应的NH3与NO的物质的量之比是 ,其理由是
(2)已知在25℃,101kPa时:
N2(g)+3H2(g) === 2NH3(g) △H=-Q1/mol
2H2(g)+O2(g) === 2H2O(1) △H=- Q2kJ/mo1
N2(g) +O2(g) === 2NO(g) △H=+ Q3kJ/mo1
请写出用NH3脱除NO的热化学方程式 。
Ⅱ.工业上还可以变“废”为“宝”,将雾霾里含有的SO2、NO等污染物转化为Na2S2O4(保险粉)和NH4NO3等化工用品,其生产流程如下:
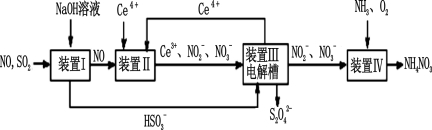
(3)装置Ⅱ中NO转变为NO3-的反应的离子方程式为 。
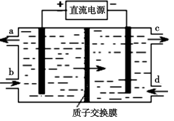
(4)装置Ⅲ制得Na2S2O4的同时还能让Ce4+再生,原理如图所示。其阴极的电极反应式为 : 。
(5)按上述流程处理含有amolSO2、bmolNO的雾霾(b>a),并制取Na2S2O4和NH4NO3。装置Ⅰ中SO2、装置Ⅱ中NO、装置Ⅲ中HSO3-和Ce3+、装置Ⅳ中NO2-全部转化,处理完毕后装置Ⅱ中Ce4+的剩余量与加入量相比没有变化,则至少需向装置Ⅳ中通入标准状况下的O2 L(用含a、b的代数式表示)。
-
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。硫、氮氧化物是形成酸雨、雾霾等环境污染的罪魁祸首,采用合适的措施消除其污染是保护环境的重要措施。
Ⅰ.研究发现利用NH3可消除硝酸工业尾气中的NO污染。NH3与NO的物质的量之比分别为1:3、3:l、4:1时,NO脱除率随温度变化的曲线如图所示。
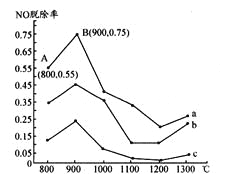
(1)①曲线a中,NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为_____mg/(m3·s)。
②曲线b对应的NH3与NO的物质的量之比是______,其理由是_________。
(2)已知在25℃,101kPa时:
N2(g)+3H2(g) =2NH3(g) △H=-Q1/mol
2H2(g)+O2(g) =2H2O(1) △H=- Q2kJ/mo1
N2(g) +O2(g) = 2NO(g) △H=+ Q3kJ/mo1
请写出用NH3脱除NO的热化学方程式__________。
Ⅱ.工业上还可以变“废”为“宝”,将雾霾里含有的SO2、NO等污染物转化为Na2S2O4(保险粉)和NH4NO3等化工用品,其生产流程如下:
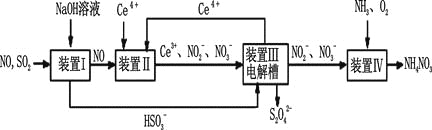
(3)装置Ⅱ中NO转变为NO3-的反应的离子方程式为__________。
(4)装置Ⅲ制得Na2S2O4的同时还能让Ce4+再生,原理如图所示。其阴极的电极反应式为 :______。
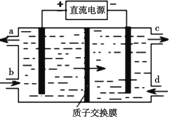
(5)按上述流程处理含有amolSO2、bmolNO的雾霾(b>a),并制取Na2S2O4和NH4NO3。装置Ⅰ中SO2、装置Ⅱ中NO、装置Ⅲ中HSO3-和Ce3+、装置Ⅳ中NO2-全部转化,处理完毕后装置Ⅱ中Ce4+的剩余量与加入量相比没有变化,则至少需向装置Ⅳ中通入标准状况下的O2____L(用含a、b的代数式表示)。
-
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。硫、氮氧化物是形成酸雨、雾霾等环境污染的罪魁祸首,采用合适的措施消除其污染是保护环境的重要措施。
I.研究发现利用NH3可消除硝酸工业尾气中的NO污染。NH3与NO的物质的量之比分别为1:3、3:1、4:1时,NO脱除率随温度变化的曲线如图所示。
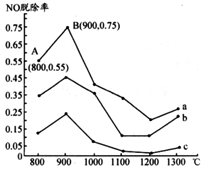
(1)①曲线a中,NO的起始浓度为6×10-4mg/m3,从A 点到B点经过0.8 s,该时间段内NO的脱除速率为____________mg/(m3·s)。
②曲线b对应的NH3与NO的物质的量之比是____,其理由是___________________
(2)已知在25℃,101 kPa时:
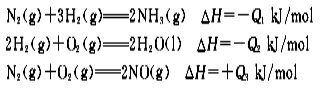
请写出用NH3脱除NO的热化学方程式:____________________________________
Ⅱ.工业上还可以变“废”为“宝”,将雾霾里含有的SO2、NO等污染物转化为Na2S2O4(保险粉)和NH4NO3等化工用品,其生产流程如下图:
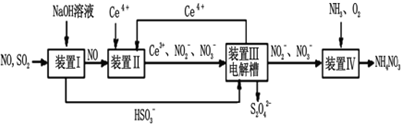
(3)装置Ⅱ中NO转变为NO3-的反应的离子方程式为__________________________________
(4)装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1 mol CH4 时,理论上可再生____mol Ce4+。
-
(14分)工业上通常用下列方法治理含氮化合物的污染。
(1)用稀土等催化剂能将汽车尾气中的CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染。已知:
①N2(g)+ O2(g)=2NO(g) △H=+180.5 kJ/mol ②2C(s)+ O2(g)=2CO(g) △H=—221.0 kJ/mol
③C(s)+ O2(g)=CO2(g) △H=—393. 5 kJ/mol
写出NO(g)与CO(g)催化转化成N2(g)和CO2(g)的热化学方程式 。
(2)用NH3还原NOx生成N2和H2O。现有NO、NO2的混合气3 L,可用同温同压下3.5 L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为 。
(3)电化学降解治理水中硝酸盐污染。在酸性条件下,电化学降解NO的原理如图1,A为电源的 极,阴极反应式为 。
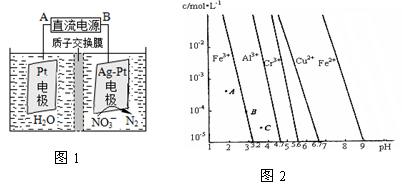
(4)通过控制溶液的pH对工业废水中的金属离子进行分离。图2是某些金属氢氧化物在不同浓度和pH时的沉淀——溶解图像,图中直线上的点表示平衡状态。当溶液中的离子浓度小于1×10-5 mol·L-1时,认为该离子沉淀完全。
①Fe (OH)3、Al(OH)3、Cr(OH)3三种物质的溶度积常数最大的是 ,
图中A、B、C三点中表示Fe(OH)3的沉淀速率大于溶解速率的是 。
②由图可得Fe(OH)2的溶度积的值为 。
-
NOx是汽车尾气中的主要污染物之一。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_____________。
(2)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:_______________________________________。
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO。原因是_______________,
元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强。


该晶胞的边长为a pm,则Cu2O的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
 ,请判断该排布图
,请判断该排布图