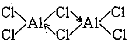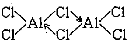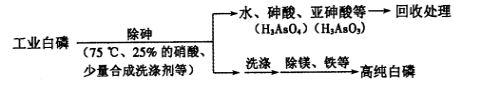-
金属Mg及其化合物有重要的用途,请回答下列问题
(1)MgO的重要用途有_______。(写出一种)
(2)井水中含有较多的Ca2+、Mg2+、HCO3-等离子,可以通过煮沸的方式将Mg2+转化为Mg(OH)2,发生的离子方程式是:__________________。
(3)金属Mg可以用来冶炼Ti:2Mg+TiCl4 Ti+2MgCl2。可以用作该反应保护气的是_______。
Ti+2MgCl2。可以用作该反应保护气的是_______。
A. He B. C02 C.N2 D.HCl
(4)在蒸发皿中放人研细的碘和镁粉,无现象,滴入几滴水后立即产生大量的紫烟,紫烟的成分是_________(填分子式);对于实验中水的作用,甲同学认为是水溶解了I2,增大了I2与Mg的接触面积,导致了反应加快,乙同学认为是I2与H2O反应生成了酸,是酸与Mg反应放出热量,加快了I2与Mg的反应,请利用供选试剂:0.01mol/L I2的CCl4溶液、0.01 mol/L I2水、I2粉、Mg粉、蒸馏水,设计实验证明哪位同学的说法合理:____________。(包括实验过程、现象和结论)
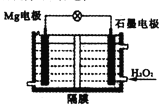
(5)一种新型的Mg-H2O2酸性介质电池工作原理如图,正极发生的电极方程式为:__________。
-
金属铁及其化合物在材料、航空工业上有重要用途。回答下列相关问题:
(1)基态钛原子中有__________个状态不同的电子,最高能层电子的电子云轮廓图形状为__________,写出其价电子的轨道表达式__________。
(2)化合物TiO2不仅是常用的白色颜料,也是一些反应的良好催化剂,如:
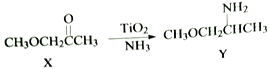
有机物X中C原子的杂化轨道类型为__________,1mol Y中所含σ键的数目是__________。
(3)已知TiCl4在常温下是无色液体,TiCl4的晶体类型是__________晶体,其空间构型是__________。
(4)自然界中有丰富的钛矿资源,如右图表示的是钡钛矿晶体的晶胞结构,经X射线分析,该晶胞为正方体,晶胞参数为apm。
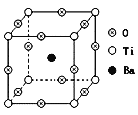
写出钡钛矿晶体的化学式__________,其密度是__________g·cm-3。
-
镁铝合金在工业上有着广泛的用途,氧化铝是冶炼金属铝的主要原料。从铝土矿(主要成分是Al2O3,含有SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
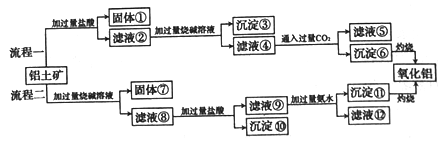
回答下列问题:
(1)Al2O3、SiO2、Fe2O3、MgO四种物质中,属于酸性氧化物的是______,属于碱性氧化物的是______。
(2)流程一中,沉淀③是_________(填化学式,下同),沉淀⑥是_________。
(3)流程二中,加入烧碱溶解SiO2的化学方程式为_________。
(4)滤液⑤中的可溶性盐是NaCl、______(填化学式),滤液⑨与过量氨水反应的离子方程式为_____。
(5)在电解氧化铝制取金属铝的反应中,氧化产物与还原产物的质量之比为______。
-
下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A.D为金属单质,其他均为化合物.试回答下列问题:
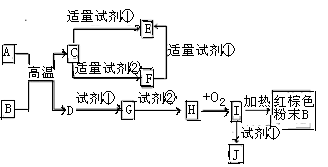
(1)写出物质C的化学式:________
(2)写出物质B的一种用途:________
(3)以J的饱和溶液制备胶体的操作为________
________。
(4)写出下列反应的方程式:
A→F的离子方程式________.
H→I的化学方程式
试剂②可以由一种淡黄色固体粉末和一种常见液体发生反应而制得,其相应的化学方程式________
(5)某同学认为J中可能同时含有同一种金属元素的两种阳离子,若要确认其中低价金属阳离子的存在,应选用________(选填序号)
A、KSCN溶液和氯水 B、铁粉和KSCN溶液 C、浓氨水 D、酸性高锰酸钾
-
Cl2及其化合物在生产、生活中有广泛用途,回答下列问题。
(1)氯气溶于水得到氯水,氯水中含有氯元素并且具有氧化性的微粒有 。
(2)新制氯水体系中,存在多个含氯元素之间的平衡关系,请写出任意两个平衡关系: 。
(3)25℃时将氯气溶于水形成氯气-氯水体系,该体系中Cl2(aq)、HClO和ClO-三种微粒分别所占分数(α)随pH变化的关系如下图所示。
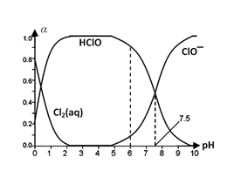
已知HClO的杀菌能力比ClO-强,由图分析,用氯气处理饮用水时,pH=7.5与pH=6时杀菌效果较强的是pH= 。
(4)ClO2是一种更高效的杀菌消毒剂,工业上可用电解法制备ClO2,方法如下:在80℃时电解氯化钠饱和溶液得到NaClO3,然后与盐酸反应得到ClO2。电解时,产生ClO3-的电极是 极,生成ClO3-的电极反应式为 。
(5)已知PCl5的热分解反应为:PCl5(g) PCl3(g)+Cl2(g),某温度下,在固定容积为10.0 L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.15 mol/L。
PCl3(g)+Cl2(g),某温度下,在固定容积为10.0 L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.15 mol/L。
①上述反应达到平衡后继续向容器充入PCl5,则上述平衡将 移动(填“正向”、“逆向”或“不”),PCl5的转化率将 (填“增大”、“减小”或“不变”)。
②计算该温度下PCl5(g) PCl3(g)+Cl2(g)的平衡常数K(写出计算过程)。
PCl3(g)+Cl2(g)的平衡常数K(写出计算过程)。
-
【物质与结构—选作】硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),更高温度下Al2Cl6则离解生成A1Cl3单分子。
①固体氯化铝 的晶体类型是 ;
的晶体类型是 ;
②写出Al2Cl6分子的结构式 ;
③单分子A1Cl3的立体构型是 ,缔合双分子
Al2Cl6中Al原子的轨道杂化类型是 。
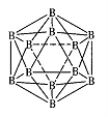
(3)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图),若其中有两个原子为10 B,其余为11B,则该结构单元有 种不同的结构类型。
(4)金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,计算确定其晶胞的类型(简单、体心或面心立方)  ;晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)= pm。
;晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)= pm。
-
【物质结构与性质】硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),结构如图
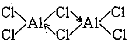
缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。
(3)B原子的电子有 个不同的能级;晶体硼熔点为2300℃,则其为 晶体。
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,它是通过在高温氢气氛围下(>750℃)三溴化硼和三溴化磷反应制得。BP晶胞如图所示。
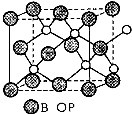
①画出三溴化硼和三溴化磷的空间结构式。
三溴化硼 三溴化磷
②在BP晶胞中B的堆积方式为 。
③计算当晶胞晶格参数为a pm(即图中立方体的每条边长为 a pm)时,磷化硼中硼原子和磷原子之间的最近距离 。
-
【物质结构与性质】硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),结构如图
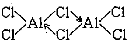
缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。
(3)B原子的电子有 个不同的能级;晶体硼熔点为2300℃,则其为 晶体。
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,它是通过在高温氢气氛围下(>750℃)三溴化硼和三溴化磷反应制得。BP晶胞如图所示。

①画出三溴化硼和三溴化磷的空间结构式。
三溴化硼 三溴化磷
②在BP晶胞中B的堆积方式为 。
③计算当晶胞晶格参数为a pm(即图中立方体的每条边长为 a pm)时,磷化硼中硼原子和磷原子之间的最近距离 。
-
硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),更高温度下Al2Cl6则离解生成A1Cl3单分子。
①固体氯化铝的晶体类型是 ;
②写出Al2Cl6分子的结构式 ;
③单分子A1Cl3的立体构型是 ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是  。
。
(3)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图),若其中有两个原子为10 B,其余为11B,则该结构单元有 种不同的结构类型。
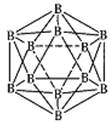
(4)金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,计算确定其晶胞的类型(简单、体心或面心立方) ;晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)= pm。
-
(16分)磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式: 。
②n越大,直链聚磷酸铵的水溶性越 (填“大”或“小”)。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。

(3)由工业白磷 (含少量砷、铁、镁等) 制备高纯白磷 ( 熔点44℃,沸点280℃),主要生产流程如下:
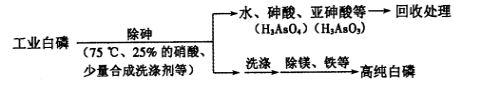
①除砷过程在75 ℃下进行,其合理的原因是 (填字母)。
a.使白磷熔化,提高反应活性
b.降低白磷的毒性
c.温度不宜过高,防止硝酸分解
d.适当提高温度,增大反应速率
②生产过程在高纯氮气保护下进行,其目的是 。
③除砷过程中,合成洗涤剂起到 作用。
④硝酸氧化除砷时被还原为NO,写出砷转化为砷酸的化学方程式: 。
氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越 (填“多”或“少”)。
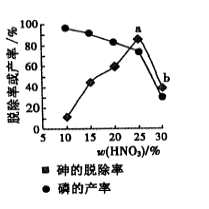
⑤某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是 。
Ti+2MgCl2。可以用作该反应保护气的是_______。