-
(13分)某同学为了验证Fe3+是否能氧化H2SO3生成了SO42–,他用50mL0.1mol/LFeCl3溶液吸收制取SO2气体的尾气,进行以下实验:
(1)检验吸收液中的SO42–:__________
_____________________________________________ ,证明Fe3+能够把H2SO3氧化成SO42–。
(2)请配平并完成上述反应中的化学方程式:
2FeCl3+SO2+________==2FeCl2+H2SO4+2HCl,反应中的还原剂是_____ (写化学式)。
(3)吸收液中除了含有H+、Cl–、SO42–以外,对其它成份(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设。
假设1:溶液中存在Fe3+、Fe2+;
假设2:溶液中存在________;
假设3:溶液中存在Fe2+ 而不存在H2SO3 (二者恰好完全反应)。
②设计方案、进行实验,验证假设。请在表中写出实验步骤以及预期现象和结论(可以不填满)。限选实验试剂和仪器:试管、滴管、0.1moLL-1KMnO4、0.1moLL-1KSCN溶液、品红稀溶液。
实验步骤
预期现象和结论
步骤1:用试管取样品溶液2-3mL,再用滴管取________
若出现血红色,则假设1成立;若未出现血红色,则假设2或假设3成立。
步骤2:________
________
结合步骤1的现象和结论,________
________
________________________________________.
高二化学实验题中等难度题查看答案及解析
-
20mL0.1mol/LFeCl3溶液中含有部分Fe2+,向其中滴加NaOH溶液至PH=4,溶液中有沉淀生成,过滤,得沉淀和滤液。已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16。
下列说法错误的是
A. 沉淀中只有Fe(OH)3 B. 沉淀中有Fe(OH)3和Fe(OH)2
C. 滤液c(Fe3+)=4.0×10-8mol/L D. 向滤液中滴加FeCl2溶液,无沉淀产生
高二化学单选题中等难度题查看答案及解析
-
20mL0.1mol/LFeCl3溶液中含有部分Fe2+,向其中滴加NaOH溶液至PH=4,溶液中有沉淀生成,过滤,得沉淀和滤液。已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16。下列说法错误的是
A.沉淀中只有Fe(OH)3 B.沉淀中有Fe(OH)3和Fe(OH)2
C.滤液c(Fe3+)=4.0×10-8mol/L D.向滤液中滴加FeCl2溶液,无沉淀产生
高二化学选择题困难题查看答案及解析
-
已知:pKa=−lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。常温下,用0.1mol·L−1NaOH溶液滴定20mL0.1mol·L−1 H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH)。下列说法不正确的是( )
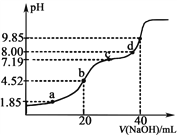
A. a点所得溶液中:2c(H2SO3)+c(SO32-)=0.1 mol·L−1
B. b点所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-)
C. c点所得溶液中:c(Na+)>3c(HSO3-)
D. d点所得溶液中:c(Na+)>c(SO32-)> c(HSO3-)
高二化学单选题困难题查看答案及解析
-
已知:pKa=−lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。常温下,用0.1mol·L−1NaOH溶液滴定20mL0.1mol·L−1 H2SO3溶液的滴定曲线如下图所示(曲线上的数字为pH)。下列说法不正确的是( )
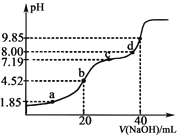
A. a点所得溶液中:2c(H2SO3)+c(SO32-)=0.1 mol·L−1
B. b点所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-)
C. c点所得溶液中:c(Na+)>3c(HSO3-)
D. d点所得溶液中:c(Na+)>c(SO32-)> c(HSO3-)
高二化学单选题困难题查看答案及解析
-
完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳,需消耗50 mL 8 mol/L的氢氧化钠溶液,则燃烧1mol无水乙醇放出的热量不可能是( )
A. 10Q B. 5Q~10Q C. 大于10Q D. 5Q
高二化学单选题中等难度题查看答案及解析
-
完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳,消耗50mL 8mol/L的氢氧化钠溶液,则1mol无水乙醇的燃烧放出的热量不可能是
A.10Q B.5Q C.11Q D.7Q
高二化学选择题简单题查看答案及解析
-
某溶液由K+、Fe3+、SO42-、CO32-、NO3-、I-中的几种离子组成,取样,滴加NaOH溶液后有红褐色沉淀生成。下列有关该溶液的说法不正确的是
A. 是否含有SO42-可用BaCl2溶液检验 B. 是否含有K+可通过焰色反应确定
C. 一定存在的离子为Fe3+、NO3- D. 一定不存在的离子为CO32-、I-
高二化学单选题中等难度题查看答案及解析
-
与100mL0.1mol/L(NH4)2SO4溶液中NH4+离子浓度相同的是( )
A.10mL 1mol/L (NH4)2SO4溶液 B.50mL 0.2mol/L NH4Cl溶液
C.10mL0.05mol/L(NH4)2SO4溶液 D.200mL 0.1mol/L NH4NO3溶液
高二化学单选题简单题查看答案及解析
-
常温下,下列溶液中,有关微粒物质的量浓度关系正确的是
A.0.1mol·L−1 (NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(H+)>c(Fe2+)
B.将100mL0.1mol·L−1 Na2CO3溶液逐滴滴加到100mL0.1mol·L−1盐酸中:c(Na+)>c(Cl−)>c(HCO3-)>c(CO32-)
C.pH=12的NaOH溶液与等体积pH=2的醋酸溶液混合后:c(CH3COO−)>c(Na+)>c(H+)>c(OH−)
D.0.1mol·L−1NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH−)+c(CO32-)
高二化学单选题中等难度题查看答案及解析