-
在压强为0.1 MPa、10L恒容的密闭容器中, 将2 mol CO与 5 mol H2的混合气体在催化剂作用下能生成甲醇:CO(g) + 2H2(g) CH3OH(g) △H<0 请回答下列问题:
CH3OH(g) △H<0 请回答下列问题:
(1)①该反应的熵变ΔS__________0(填“>”、“<”或“=”)。
②若温度T1 >T2,则平衡常数K(T1)___________K(T2)(填“大于”、“小于”或“等于”)
③下列措施既可加快反应速率又可增加甲醇产率的是__________;
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入2 mol CO和5 mol H2
④下列可说明反应已达到化学平衡状态的是________;
A.v生成(CH3OH)=v消耗(CO) B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.CO与H2浓度比不再变化
(2)若温度T2时,5min后反应达到平衡,CO的转化率为75%,则:
①平衡时体系总的物质的量为________mol;
②反应的平衡常数K=______________;
③反应在0-5min区间的平均反应速率v(H2)=____________。
-
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题。
(1)CO可用于合成甲醇。在压强为0.1 MPa条件下,在体积为b L的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
平衡时CO的转化率与温度、压强的关系如下图:
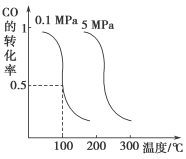
(ⅰ)该反应属于___________反应(填“吸热”或“放热”)。
(ⅱ)100 ℃时,若一个可逆反应的平衡常数K值很大,对此反应的说法正确的是___________(填序号)。
a.该反应使用催化剂意义不大
b.该反应发生将在很短的时间内完成
c.该反应达到平衡时至少有一种反应物百分含量很小
d.该反应一定是放热反应
(ⅲ)在温度和容积不变的情况下,再向平衡体系中充入a mol CO、2a mol H2,达到平衡时CO的转化率___________(填“增大”、“不变”或“减小”,下同),平衡常数___________。
(ⅳ)在某温度下,向一容积不变的密闭容器中充入2.5 mol CO、7.5 mol H2,反应生成CH3OH(g)达到平衡时,CO的转化率为90%,此时容器内压强为开始时压强的___________倍。
(2)某温度下,若将CO2(g)和H2(g)以体积比1∶4混合,在适当压强和催化剂作用下可制得甲烷,已知:
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
则CO2(g)和H2(g)反应生成甲烷和液态水的热化学方程式为____________________。
-
(1)在压强为0.1MPa条件下,将amolCO与3amolH2的混合气体在催化剂作用下能自发反应生成甲醇;CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
① 则该反应的△S________0,△H_________0 (填“<”、“>”或“=”)。
② 若容器容积不变,下列措施可提高CO转化率的是________.
A.升高温度 B.将CH3OH从体系中分离
C.充入He,使体系总压强增大 D.再充入lmolCO和3 molH2
(2)以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4(g)+ H2O(g) CO(g)+3H2(g) △H =+206.0kJ/mol
CO(g)+3H2(g) △H =+206.0kJ/mol
II:CH3OH(g) CO(g)+2H2(g) △H =+129.0kJ/mol CH4(g)和 H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为__________。
CO(g)+2H2(g) △H =+129.0kJ/mol CH4(g)和 H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为__________。
(3)在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g) 2HI(g) △H<0。改变下列条件能加快化学反应速率的是________
2HI(g) △H<0。改变下列条件能加快化学反应速率的是________
(a)保持容器容积不变,向其中加入1molH2。
(b)保持容器容积不变,向其中加入1molN2。(N2不参加反应)。
(c)保持容器内气体压强不变,向其中加入1molN2(N2不参加反应)。
(d)保持容器内气体压强不变,向其中加入1molH2(g)和1molN2(g)。
(e)提高起始的反应温度。
-
某一温度下将1mol N2和4mol H2导入一体积为2L的密闭容器中,测得容器内压强为40Mpa,当20min后,反应达到平衡,测得NH3在混合气体里占25%(体积含量).求:(1)N2的平衡转化率; (2)H2的平均反应速率; (3)平衡时容器内的压强.
-
Ⅰ.CO可用于合成甲醇。在压强为0.1MPa条件下,在体积为bL的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:
CO(g)+2H2(g) CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
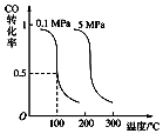
(1)该反应属于 反应(填“吸热”或“放热”)。
(2)100℃时,该反应的平衡常数:K= (用a、b 的代数式表示)。
(3)在温度和容积不变的情况下,再向平衡体系中充入a mol CO,2a mol H2,达到平衡时CO转化率
(填“增大”“不变”或“减小”)
Ⅱ.T ℃时,纯水中c(OH-)为10-6 mol·L-1,则该温度时
(1)将pH=3 的H2SO4溶液与pH=10的NaOH溶液按体积比9:2 混合,所得混合溶液的pH为 。
(2)若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 。
Ⅲ. 在25mL的氢氧化钠溶液中逐滴加入0. 2 mol/ L醋酸溶液,滴定曲线如图所示。
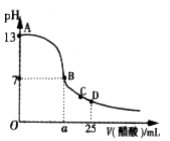
(1)该氢氧化钠溶液浓度为________________。
(2)在B点,a_________12.5 mL(填“<”“>”或“=”)。
(3)在D点,溶液中离子浓度大小关系为_____________________。
-
在某温度下,将H2(g)和I2(g)各0.1mol的气体混合物充入10L的密闭容器中,充分反应,达到平衡时,测得c(H2)=0.0080mol/L,求:
(1)求该反应的平衡常数.
(2)在上述温度下,该容器中若充入的H2(g)和I2(g)各0.2mol,求达到化学平衡时HI(g)的平衡浓度.
-
在10L密闭容器中,1moLA和3moLB在一定条件下反应:
A(g)+xB(g) 2C(g),在2min后反应达到平衡时,测得混合气体共3.4moL,生成0.4moLC, 则下列计算结果不正确的是( )
2C(g),在2min后反应达到平衡时,测得混合气体共3.4moL,生成0.4moLC, 则下列计算结果不正确的是( )
A.平衡时,物质的量之比A︰B︰C=2︰11︰4
B.x值等于4
C.A的转化率为20%
D.平衡时B的平均反应速率为0.04moL/(L·min)
-
在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内压强减小20%。下列说法正确的是( )
A. 该温度下此反应的平衡常数K=400
B. 其他条件不变,再充入0.3mol SO2和0.2mol O2平衡时,SO2的体积分数增大
C. 平衡时,SO2的转化率为95%
D. 前2min SO2的平均反应速率0.02mol/(L·s)
-
在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内压强减小20%。下列说法正确的是
A.该温度下此反应的平衡常数K=400
B.其他条件不变,再充入0.3mol SO2和0.2mol O2平衡时,SO2的体积分数增大
C.平衡时,SO2的转化率为95%
D.前2min SO2的平均反应速率0.02mol/(L·s)
-
在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内压强减小20%。下列说法正确的是( )
A.该温度下此反应的平衡常数K=400
B.其他条件不变,再充入0.3mol SO2和0.2mol O2平衡时,SO2的体积分数增大
C.平衡时,SO2的转化率为95%
D.前2min SO2的平均反应速率0.02mol/(L·s)
CH3OH(g) △H<0 请回答下列问题:


