-
无水氯化亚铁用于制造铁系催化剂、印染的媒染剂和染料还原剂,还可用于冶金、医药、照相等行业。一实验小组模仿工业方法在反应器M中制取氯化亚铁,设计装置如图:
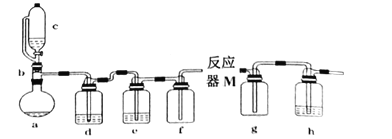
通过查阅相关资料可知:
①在持续高温500℃时,铁与纯净、干燥的Cl2反应可生成FeCl2,在温度较低时可生成FeCl3;
②FeCl3熔沸点低,易升华;
③常见的物质氧化性由大到小顺序:KMnO4(H+)>K2Cr2O7(H+)>MnO2
根据以上信息回答相关的问题:
(1)a、b、c仪器组合成制取氯气的装置,反应无需加热,请写出a容器内所发生反应的化学方程式:___。
(2)e中盛装的药品是浓硫酸,则d中盛装的药品是___。
(3)反应器M为硬质玻璃管,纯净铁粉与干燥纯净的氯气在持续500℃左右反应,其化学反应方程式为__。
(4)实验小组记录的实验现象如下:
| 观察到的部分现象 |
| 第一次实验 | 反应器M中有白雾、红棕色固体,g瓶有白雾和黄绿色气体 |
| 第二次实验 | 反应器M中有绿色晶体,g瓶有红棕色的烟和黄绿色气体 |
| 第三次实验 | 反应器M中有绿色晶体,g瓶有黄绿色气体 |
①第一次实验,反应器M得到红棕色固体可能是__,其原因可能是__。
②第三次实验得到的固体中,最可能含有的微量杂质是___,如果用此固体配制约2~3mol•L-1的染料还原剂溶液,则无需除去含有的杂质,理由是___。
-
无水氯化亚铁用于制造铁系催化剂、印染的媒染剂和染料还原剂,还可用于冶金、医药、照相等行业。一实验小组模仿工业方法制取氯化亚铁,设计装置如下
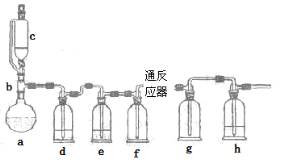
通过查阅相关资料可知:
①在持续高温500℃时,铁与纯净、干燥Cl2反应可生成FeCl2,在温度较低时可生成FeCl3;
②FeCl3熔沸点低,易升华。
根据以上信息回答相关的问题
(1)abc仪器组合成制取氯气的装置,反应无需加热,请写出a容器内所发生的化学反应方程式 。
(2)d、e盛装的药品分别是 和 ,f、g的作用是 。
(3)反应器为硬质玻璃管,纯净铁粉与氯气在500℃左右反应。
①化学反应方程式为
②实验操作顺序是:组装仪器、 、装入药品、 、 、停止加热、关闭c的活塞。
(4)实验小组记录的实验现象如下:
| 观察到的部分现象 |
| 第一次实验 | 反应器中有白雾、红色固体、g瓶有白雾和黄绿色气体 |
| 第二次实验 | 反应器中有绿色晶体,g瓶有红棕色的烟和黄绿色气体 |
| 第三次实验 | 反应器中有绿色晶体,g瓶有黄绿色气体 |
①第一次实验,发现e瓶没有盛装任何药品,所以得到红色固体,其原因是 。
②第二次实验,g瓶有红棕色的烟,其原因是 。
(5)第三次实验得到的固体,最可能含有微量杂质是 ,如果需要配制约2~3mol/L的染料还原剂溶液,则无需除去,理由是 。
-
无水氯化亚铁用于制造铁系催化剂、印染的媒染剂和染料还原剂,还可用于冶金、医药、照相等行业。一实验小组模仿工业方法制取氯化亚铁,设计装置如下
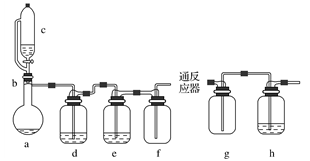
通过查阅相关资料可知:
①在持续高温500℃时,铁与纯净、干燥Cl2反应可生成FeCl2,在温度较低时可生成FeCl3;
②FeCl3熔沸点低,易升华。
根据以上信息回答相关的问题
(1)abc仪器组合成制取氯气的装置,反应无需加热,请写出a容器内所发生的化学反应方程式 。
(2)d、e盛装的药品分别是 和 ,f、g的作用是 。
(3)反应器为硬质玻璃管,纯净铁粉与氯气在500℃左右反应。
①化学反应方程式为
②实验操作顺序是:组装仪器、 、装入药品、 、 、停止加热、关闭c的活塞。
(4)实验小组记录的实验现象如下:
| | 观察到的部分现象 |
| 第一次实验 | 反应器中有白雾、红色固体、g瓶有白雾和黄绿色气体 |
| 第二次实验 | 反应器中有绿色晶体,g瓶有红棕色的烟和黄绿色气体 |
| 第三次实验 | 反应器中有绿色晶体,g瓶有黄绿色气体 |
①第一次实验,发现e瓶没有盛装任何药品,所以得到红色固体,其原因是 。
②第二次实验,g瓶有红棕色的烟,其原因是 。
(5)第三次实验得到的固体,最可能含有微量杂质是 ,如果需要配制约2~3mol/L的染料还原剂溶液,则无需除去,理由是 。
-
氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理。某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性。
某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用)。
查阅资料知:氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2和HCl。
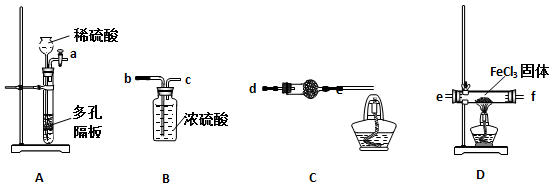
(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法: 。
(2)气流从左至右,装置接口连接顺序是:
a→ ( )→( )→( )→( )→( )
(3)装置C中干燥管中所盛试剂为碱石灰,其作用是: 、
用上述方法制得的氯化亚铁中可能含有氯化铁,某同学设计了如下实验,测定样品中铁元素的质量分数x.请按要求回答下列问题:
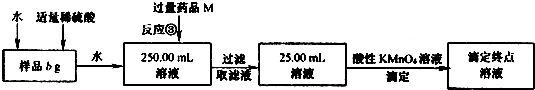
(4)反应③的离子方程式为__ ___.
(5)若3次平行滴定实验,平均消耗c mol/L KMnO4溶液的体积为d mL,则样品中铁元素的质量分数(化简代数式)x=_____________;若样品溶解仍使用盐酸而不改用稀硫酸,则所得样品中铁元素的质量分数将(填“偏大”、“偏小”或“无影响”)____ _________.
-
氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理。某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性。
某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用)。
查阅资料知:氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2和HCl。
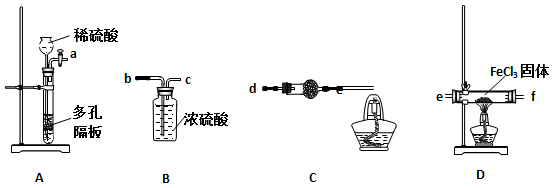
(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法: 。
(2)气流从左至右,装置接口连接顺序是:
A→ ( )→( )→( )→( )→( )
(3)装置C中干燥管中所盛试剂的名称是: ,作用是: 。
(4)装置C中酒精灯的作用是: 。
(5)为了测定氯化亚铁的质量分数,某同学进行了如下实验:
称取实验制备的氯化亚铁样品5.435g,配成溶液,用1.00mol·L-1酸性KMnO4标准溶液滴定至终点。(已知还原性Fe2+>Cl-)滴定结果如下表所示:
| 滴定次数 | 标准溶液的体积 |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 1.04 | 25.03 |
| 2 | 1.98 | 25.99 |
| 3 | 3.20 | 25.24 |
| | |
①写出滴定过程中所发生的2个离子方程式:
、
。
②样品中氯化亚铁的质量分数为 。
-
氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理。某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性。
某同学选择下列装置用氯化铁制备少量氯化亚铁(装置不可以重复使用)。
查阅资料知:氯化铁遇水剧烈水解,在加热条件下氢气还原氯化铁生成FeCl2和HCl。
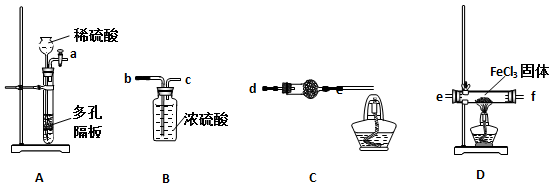
(1)实验开始前应先检查装置的气密性,请叙述装置A气密性检验的方法: 。
(2)气流从左至右,装置接口连接顺序是:
A→ ( )→( )→( )→( )→( )
(3)装置C中干燥管中所盛试剂的名称是: ,作用是: 。
(4)装置C中酒精灯的作用是: 。
(5)为了测定氯化亚铁的质量分数,某同学进行了如下实验:
称取实验制备的氯化亚铁样品5.435g,配成溶液,用1.00mol·L-1酸性KMnO4标准溶液滴定至终点。(已知还原性Fe2+>Cl-)滴定结果如下表所示:
| 滴定次数 | 标准溶液的体积 |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 1.04 | 25.03 |
| 2 | 1.98 | 25.99 |
| 3 | 3.20 | 25.24 |
| | |
①写出滴定过程中所发生的2个离子方程式:
、
。
②样品中氯化亚铁的质量分数为 。
-
硫酰氯(SO2C12)常用于制造医药品、染料等。通常情况下其熔点为-54.1℃,沸点69.2℃,遇水发生剧烈反应生成氯化氢气体。某实验小组拟用干燥的氯气和二氧化硫在活性炭催化下制取硫酰氯,其实验装置如下:
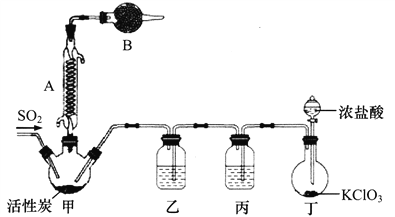
(1)B中的试剂为___________,作用为______________________________。
(2)在不改变装置的前提下,丁中的KClO3可用_____________代替(填化学式)。
(3)该小组向Cu(NO3)2·3H2O晶体中滴加SO2C12制备少量无水Cu(NO3)2。
①请写出SO2C12与水反应的化学方程式__________________________________。
②滴加SO2C12的作用除了吸水之外,还有_____________________________。
(4)测定无水Cu(NO3)2的纯度,可用分光光度法。现测得[Cu(NH3)4]2+的吸光度A与Cu2+标准浓度关系如图所示(已知4NH3·H2O+Cu2+==[Cu(NH3)4]2++4H2O)。
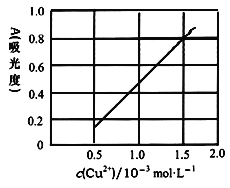
称取0.3150g制得的无水Cu(NO3)2样品,用蒸馏水溶解并配制成100mL溶液,用__________(填仪器名称)准确量取10.00mL,加过量氨水,再用蒸馏水稀释至100mL,测得其吸光度A=0.8。则此无水Cu(NO3)2样品的纯度是___________(保留三位有效数字)。
-
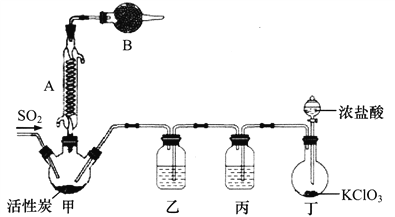
硫酰氯(SO2C12)常用于制造医药品、染料等。通常情况下其熔点为-54.1℃,沸点69.2℃,遇水发生剧烈反应生成氯化氢气体。某实验小组拟用干燥的氯气和二氧化硫在活性炭催化下制取硫酰氯,其实验装置如下:
(1)有关冷凝管的使用原理,下列说法正确的是(填字母)______________。
a.蒸气冷凝在内管的外壁上
b.当蒸馏液体的沸点超过140℃,水冷易炸裂仪器,此时多采用空气冷凝管
c.蛇形冷凝管多用于有机制备的回流,适用于沸点较低的液体
d.内外管所围出的空间为行水区,有吸收蒸气热量并将热量移走的功用
(2)B中的试剂为___________,作用为______________________________。
(3)在不改变装置的前提下,丁中的KClO3可用_____________代替(填化学式)。
(4)该小组向Cu(NO3)2·3H2O晶体中滴加SO2C12制备少量无水Cu(NO3)2。
①请写出SO2C12与水反应的化学方程式__________________________________。
②滴加SO2C12的作用除了吸水之外,还有_____________________________。
(5)测定无水Cu(NO3)2的纯度,可用分光光度法。现测得[Cu(NH3)4]2+的吸光度A与Cu2+标准浓度关系如图所示(已知4NH3·H2O+Cu2+==[Cu(NH3)4]2++4H2O)。
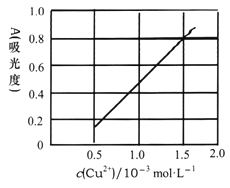
称取0.3150g制得的无水Cu(NO3)2样品,用蒸馏水溶解并配制成100mL溶液,用__________(填仪器名称)准确量取10.00mL,加过量氨水,再用蒸馏水稀释至100mL,测得其吸光度A=0.8。则此无水Cu(NO3)2样品的纯度是___________(保留三位有效数字)。
-
KClO3是一种常见的氧化剂,常用于医药工业、印染工业和制造烟火。实验室用KClO3和MnO2混合加热制氧气,现取KClO3和MnO2的混合物16.60g加热至恒重,将反应后的固体加15g水充分溶解,剩余固体6.55g(25℃),再加5g水充分溶解,仍剩余固体4.80g(25℃)。
(1)若剩余的4.80g固体全是MnO2,则原混合物中KClO3的质量为___g;
(2)若剩余的4.80g固体是MnO2和KCl的混合物
①求25℃时KCl的溶解度___;
②求原混合物中KClO3的质量___;
③所得KCl溶液的密度为1.72g/cm3,则溶液的物质的量浓度为多少___?(保留2位小数)
(3)工业常利用3Cl2+6KOH(热)→KClO3+5KCl+3H2O,制取KClO3(混有KClO)。实验室模拟KClO3制备,在热的KOH溶液中通入一定量氯气充分反应后,测定溶液中n(K+):n(Cl-)=14:11,将所得溶液低温蒸干,那么在得到的固体中KClO3的质量分数的取值范围为多少?___
-
氯化亚铜(CuCl)广泛用于有机合成、气体吸收、冶金、医药化工等行业。
(1).工业上氯化亚铜可由下列反应制备:
2CuSO4+ Na2SO3 + 2NaCl + Na2CO3 2CuCl ↓+ 3Na2SO4 + CO2↑。制备过程中需要20% 的CuSO4溶液,配制100g 该CuSO4溶液需要胆矾 g,需要水 g。
(2).实验室可用如下方法制备少量CuCl:取10mL 0.2mol/L CuCl2溶液,加入0.128g铜屑和36.5%的浓盐酸(密度为1.2g/mL)3mL,在密闭容器中加热,充分反应后,得到无色溶液A;将溶液A全部倾入水中,可得到白色的氯化亚铜沉淀。
已知溶液A中只含氢离子和两种阴离子(不考虑水的电离),其中,n(H+)=0.036mol、n(Cl–)=0.032mol。请通过分析和计算,确定溶液A中另一阴离子的化学式和物质的量。
(3).由CO2、O2、CO、N2组成的混合气体1.008L,测得其密度为1.429g/L,将该气体依次通过足量的30%KOH溶液、氯化亚铜氨溶液(可完全吸收O2和CO) (假定每一步反应都能进行完全),使上述液体分别增加0.44g、0.44g(体积和密度均在标准状况下测定)。
①该混合气体的摩尔质量是 g/mol;混合气体中n(CO2): n(CO和N2) = 。
列式计算:
②混合气体中CO的质量是多少?
③最后剩余气体的体积是多少?










