单质硫在KOH的热溶液中发生岐化反应:3 S + 6 KOH2 K2S + K2SO3 + 3 H2O
若硫过量,进一步生成K2Sx(x ≤ 5)和K2S2O3。将0.08 mol单质硫与含0.06 mol KOH的热溶液充分反应恰好生成a mol K2Sx和b mol K2S2O3,再加入足量KClO-KOH的混合溶液,硫元素全部转化为K2SO4,转移电子n mol。则以下正确的是
A.a = 2b B.x = 2 C.n = 0.48 D.b = 0.02
高三化学选择题中等难度题
单质硫在KOH的热溶液中发生岐化反应:3 S + 6 KOH2 K2S + K2SO3 + 3 H2O
若硫过量,进一步生成K2Sx(x ≤ 5)和K2S2O3。将0.08 mol单质硫与含0.06 mol KOH的热溶液充分反应恰好生成a mol K2Sx和b mol K2S2O3,再加入足量KClO-KOH的混合溶液,硫元素全部转化为K2SO4,转移电子n mol。则以下正确的是
A.a = 2b B.x = 2 C.n = 0.48 D.b = 0.02
高三化学选择题中等难度题
单质硫在KOH的热溶液中发生岐化反应:3 S + 6 KOH2 K2S + K2SO3 + 3 H2O
若硫过量,进一步生成K2Sx(x ≤ 5)和K2S2O3。将0.08 mol单质硫与含0.06 mol KOH的热溶液充分反应恰好生成a mol K2Sx和b mol K2S2O3,再加入足量KClO-KOH的混合溶液,硫元素全部转化为K2SO4,转移电子n mol。则以下正确的是
A.a = 2b B.x = 2 C.n = 0.48 D.b = 0.02
高三化学选择题中等难度题查看答案及解析
单质硫在NaOH的热溶液中发生歧化反应:3S+6NaOH→2Na2S+Na2SO3+3H2O,若硫过量,进一步生成Na2Sx(x≤5)和Na2S2O3,将2.56g硫与含0.06molNaOH的热溶液充分反应恰好生成amolNa2S3和bmolNa2S2O3,再加入足量NaClO―NaOH的混合溶液,硫元素全部转化为Na2SO4,转移电子nmol,则以下正确的是( )
A.a=2b B.2a=b C.n=0.48 D.b=0.02
高三化学多选题中等难度题查看答案及解析
(8分)已知:①MnO4— +e-MnO42― (绿色)(强碱性条件)
②MnO4—+ 8H+ + 5e-Mn2+ (无色)+ 4H2O(强酸性条件)
(1)在KOH溶液中,KMnO4与K2SO3溶液发生反应, 写出反应的离子方程式________。
(2)将KMnO4溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式________.
(3)用酸性KMnO4溶液与亚铁盐的反应证明Fe2+具有还原性,MnO4‑ 具有氧化性,最合适的亚铁盐是________(选填编号),可用来酸化KMnO4溶液的试剂是________(选填编号)
a. FeCl2 b. FeSO4 c.Fe(NO3)2 d稀硫酸 e. 盐酸 f. 硝酸
(4)向20 mL浓度为0.05mol/L的KMnO4溶液中滴加FeSO4溶液,使MnO4‑ 全部转化为Mn2+ ,则反应前需向KMnO4溶液加入c(H+)=1mol/L的酸不少于________mL
高三化学填空题简单题查看答案及解析
向等物质的量浓度的K2S、KOH混合溶液中滴加稀盐酸至过量。其中主要含硫各物种(H2S、HS−、S2−)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出)。下列说法不正确的是
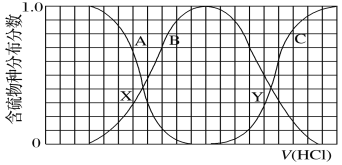
A.A曲线表示S2-随盐酸加入量增加时的分布分数改变情况
B.X、Y为曲线两交叉点。若已知Y点处的pH,则可计算Ka1(H2S)
C.X、Y点对应溶液中水的电离程度大小关系为:X<Y
D.Y点对应溶液中c(K+)与含硫各微粒浓度的大小关系为:c(K+)=3[c(H2S)+c(HS−)+c(S2−)]
高三化学单选题中等难度题查看答案及解析
在反应S+KOH→K2SO3+K2S2+H2O(未配平)中,被氧化与被还原的硫原子个数比为
A. 1∶4 B. 4∶1 C. 1∶2 D. 2∶1
高三化学单选题简单题查看答案及解析
已知P单质在KOH溶液中的变化是:4P+3KOH+3H2O=3KH2PO2+PH3↑,下列说法正确的是
A.产物PH3分子中所有的原子可能共平面
B.该反应中P做还原剂,H2O做氧化剂
C.相关元素的第一电离能的大小顺序:S>P>Si
D.该反应每发生0.3摩尔电子转移,PH3分子中就有0.3摩尔P-H键形成
高三化学选择题中等难度题查看答案及解析
已知P单质在KOH溶液中的变化是:4P+3KOH+3H2O=3KH2PO2+PH3↑,下列说法正确的是
A.产物PH3分子中所有的原子可能共平面
B.该反应中P做还原剂,H2O做氧化剂
C.相关元素的第一电离能的大小顺序:S>P>Si
D.该反应每发生0.3摩尔电子转移,PH3分子中就有0.3摩尔P-H键形成
高三化学单选题中等难度题查看答案及解析
能正确表示下列反应的离子方程式为
A. NH4HCO3溶于过量的浓KOH溶液中:NH4++ HCO3-+2OH-= CO32-+ NH3·H2O+2 H2O
B. 醋酸除去水垢:2H++CaCO3=Ca2++ CO2↑+ H2O
C. 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+===SO2↑+H2O
D. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:Al3++2SO42-+2Ba2++4OH -= AlO2-+2BaSO4↓+2H2O
高三化学单选题中等难度题查看答案及解析
下列方程式书写正确的是
A.溴乙烷发生消去反应:
B.向溶液中加入过量氨水:
C.向溶液中加入过量
溶液:
D.向含和KOH均为0.1 mol的混合溶液中通人标准状况下4.48 L
气体:
高三化学单选题简单题查看答案及解析
下列表示溶液中所发生反应的离子方程式正确的是 ( )
A.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH- NH3↑+ H2O
B.Ca(HCO3)2溶液中加入少量NaOH溶液:
Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O
C.KI溶液与H2SO4酸化的H2O2溶液混合:
2I-+ H2O2 + 2H+ =2H2O + I2
D.向氯化银悬浊液中加入饱和碘化钾溶液:Ag+ +I-=AgI ↓
高三化学选择题中等难度题查看答案及解析