-
(8分)写出下列元素原子的电子排布式
P________,Cr________,
Al________, Cu________,
高二化学选择题简单题查看答案及解析
-
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)①上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Cu原子的核外电子排布式:______。
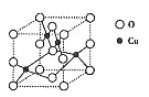
②铜的一种氧化物晶胞中(结构如图所示),所包含的Cu原子数目为______。
③其中O原子的配位数为______。
(2)根据等电子原理,写出CO分子的结构式______。
(3)甲醇催化氧化可得到甲醛(HCHO),甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇沸点比甲醛高得多的原因是______。
②甲醇分子中原子轨道的杂化类型为sp3的原子个数为______。
③甲醛分子的空间构型是______;1mol甲醛分子中σ键的数目为______。
④甲醇中C、H、O三种元素电负性由大到小的顺序为______。
⑤Cu2O的熔点比Cu2S高的原因是______。
高二化学综合题中等难度题查看答案及解析
-
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式:________。
(2)根据等电子原理,写出CO分子的结构式__________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醛分子中碳原子轨道的杂化类型为_______________。
②甲醛分子的空间构型是___________;1 mol甲醛分子中σ键的数目为______________。
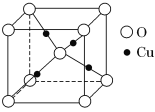
③在1个Cu2O晶胞(结构如图所示)中,所包含的Cu原子数目为______________。
高二化学综合题中等难度题查看答案及解析
-
Ⅰ.请按下列要求写出相应粒子的电子排布式,并回答有关问题:
⑴写出基态原子或离子的电子排布式:
①Fe3+_________________; ②Cr _______________; ③Cu _______________.
⑵比较 Fe2+与Fe3+的化学稳定性:Fe2+________Fe3+,半径大小:Fe2+________Fe3+
Ⅱ⑴在第三周期中,第一电离能最小的元素是________,电负性最大的元素是________(用元素符号表示)。
⑵第二、三、周期原子中p轨道半充满的元素是_______________(用元素符号表示)。
⑶第二周期原子中,未成对电子数等于周期系数的原子有________(用元素符号表示)
Ⅲ. (2010·滁州模拟)ClO、ClO、ClO中Cl都是以sp3杂化轨道与O原子成键的,试推测下列微粒的立体结构。
微粒
ClO
ClO
ClO
立体结构
高二化学填空题中等难度题查看答案及解析
-
生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式______________。
(2)根据等电子原理,写出CO分子的结构式________________________ ________________________________________________________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是______________________;甲醛分子中碳原子轨道的杂化类型为________。
②甲醛分子的空间构型是____________;1 mol甲醛分子中σ键的数目为________。
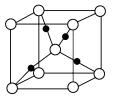
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为________。
高二化学填空题困难题查看答案及解析
-
(6分) 写出下列原子或离子的电子排布式或价电子排布:
(1)电子排布式
Al3+________ 24Cr________ 30Zn________
(2)价电子排布
K________ O________ 28Ni
高二化学填空题中等难度题查看答案及解析
-
按要求填空。
(1)下列微粒基态的电子排布中未成对电子数最多的是________(填字母)。
A.N3- B.Fe3+ C.Cu D.Cr E.C
(2)与铜同周期的所有元素的基态原子中,未成对电子数与铜原子相同的元素有________种。
(3)基态铬原子的价电子排布式是_____,这样排布使整个体系能量降低,原因是________。
(4)基态砷原子的价电子排布式为_______,其原子核外有________个能层,________个能级,其原子轨道达到全充满状态的个数是________,与其同周期元素基态原子未成对电子数相同的元素还有________种。
(5)短周期元素中,原子基态时具有1个未成对电子的元素共有________种。
(6)某元素基态原子的最外层电子排布式为nsnnpn+1,则电子排布式中n=________,该元素基态原子中能量最高的能级是_____,其电子云在空间中有______方向,呈现_____形。
高二化学综合题中等难度题查看答案及解析
-
(13分)过渡元素具有较多的空轨道,所以第四周期的Cr、Fe、Co、Ni、Cu、Zn等多种金属能形成配合物。
(1)铬元素的基态原子的外围电子排布式是 。
(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:
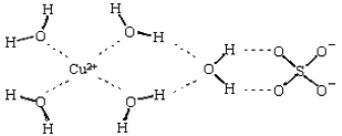
图中虚线表示的作用力为 ______________________;
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4·H2O晶体。在Cu(NH3)4SO4·H2O晶体中,[Cu(NH3)4]2+为平面正方形结构,则呈正四面体结构的原子团是 __,其中心原子的杂化轨道类型是 ___;
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。试推测四羰基镍的晶体类型是 ___,Ni(CO)4易溶于下列 __(用序号作答)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
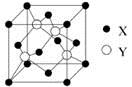
(5)元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子最外层电子数是其内层的3倍。X与Y所形成化合物晶体的晶胞如图所示,该化合物的化学式为 ____。
高二化学填空题困难题查看答案及解析
-
(9分)请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有________种。
(2)请写出Cr元素的核外电子排布式________。
(3)某元素的正三价离子的3d能级为半充满,该元素的元素名称为________,其单质在一定条件下能与S反应,试写出该反应的化学方程式________ 。
(4)某元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的电子排布图为 。
高二化学填空题中等难度题查看答案及解析
-
下列各选项所述的两个量,前者一定大于后者的是 ( )
①Al原子和N原子的未成对电子数;②Ag+、Cu2+与NH3形成配合物时的配位数;③Al的金属性和Mg的金属性;④F元素和O元素的电负性;⑤N和O元素的第一电离能;⑥H 原子和H+离子的半径
A.①④⑤ B.②④⑥ C.④⑤⑥ D.③⑤⑥
高二化学选择题简单题查看答案及解析