-
(5分)某温度下1L密闭容器中加入1molN2和3molH2,使反应N2+3H2  2NH3达平衡,测得混合气体中N2、H2、NH3的量分别为m、n、gmol,如温度不变,只改变初始物质的加入量,而要求m、n、g总保持不变。若N2、H2、NH3的起始加入量用x、y、z表示时,应满足条件:
2NH3达平衡,测得混合气体中N2、H2、NH3的量分别为m、n、gmol,如温度不变,只改变初始物质的加入量,而要求m、n、g总保持不变。若N2、H2、NH3的起始加入量用x、y、z表示时,应满足条件:
(1)若x=0,y=0时z= ____________mol,
(2)若x=0.25mol,则y= ____________mol,z= ____________mol,
(3)x、y、z应满足的一般条件是(用含x、y、z的代数式表示)________。
-
在恒温、容积为2L 的密闭容器中通入1molN2和xmolH2 发生如下反应:N2(g)+3H2(g)  2NH3(g) 。经过5min 达到平衡时,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%。试回答(请书写必要的计算步骤) :
2NH3(g) 。经过5min 达到平衡时,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%。试回答(请书写必要的计算步骤) :
(1)起始时充入H2的物质的量_________;
(2)平衡时N2的浓度_______;
(3)5min 内用NH3表示的化学反应速率__________。
-
将1molN2气体和3molH2气体在2L的恒容容器中,并在一定条件下发生如下反应:N2(g)+3H2(g)  2NH3(g),若经2s后测得NH3的浓度为0.6mol·L-1,现有下列几种说法:其中不正确的是
2NH3(g),若经2s后测得NH3的浓度为0.6mol·L-1,现有下列几种说法:其中不正确的是
A. 用N2表示的反应速率为0.15mol·L-1·s-1 B. 2s时H2的转化率为40%
C. 2s时N2与H2的转化率相等 D. 2s时H2的浓度为0.6mol·L-1
-
一定条件下,在体积一定的密闭容器中加入1molN2和3molH2发生反应:N2 +3H2 2NH3(正反应是放热反应)。下列有关说法正确的是
2NH3(正反应是放热反应)。下列有关说法正确的是
A.达到化学反应限度时,生成2mol NH3
B.向容器中再加入N2,可以加快反应速率
C.降低温度可以加快反应速率
D.1mol N2 和3mol H2的总能量低于2mol NH3的总能量
-
一定条件下,a L密闭容器中放入1molN2和3molH2发生N2+3H22NH3的反应,下列选项中能说明反应已达到平衡状态的是
A.c(N2)∶c(H2)∶c(NH3)=1∶3∶2
B.2v(H2)=3v(NH3)
C.单位时间内1个N≡N键断裂的同时,有6个N-H键断裂
D.单位时间消耗0.1molN2的同时,生成0.2molNH3
-
一定温度下,在1L密闭容器中,反应N2 + 3H2  2NH3达到化学平衡状态的标志是( )
2NH3达到化学平衡状态的标志是( )
A.N2∶ H2∶NH3 =1∶3∶2
B.N2、H2、NH3的物质的量不再改变
C.混合气体的密度保持不变
D.单位时间里每增加1mol N2,同时增加3mol H2
-
一定温度下,在1L的密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g),达到平衡的标志是
2NH3(g),达到平衡的标志是
A.NH3的生成速率与H2的生成速率相等 B.混合气体的密度不再发生变化
C.N2、H2、NH3的分子数之比为1∶3∶2 D.N2的转化率不再发生改变
-
一定温度下,在1L的密闭容器中发生可逆反应:N2(g)+3H2(g)⇌2NH3(g)达到平衡的标志是( )
A.NH3的生成速率与H2的生成速率相等
B.混合气体的密度不再发生变化
C.N2、H2、NH3的分子数之比为1:3:2
D.N2的转化率不再发生改变
-
工业合成氨反应的化学方程式为:N2(g)+3H2(g)  2NH3(g) △=-92.3kJ/mol。一定温度下,向体积为2L的密闭容器中加入1mol N2和3mol H2,经2min后达到平衡,平衡时测得NH3的浓度为0.5 mol/L。
2NH3(g) △=-92.3kJ/mol。一定温度下,向体积为2L的密闭容器中加入1mol N2和3mol H2,经2min后达到平衡,平衡时测得NH3的浓度为0.5 mol/L。
(1)2min 内H2的反应速率v(H2)= ;
(2)充分反应并达到平衡时,放出的热量 92.3kJ(填“大于”、“小于”或“等于”)。
原因是 。
(3)下列说法可证明反应达到平衡状态的 。
A.单位时间内,断开1mol N≡N,同时断开3mol H—H
B.单位时间内,形成1mol N≡N,同时形成3mol N—H
C.单位时间内,断开1mol N≡N,同时断开6mol N—H
D.单位时间内,形成1mol N≡N,同时断开3mol H—H
(4)氨的一个重要用途是用于制备火箭发射原料N2H4(肼),已知:火箭发射的原理是N2H4(肼)在NO2中燃烧,生成N2、水蒸气。根据如下反应:
N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534.0kJ/mol
写出在相同状态下,发射火箭反应的热化学方程式 。
-
I.在恒温、体积为1.0L的密闭容器中通入1.0 mol N2和x mol H2发生如下反应N2(g)+3H2(g) 2NH3(g),20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:
2NH3(g),20 min后达到平衡,测得反应放出的热量为18.4 kJ,混合气体的物质的量为1.6 mol,容器内的压强变为原来的80%。请回答下列问题:
(1)20 min内,V(N2)=______。
(2)该反应的热化学方程式为____________。
(3)下列叙述中能表示该反应达到平衡状态的是_______(填序号)。
①N2体积分数保持不变
②单位时间断裂03tmol H- H键,同时生成0.6 molN-H键
③混合气体的密度不再改变
④2v正(H2)=3v逆(NH3)
⑤混合气体的平均摩尔质量不再改变
II.1883年,瑞典化学家阿伦尼乌斯创立了电离学说,在水溶液范围内对酸、碱作出了严密的概括。请回答下列有关水溶液的问题:
(4)①用电离方程式表示氨水溶液是碱性的原因________;
②用离子方程式表示碳酸钠溶液显碱性的原因__________。
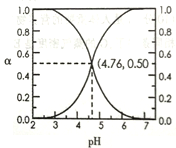
(5)25℃时,在含HA和A-的溶液中,HA和A-两者中各自所占的物质的量分数(a)随溶液pH变化的关系如下图所示。请比较下列大小关系(填编号)
①在pH<4.76的溶液中,c(A-)____(HA);
②在pH>4.76的溶波中,c(A-)+(OH-)_____c(H+)。
A.大于 B.小于 C.等于 D.可能大于,也可能等于 E.可能小于,也可能等于
2NH3达平衡,测得混合气体中N2、H2、NH3的量分别为m、n、gmol,如温度不变,只改变初始物质的加入量,而要求m、n、g总保持不变。若N2、H2、NH3的起始加入量用x、y、z表示时,应满足条件:
