-
元素周期表是化学学习的重要工具。根据所学知识完成下列问题。
(1)元素周期表中,第三周期原子半径最大的金属元素是___________(填写元素符号),元素的最高价氧化物对应的水化物中酸性最强是___________(填写化学式)。
(2)在下列变化中,化学键没有破坏的是____________(填写序号,下同),仅发生离子键破坏的是___________,仅发生共价键破坏的是_________,既发生共价键破坏又发生离子键破坏的是_________。
①I2的升华 ②烧碱熔化 ③NaCl溶于水 ④HC1溶于水 ⑤O2溶于水 ⑥Na2O2溶于水
高一化学填空题中等难度题查看答案及解析
-
元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,请参照元素 ①~⑩在表中的位置回答下列问题.

(1)在这 10 种元素中,原子半径最大的是_________(填元素符号)。
(2)⑧、⑨的最高价氧化物对应水化物的酸性强弱顺序是______>_____(填化学式)。
(3)写出①、④元素组成比为1:1的化合物的电子式是_________。
(4)④⑤⑥⑦对应的离子半径最小的是_________(填离子符号)。
(5)写出实验室制取③的气态氢化物的化学方程式_________。
(6)⑦单质可用来制造⑦—空气燃料电池,该电池通常以氯化钠或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。若以氯化钠为电解质溶液时,正极的反应式为_________。若以氢氧化钾溶液为电解质溶液时,电池的总反应式为_____________________________。
高一化学综合题中等难度题查看答案及解析
-
元素周期表是学习物质结构和性质的重要工具,如图是元素周期表的一部分,请参照元素①~⑩在表中的位置回答下列问题.
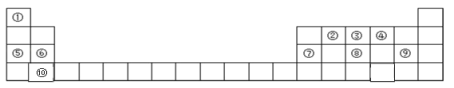
(1)在这 10 种元素中,原子半径最大的是_________(填元素符号)。
(2)⑧、⑨的最高价氧化物对应水化物的酸性强弱顺序是______>_____(填化学式)。
(3)写出①、⑩元素组成比为2:1的化合物的电子式是_________。
(4)④⑤⑥⑦对应的离子半径最小的是_________(填离子符号)。
(5)写出实验室制取③的气态氢化物的化学方程式_________。
(6)⑦单质—空气燃料电池,以氢氧化钾溶液为电解质溶液,正极的反应式为_________
高一化学综合题中等难度题查看答案及解析
-
(12分)元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是 。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水合物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为 ,氧化性最弱的简单阳离子是 。
(3)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:

写出SiCl4的电子式: ;在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收akJ热量,则生成1mol纯硅吸收的热量为
(4)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式: 。
高一化学填空题极难题查看答案及解析
-
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为 ,氧化性最弱的简单阳离子是 。
(3)已知:
化合物
MgO
Al2O3
MgCl2
AlCl3
类型
离子化合物
离子化合物
离子化合物
共价化合物
熔点/℃
2800
2050
714
191
工业制镁时,电解MgCl2而不电解MgO的原因是 ;
制铝时,电解Al2O3而不电解AlCl3的原因是 。
(4)晶体硅(熔点1410 ℃)是良好的半导体材料。由粗硅制纯硅过程如下:
写出SiCl4的电子式: ;在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
(7)工业上,通过如下转化可制得KClO3晶体:
完成Ⅰ中反应的总化学方程式:
Ⅱ该反应过程能析出KClO3晶体而无其他晶体析出的原因是 。
高一化学简答题极难题查看答案及解析
-
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是______。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.单质的熔点降低
d.氧化物对应的水化物碱性减弱,酸性增强
原子最外层电子数与次外层电子数相同的元素名称为_____,氧化性最弱的简单阳离子是____。
(2)已知:
化合物
MgO
Al2O3
MgCl2
AlCl3
类型
离子化合物
离子化合物
离子化合物
共价化合物
熔点/℃
2800
2050
714
191
工业制镁时,电解MgCl2而不电解MgO的原因是_____;制铝时,电解Al2O3而不电解AlCl3的原因是_____。
(3)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗)
SiCl4
SiCl4(纯)
Si(纯)
写出SiCl4的电子式:_____;
(4)下列气体不能用浓硫酸干燥,可用P2O5干燥的是_____。
a.NH3 b.HI c.SO2 d.CO2
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:____。
高一化学综合题中等难度题查看答案及解析
-
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为________,氧化性最弱的简单阳离子是________。
(3)已知:
化合物
MgO
Al2O3
MgCl2
AlCl3
类型
离子化合物
离子化合物
离子化合物
共价化合物
熔点/℃
2800
2050
714
191
工业制镁时,电解MgCl2而不电解MgO的原因是_______________________________ ___;
制铝时,电解Al2O3而不电解AlCl3的原因是____________________________ __。
(4)晶体硅(熔点1410 ℃)是良好的半导体材料,SiCl4(熔点-70 ℃)。由粗硅制纯硅过程如下:
SiCl4属于 晶体。在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:______________________________________ 。
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是________。
a.NH3b.HI c.SO2d.CO2
高一化学填空题简单题查看答案及解析
-
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是____________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为_________,氧化性最弱的简单阳离子是_______。
(3)晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗)
SiCl4
SiCl4(纯)
Si(纯)。写出SiCl4的结构式_________________。
(4)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是__________。
a.NH3 b.HI c.SO2 d.CO2
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1︰1。写出该反应的化学方程式_____________________。
高一化学填空题困难题查看答案及解析
-
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是_______。
a.单质的熔点降低
b.原子半径和简单离子半径均减小
c.元素的金属性减弱,非金属性增强
d.氧化物对应的水化物碱性减弱,酸性增强
(2)氧化性最弱的简单阳离子是_______;热稳定性:H2O____H2S(填>、<、=)。
(3)写出SiCl4的电子式:________。
(4)已知化合物M由第三周期的两种相邻元素按原子个数比1:1组成,不稳定,遇水反应生成谈黄色沉淀A和两种无色有刺意性气味气体B、C,相应物质的转化关系如图:
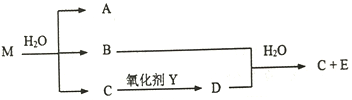
①已知M的摩尔质量为135g/mol,写出M的化学式_____。
②任选一种合适的氧化剂Y,写出C的浓溶液与Y反应生成D的离子反应方程式_______。
③M中的一种元素可形成化合物KXO3,可用于实验室制O2。若不加催化剂,400 ℃时KXO3分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:____________。
高一化学综合题中等难度题查看答案及解析
-
元素周期表是学习化学的重要工具,它隐含着许多信息和规律。根据下表中短周期元素的原子半径和主要化合价,回答表后的问题。
①
②
③
④
⑤
⑥
⑦
⑧
原子半径(10-10m)
0.74
1.60
0.53
1.10
0.99
1.11
0.75
1.43
最高或最低化合价
+2
+1
+5
+7
+2
+5
+3
-2
-3
-1
-3
(1)上述元素中与元素⑧处于同一周期的有______________________(填元素符号)
(2)元素①在元素周期表中的位置是_______________________
(3)①④⑦三种元素的氢化物的稳定性由强到弱的顺序为__________________(填化学式)
(4) 请写出下列元素形成的常见化合物的电子式:
③⑤_____________ ②⑤_____________ ③⑦_____________
(5) 请写出⑤⑧两种元素的最高价氧化物对应水化物间反应的离子方程式:_________________________。
高一化学简答题困难题查看答案及解析