如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl—NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜。
下列说法中正确的是
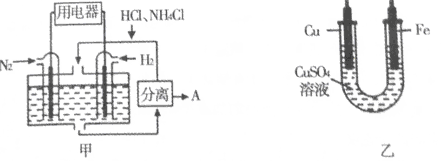
A. 通入H2—极与图乙中的铜电极相连
B. 电池工作一段时间后,溶液pH减少
C. 当消耗0.025molN2时,则铁电极增重1.6g
D. 通入N2―端的电极反应式为:N2+ 8H++ 6e-=2NH4+
高三化学选择题困难题
如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl—NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜。
下列说法中正确的是

A. 通入H2—极与图乙中的铜电极相连
B. 电池工作一段时间后,溶液pH减少
C. 当消耗0.025molN2时,则铁电极增重1.6g
D. 通入N2―端的电极反应式为:N2+ 8H++ 6e-=2NH4+
高三化学选择题困难题
如图甲是一种既能提供电能,又能实现氮固定的新型燃料电池(采用新型电极材料,N2、H2为电极反应物,HCl—NH4Cl为电解质溶液);图乙是利用甲装置产生的电能在铁上镀铜。
下列说法中正确的是

A. 通入H2—极与图乙中的铜电极相连
B. 电池工作一段时间后,溶液pH减少
C. 当消耗0.025molN2时,则铁电极增重1.6g
D. 通入N2―端的电极反应式为:N2+ 8H++ 6e-=2NH4+
高三化学选择题困难题查看答案及解析
使用新型电极材料,以N2、H2为电极反应物,以HC1-NH4C1为电解质溶液,可制造出一种既能提供电能,又能实现氮固定的新型燃料电池,原理如下图所示。下列有关分析正确的是( )

A. 通入H2—极为正极 B. 分离出的物质X为HC1
C. 电池工作一段时间后,溶液pH减小 D. 通入N2一极的电极反应式为:N2+6e-+8H+=2NH4+
高三化学单选题中等难度题查看答案及解析
使用新型电极材料,以N2、H2为电极反应物,以HC1-NH4C1为电解质溶液,可制造出一种既能提供电能,又能实现氮固定的新型燃料电池,原理如下图所示。下列有关分析正确的是( )

A. 通入H2—极为正极 B. 分离出的物质X为HC1
C. 电池工作一段时间后,溶液pH减小 D. 通入N2一极的电极反应式为:N2+6e-+8H+=2NH4+
高三化学选择题中等难度题查看答案及解析
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。下列说法不正确的是
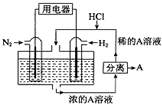
A.通入N2的电极发生的电极反应式为:N2+6e-+8H+=2NH4+
B.反应过程中溶液的pH会变大,故需要加入盐酸
C.该电池外电路电流从通入H2的电极流向通入N2的电极
D.通入H2的电极为负极,A为NH4Cl
高三化学选择题中等难度题查看答案及解析
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。下列说法不正确的是( )

A.通入N2的电极发生的电极反应式为:N2+6e-+8H+=2NH4+
B.反应过程中溶液的pH会变大,故需要加入盐酸
C.该电池外电路电流从通入H2的电极流向通入N2的电极
D.通入H2的电极为负极,A为NH4Cl
高三化学选择题困难题查看答案及解析
一种既能提供电能又能固氮的新型氢氮燃料电池的工作原理如图所示,其中电解质溶液为溶有化合物A的稀盐酸。下列有关表述错误的是( )

A. 通入N2的电极发生的电极反应式为N2+6e-+8H+=2NH4+
B. 该装置能将化学能转化为电能,化合物A 为NH4Cl
C. 电子从通入N2的电极流出,经过用电器流向通入H2的电极
D. 反应过程中电解质溶液的pH会变大,故需要通入氯化氢气体
高三化学单选题中等难度题查看答案及解析
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是
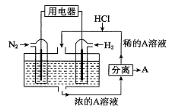
A.通入N2的电极发生的电极反应式为:N2 + 6e- + 8H+== 2NH4+
B.反应过程中溶液的pH会变大,故需要加入盐酸
C.该电池外电路电流从通入H2的电极流向通入N2的电极
D.通入H2的电极为负极,A为NH4Cl
高三化学选择题中等难度题查看答案及解析
科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是
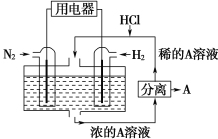
A. 通入N2的电极发生的电极反应式为:N2+6e-+8H+=2NH4+
B. 反应过程中溶液的pH会变大,故需要加入盐酸
C. 该电池外电路电流从通入H2的电极流向通入N2的电极
D. 通入H2的电极为负极,A为NH4Cl
高三化学单选题简单题查看答案及解析
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将甲烷燃料电池作为电源进行氯化镁溶液龟解实验,电解装置如图所示。
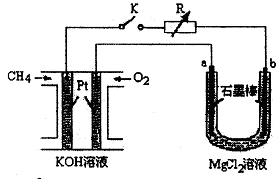
请回答下列问题:
(1)甲烷燃料电池负极的电极反应式为: ________。
(2)闭合开关K后,a、b电极上均有气体产生,其中a电极上的气体可用________检验,b电极上得到的气体是________,电解氯化镁溶液的离子方程式为________。
(3)若甲烷通入量为1.12 L(标准状况),且反应完全,则理论上通过电解池的电子的物质的量为________,产生的氯气体积为________L(标准状况)。
(4)已知常温常压下,0.25molCH4完全燃烧生成CO2和H2O时,放出222.5kJ热量,请写出CH4燃烧热的热化学方程式。
已知;①C(石墨)+O2(g)=CO2(g)△H1=-393.5kJ/mol
②2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ/mol
计算:C(石墨)与H2(g)反应生成1molCH4(g)的△H=________。
高三化学填空题困难题查看答案及解析
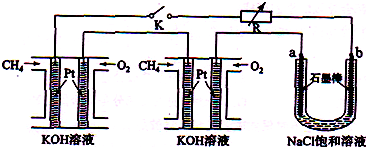
高三化学解答题中等难度题查看答案及解析