-
合成氨工业中氢气可由天然气和水蒸汽反应制备,其主要反应为:
CH4+ 2H2O  CO2+4H2,已知:
CO2+4H2,已知:
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890KJ/mol
2H2(g)+O2(g)=2H2O(l) △H=-571.6KJ/mol
H2O(g)=H2O(l) △H=-44KJ/mol
(1)写出由天然气和水蒸汽反应制备H2的热化学方程式: 。
(2)某温度下,10L密闭容器中充入2mol CH4和3mol H2O(g),发生CH4(g)+ 2H2O(g)  CO2(g)+4H2 (g)反应,过一段时间反应达平衡,平衡时容器的压强是起始时的1.4倍。
CO2(g)+4H2 (g)反应,过一段时间反应达平衡,平衡时容器的压强是起始时的1.4倍。
则①平衡时,CH4的转化率为 ,H2的浓度为 ,反应共放出或吸收热量 KJ。
②升高平衡体系的温度,混合气体的平均相对分子质量 ,密度 。(填“变大”“变小”或“不变”)。
③当达到平衡时,充入氩气,并保持压强不变,平衡将 (填“正向”“逆向”或“不”)移动。
④若保持恒温,将容器压缩为5L(各物质仍均为气态),平衡将 (填“正向”“逆向”或“不”)移动。达到新平衡后,容器内H2浓度范围为 。
-
天然气(以甲烷计)在工业生产中用途广泛。
Ⅰ.在制备合成氨原料气H2 中的应用
(1)甲烷蒸汽转化法制H2的主要转化反应如下:
CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH = +206.2 kJ/mol
CO(g) + 3H2(g) ΔH = +206.2 kJ/mol
CH4(g) + 2H2O(g)  CO2(g) +4H2(g) ΔH = +165.0kJ/mol
CO2(g) +4H2(g) ΔH = +165.0kJ/mol
上述反应所得原料气中的CO能使氨合成催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时又可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是________。
(2)CO变换反应的汽气比(水蒸气与原料气中CO物质的量之比)与CO平衡变换率
(已转化的一氧化碳量与变换前一氧化碳量之比)的关系如下图所示:
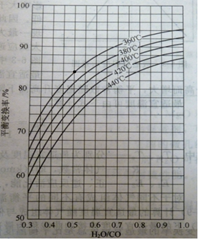
汽气比与CO平衡变换率的关系
析图可知:
① 相同温度时,CO平衡变换率与汽气比的关系是________。
② 汽气比相同时,CO平衡变换率与温度的关系是________。
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度也可以表示平衡常数(记作Kp),则CO变换反应的平衡常数表示式为:Kp=________。随温度的降低,该平衡常数________(填“增大”“减小”或“不变”)。
Ⅱ.在熔融碳酸盐燃料电池中的应用
以熔融Li2CO3和K2CO3为电解质,天然气经内重整催化作用提供反应气的燃料电池示意图如下:
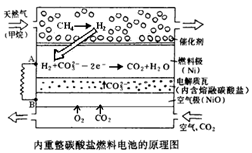
(1)外电路电子流动方向:由________流向________(填字母)。
(2)空气极发生反应的离子方程式是________。
(3)以此燃料电池为电源电解精炼铜,当电路有0.6 mol e‑ 转移,有________ g 精铜析出。
-
甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H1=-890.3kJ·mol-1
CO(g)+ O2(g)=CO(g) ∆H2=-283.0kJ·mol-1
O2(g)=CO(g) ∆H2=-283.0kJ·mol-1
H2(g)+ O2(g)=H2O(l) ∆H3=-285.8kJ•mol-1
O2(g)=H2O(l) ∆H3=-285.8kJ•mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ∆H4=-41.0kJ•mol-1
则甲烷水蒸气重整反应的△H=__kJ·mol-1。
(2)通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行了热力学计算,反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。
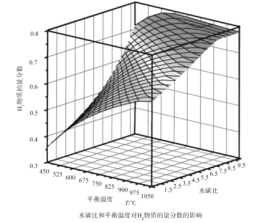
①H2的物质的量分数与水碳比(1~10)的关系是平衡温度一定时,__;其原因是__。
②据模拟实验可知,平衡温度为900℃,水碳比为1.0时,H2的物质的量分数为0.6,CH4的转化率为__,其压强平衡常数为__;反应速率方程为v=kp(CH4)p-1(H2),此时反应速率=__(已知:气体分压=气体的物质的量分数×总压,速率方程中k为速率常数)。
(3)厌氧细菌可将葡萄糖转化为CH4和H2,pH为5.5时不同热预处理温度和时间下的甲烷和氢气的产率如图所示,若要提高H2的产率,最佳温度为__;与甲烷水蒸气重整制氢相比其优点有__(至少写两点)。

-
甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H1=-890.3kJ·mol-1
CO(g)+ O2(g)=CO(g) ∆H2=-283.0kJ·mol-1
O2(g)=CO(g) ∆H2=-283.0kJ·mol-1
H2(g)+ O2(g)=H2O(l) ∆H3=-285.8kJ•mol-1
O2(g)=H2O(l) ∆H3=-285.8kJ•mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ∆H4=-41.0kJ•mol-1
则甲烷水蒸气重整反应的△H=__kJ·mol-1。
(2)通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行了热力学计算,反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。
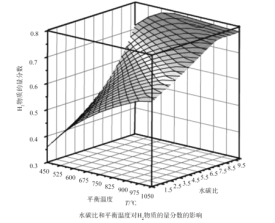
①H2的物质的量分数与水碳比(1~10)的关系是平衡温度一定时,__;其原因是__。
②据模拟实验可知,平衡温度为900℃,水碳比为1.0时,H2的物质的量分数为0.6,CH4的转化率为__,其压强平衡常数为__;反应速率方程为v=kp(CH4)p-1(H2),此时反应速率=__(已知:气体分压=气体的物质的量分数×总压,速率方程中k为速率常数)。
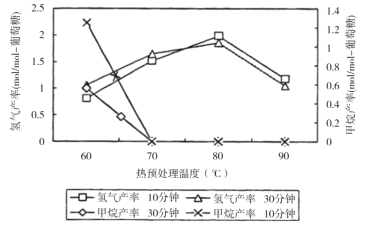
(3)厌氧细菌可将葡萄糖转化为CH4和H2,pH为5.5时不同热预处理温度和时间下的甲烷和氢气的产率如图所示,若要提高H2的产率,最佳温度为__;与甲烷水蒸气重整制氢相比其优点有__(至少写两点)。
-
甲烷水蒸气的重整反应是工业制备氢气的重要方式,其化学反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:
(1)已知CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-890.3kJ·mol-1
CO(g)+0.5O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
H2(g)+0.5O2(g)=H2O(l) ΔH3=-285.8kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH4=-41.0kJ·mol-1
则甲烷水蒸气重整反应的ΔH=_____kJ·mol-1。
(2)通过计算机模拟实验,对400~1200℃、操作压强为0.1MPa条件下,不同水碳比(1~10)进行了热力学计算,反应平衡体系中H2的物质的量分数与水碳比、平衡温度的关系如图所示。
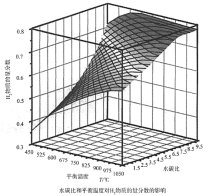
①温度一定时,H2的物质的量分数与水碳比(1~10)的关系是_____,产生该结论的原因是_____。
②据模拟实验可知,平衡温度为900℃,水碳比为1.0时,H2的物质的量分数为0.6,CH4的转化率为_____,其压强平衡常数为_____;反应速率方程为v=kp(CH4)p-1(H2),此时反应速率v=_____。
(已知:气体分压=气体的物质的量分数×总压,速率方程中k为速率常数)。
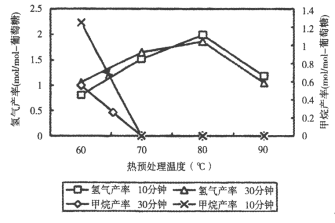
(3)厌氧细菌可将葡萄糖转化为CH4和H2,pH为5.5时不同热预处理温度和时间下的甲烷和氢气的产率如图所示,若要提高H2的产率,最佳温度为_____。
-
下图为工业合成氨生产简易流程图:
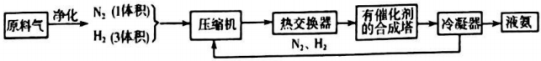
回答下列问题:
(1)合成氨所需的氮气来源于__________;合成氨所需的原料气氢气可由天然气制备,其主要反应为CH4(g)+H2O(g)=CO(g)+3H2(g);CH4和O2的反应:2CH4(g)+O2(g)=2CO(g)+4H2(g).CH4和H2O(g)及富氧空气(O2含量较高,不同富氧空气中氧气含量不同)混合反应,产物气体组成如下表:
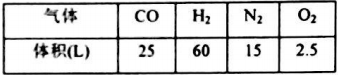
计算该富氧空气中O2和N2的体积比V(O2):V(N2)=__________。
(2)在合成氨的原料气中混有的杂质必须除去的原因是__________;
上述流程中热交换器的作用是__________。从合成塔出来的混合气体,通常仅含有15%(体积分数)的氨。为提高原料的利用率,通常采取的措施是__________。
(3)合成氮为放热反应,但工业上采用400℃-500℃的温度,主要原因是:
①该温度范围内反应速率较快,②__________。
(4)氨可与CO2反应制备尿素(CO(NH2)2],反应过程分为两步,试写出有关的化学方程式:
①氮气与二氧化碳在加热加压条件下化合生成氨基甲酸铵(H2NCOONH4):__________。
②氨基甲酸铵受热分解为尿素与水:__________。
(5)新法合成氨常采用电解法合成。即常压下将氢气和用氢气稀释的氮气分别通入一个加热到570℃的电解池中,氢气和氮气在电极上合成了氨,大大提高了氨的产率,新法合成氨所用的电解质能传导H+,则阴极的电极反应式为__________。
-
化学反应原理在工业生产中具有十分重要的意义。
(1)合成氨用的氢气有多种制取方法:请你写出用C制备水煤气的化学反应方程式________。还可以由天然气或重油制取氢气:CH4+H2O(g) 高温催化剂CO+3H2;比较以上两种方法转移6mol电子时,C和CH4的质量之比是________。
(2)工业生产可以用NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如下:
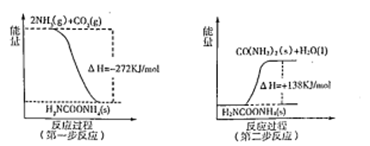
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为________。
(3)已知反应Fe(s)+CO2(g)=FeO(s)+CO(g) △H=akJ/mol。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
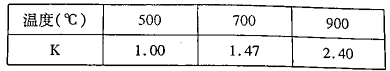
①该反应的化学平衡常数表达式K=________,a________0(填“>”、“<”或“:”)。在500℃2L密闭容器中进行反应,Fe和CO2的起始量均为4 mol,则5min后达到平街时CO2的转化率为________,生成CO的平均速率v(CO)为________。
②700℃反应达到平衡后,要使该平衡向右移动,其他条件不变时,可以采取的措施有________(填字母)。
A.缩小反应器容积 B.增加Fe的物质的量
C.升高温度到900℃ D.使用合适的催化剂
-
合成氨反应是化学上最重要的反应:
(1)合成氨原料气中的氢气可利用天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应制得,反应中每生成2mol CO2吸收316kJ热量,该反应的热化学方程式是 ,该方法制得的原料气中主要杂质是CO2,若用K2CO3溶液吸收,该反应的离子方程式是 .
(2)已知N2(g)+3H2(g)⇌2ΝΗ3(g)△H<0.图是当反应器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线.
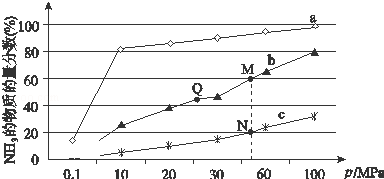
①曲线a对应的温度是 .
②关于工业合成氨的反应,下列叙述正确的是 (填序号)
A.图中M、N、Q点平衡常数K的大小关系为K(M)=K(Q)>K(N)
B.加催化剂能加快反应速率但H2的平衡转化率不变
C.相同压强下,投料相同,达到平衡消耗时间关系为c>b>a
D.由曲线a可知,当压强增加到100MPa以上,NH3的物质的量分数可达到100%
③N点时c(NH3)=0.2mol•L﹣1,N点的化学平衡常数K= (用分数表示).
(3)合成氨工业中含氨废水的处理方法之一是电化学氧化法,将含氨的碱性废水通入电解系统后,在阳极上氨被氧化成氮气而脱除,阳极的电极反应式为 .
(4)NH3 可以处理NO2 的污染,方程式如下:NO2+NH3 N2+H2O(未配平)当转移0.6mol电子时,消耗的NO2在标准状况下是 L.
N2+H2O(未配平)当转移0.6mol电子时,消耗的NO2在标准状况下是 L.
-
合成氨反应是化学上最重要的反应:
(1)合成氨原料气中的氢气可利用天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应制得,反应中每生成2 mol CO2吸收316kJ热量,该反应的热化学方程式是_______________________,该方法制得的原料气中主要杂质是CO2,若用K2CO3溶液吸收,该反应的离子方程式是________________。
(2)已知N2(g)+3H2(g) 2NH3(g) ΔH<0。下图是当反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
2NH3(g) ΔH<0。下图是当反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
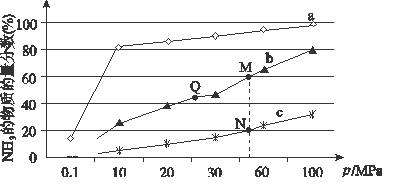
①曲线a对应的温度是________。
②关于工业合成氨的反应,下列叙述正确的是________(填序号)
A.上图中M、N、Q点平衡常数K的大小关系为K(M)=K(Q) >K(N)
B.加催化剂能加快反应速率但H2的平衡转化率不变
C.相同压强下,投料相同,达到平衡消耗时间关系为c>b>a
D.由曲线a可知,当压强增加到100 MPa以上,NH3的物质的量分数可达到100%
③N点时c(NH3)=0.2 mol·L-1,N点的化学平衡常数K=_________________(精确到小数点后两位)。
(3)合成氨工业中含氨废水的处理方法之一是电化学氧化法,将含氨的碱性废水通入电解系统后,在阳极上氨被氧化成氮气而脱除,阳极的电极反应式为______________________。
(4)NH3 可以处理NO2 的污染,方程式如下: NO2+ NH3 N2+ H2O(未配平)当转移0.6 mol电子时,消耗的NO2在标准状况下是 L。
N2+ H2O(未配平)当转移0.6 mol电子时,消耗的NO2在标准状况下是 L。
-
煤制合成天然气是煤气化的一种重要方法,其工艺核心是合成过程中的甲烷化,涉及的主要反应:
CO(g)+3H2(g) CH4(g)+H2O(g) ΔH<0 ①
CH4(g)+H2O(g) ΔH<0 ①
CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH<0 ②
CH4(g)+2H2O(g) ΔH<0 ②
现在300 ℃、容积为2 L的密闭容器中进行有关合成天然气的实验,相关数据记录如下:
| CO/mol | CO2/mol | H2/mol | CH4/mol | H2O/mol |
| 0 min | 4 | 3 | 40 | 0 | 0 |
| 30 min | 2 | 2 | a | 3 | |
| 70 min | 1 | b | c | d | 6 |
下列有关说法错误的是
A.a=30,b=1.5
B.c=25,d=4.5
C.前30 min内,反应①的平均反应速率v(CH4)=0.05 mol·L−1·min−1
D.后40 min内,反应②的平均反应速率v(H2)=0.025 mol·L−1·min−1
CO2+4H2,已知:
CO2(g)+4H2 (g)反应,过一段时间反应达平衡,平衡时容器的压强是起始时的1.4倍。






 CO(g)+3H2(g)。回答下列问题:
CO(g)+3H2(g)。回答下列问题:






