-
黄铜矿(CuFeS2)是冶炼铜及制备铁的氧化物的重要矿藏,常含有微量的金、银等。如图是以黄铜矿为主要原料生产铜、铁红(氧化铁)颜料的工艺流程图:
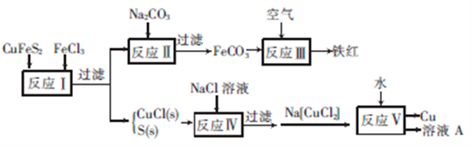
(1)反应Ⅰ的离子方程式为_________________________________________。
(2)CuCl难溶于水,但可与过量的Cl-反应生成溶于水的[CuCl2]-。该反应的离子方程式为_________________________________________________。
(3)有大量Cl-存在时,Na2SO3可将CuCl2还原成[CuCl2]-。 Na2SO3要缓慢滴加到溶液中的原因是_________________________________________________。
(4)反应Ⅰ〜Ⅴ五个反应中属于非氧化还原反应的是反应____________。
(5)已知Cu+在反应Ⅴ中发生自身氧化还原反应,歧化为Cu2+和Cu,由此可推知溶液A中的溶质为_______________(填化学式)。
(6)含AsO43-的废水对环境造成严重污染,常用新制的氢氧化铁沉淀与之作用形成FeAsO4沉淀而除去,相同温度下溶解度:Fe(OH)3__________(填“<”“ >”或“=”)FeAsO4。
(7)在酸性、有氧条件下,一种叫Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程中发生反应的离子方程式为________________________________。
(8)将一定量的铁红溶于160 mL 5 mol • L-1盐酸中,再加入足量铁粉,待反应结束后共收集到气体2.24 L (标准状况),经检测,溶液中无 Fe3+,则参加反应的铁粉的质量为_____________。
-
黄铜矿(CuFeS2)是冶炼铜及制备铁氧化物的重要矿藏,常含有微量金、银等。下图是以黄铜矿为主要原料生产铜、铁红(氧化铁)颜料的工艺流程图:

(1)CuCl难溶于水,但可与过量Cl-反应生成可溶于水的[CuCl2]-,该反应的离子方程式为________________________________。
(2)有大量Cl-存在时,Na2SO3可将CuCl2还原成[CuCl2]-,因此Na2SO3要缓慢滴入到溶液中的原因是_______________________________。
(3)反应I〜V中,属于非氧化还原反应的是反应_______________________。
(4)已知反应V中Cu+发生自身氧化还原反应,歧化为Cu2+和Cu,由此可推知溶液A中的溶质为________________(填化学式)。
(5)在酸性、有氧条件下,一种叫做Thibacillus ferroxidans的细菌能将黄铜矿转化成硫酸盐,该过程中发生反应的离子方程式为_____________________________。
(6)将一定量铁红溶于160 mL 5 mol·L-1盐酸中,再加入足量铁粉,待反应结束后共收集气体2.24L(标准状况下),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为_____________g。
-
黄铜矿(CuFeS2)是重要的矿藏,以黄铜矿为原料生产碱式氯化铜和铁红(氧化铁)颜料的工艺流程如图所示。
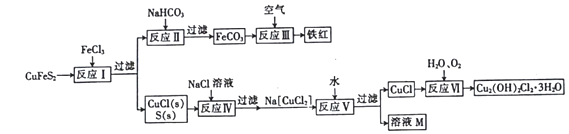
(1)反应Ⅰ的离子方程式为_____________ ,该反应的氧化剂是________________。
(2)反应Ⅱ的离子方程式为_________________________。
(3)反应Ⅵ是在45~50 ℃的条件下进行的,写出该反应的化学方程式:__________________。
(4)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O,为测定某碱式氯化铜的组成,某实验小组进行下列实验:
①称取样品9.30 g,用少量稀HNO3 溶解后配成100.00 mL溶液A;
②取25.00 mL溶液A,加入足量AgNO3 溶液,得到AgCl 固体1.435 g;
③另取25.00 mL 溶液A,调节pH 为4~5,用浓度为0.40 mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+(离子方程式为Cu2++ H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液50.00 mL。通过计算确定该样品的化学式为___________(填化学式)。
-
黄铜矿(CuFeS2)是重要的矿藏,以黄铜矿为原料生产碱式氯化铜和铁红(氧化铁)颜料的工艺流程如图所示。
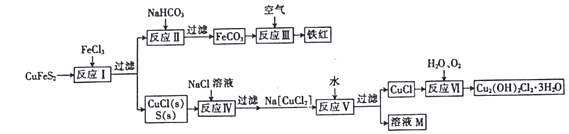
(1)反应Ⅰ的离子方程式为_____________,该反应的氧化剂是________________。
(2)反应Ⅱ的离子方程式为_________________________。
(3)反应Ⅵ是在45~50℃的条件下进行的,写出该反应的化学方程式:__________________。
(4)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O,为测定某碱式氯化铜的组成,某实验小组进行下列实验:①称取样品9.30g,用少量稀HNO3溶解后配成100.00mL溶液A;②取25.00mL溶液A,加入足量AgNO3 溶液,得到AgCl固体1.435g;③另取25.00mL溶液A,调节pH 为4~5,用浓度为0.40mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液50.00mL。通过计算确定该样品的化学式为___________(填化学式)。
-
黄铜矿(CuFeS2)是重要的矿藏,以黄铜矿为原料生产碱式氯化铜和铁红(氧化铁)颜料的工艺流程如图所示。
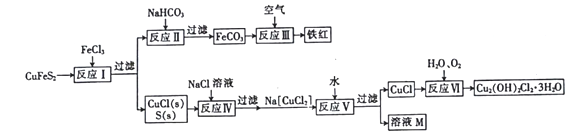
(1)反应Ⅰ的离子方程式为_____________,该反应的氧化剂是________________。
(2)反应Ⅱ的离子方程式为_________________________。
(3)反应Ⅵ是在45~50℃的条件下进行的,写出该反应的化学方程式:__________________。
(4)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O,为测定某碱式氯化铜的组成,某实验小组进行下列实验:①称取样品9.30g,用少量稀HNO3溶解后配成100.00mL溶液A;②取25.00mL溶液A,加入足量AgNO3 溶液,得到AgCl固体1.435g;③另取25.00mL溶液A,调节pH 为4~5,用浓度为0.40mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液50.00mL。通过计算确定该样品的化学式为___________(填化学式)。
-
黄铜矿(CuFeS2)是重要的矿藏,以黄铜矿为原料生产碱式氯化铜和铁红(Fe2O3)颜料的工艺流程如图所示。
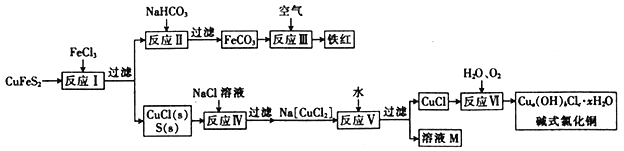
已知:a、b、c、x均为整数。
(1)该流程需进行多次过滤,过滤时用到的玻璃仪器为__________、__________和__________。
(2)反应Ⅰ的离子方程式为__________________,该反应的还原剂是__________(填化学式,下同),氧化产物是__________。
(3)反应Ⅱ 的离子方程式为___________________________。
(4)反应Ⅵ是在45~50℃的条件下进行的,该反应中氧化剂与还原剂的物质的量之比为____________。
(5)为测定制得的碱式氯化铜的组成,某实验小组进行下列实验:
①称取样品9.30g,用少量稀HNO3 溶解后配成100.00 mL溶液A;
②取25.00mL溶液A,加入足量AgNO3溶液,得到AgCl 固体1.435 g;
③另取25.00mL溶液A,调节pH为4~5,用浓度为0.40mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液50.00 mL。通过计算确定该样品的化学式为_________________________(填化学式)。
-
铜是一种重要的战略物资,以黄铜矿(主要成分是CuFeS2)为主要原料生产铜、铁红、单质硫时,原料的综合利用率较高,其主要流程如图所示(己知Na[CuCl2]的电离方程式为:Na[CuCl2]=Na++[CuCl2]-):

(1)流程中粉碎的目的是_____________,操作①、②、③、④的目的相同,在实验中这种操作的名称是____________。
(2)铁红的重要用途:__________________,固体B中含有两种产物,一种是单质C、另一种是原子个数比为1:l 的一种金属的低价态盐,写出堆浸时反应的化学方程式:________。
(3)反应V的离子方程式:___________________。
(4)此方法中得到的铜纯度不能满足某些生产的需要,需要利用电解法进行提纯。若用如图所示的装置进行电解精炼,则乙中溶液的溶质是_________,e电极上的电极反应式为_____。

若当电路中有2mol电子通过时,乙中某个电极质量减轻了63.92g,则粗铜的纯度为(假设杂质只有铁且精炼时铜与铁的放电比例与混合物比例相同,计算时用%表示保留一位小数)____________(已知相对原子质量:Fe 56 Cu 64 )。
-
(14分)黄铜矿( CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)、若冶炼铜的反应为:8 CuFeS2+21O2  8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
CuFeS2中Fe的化合价为+2,反应中被氧化的元素是___________(填元素符号)。
(2)、上述冶炼过程中产生大量SO2,下列处理方案合理的是___________(填代号)。
a.高空排放 b.用于制备硫酸
c.用浓硫酸吸收 d.用纯碱溶液吸收制Na2SO3
(3)、采用火法熔炼工艺生产铜的中间过程会发生Cu2O与Cu2S在高温下转化为Cu,放出SO2气体的反应。若Cu2O和Cu2S正好完全反应,Cu2O和Cu2S的物质的量之比为_____;Cu2S和HNO3有如下反应:3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO +8H2O若生成11.2LNO(标准状况),则反应中转移电子的物质的量为__________。
+8H2O若生成11.2LNO(标准状况),则反应中转移电子的物质的量为__________。
(4)、过二硫酸钾(K2S2O8)具有强氧化性,可将I—氧化为I2:S2O82-+2I— 2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe2+对上述反应的催化过程:____________________________、______________________________。
2SO42-+I2通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe2+对上述反应的催化过程:____________________________、______________________________。
-
(11分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是 (填代号)。
a.高空排放 b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO4 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I—氧化为I2:S2O82—+2I—=2SO42—+I2。通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程: 、 (不必配平)
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
a.除去Al3+的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为 。
证明炉渣中含有FeO的实验现象为 。
-
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是________(填元素符号)。
(2)上述冶炼过程中产生大量SO2。下列处理方案合理的是________(填代号)。
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧。
据以上信息回答下列问题:
a.除去Al3+的离子方程式是________。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水。所选试剂为________。证明炉渣中含有FeO的实验现象为________。







