-
Ⅰ.请回答:
(1)燃着的钠不能用CO2灭火,其理由 (用化学方程式表示)。
(2)完成以下氧化还原反应的离子方程式:
( )Fe3++( )ClO-+______=( )FeO42-+( )Cl-+( )H2O
(3)剧毒物氰化钠的电子式为 ,碳元素的化合价为 ;用ClO2处理泄漏的氰化钠,得到无毒的NaCl、N2和CO2。若处理4×10-5mol·L-1的废水1000L,至少需要ClO2的质量为 g。
,碳元素的化合价为 ;用ClO2处理泄漏的氰化钠,得到无毒的NaCl、N2和CO2。若处理4×10-5mol·L-1的废水1000L,至少需要ClO2的质量为 g。
II.化合物A是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:
A(s)+H2(g) B(s)+LiH(s) ΔH= -44.5kJ•mol-1……①
B(s)+LiH(s) ΔH= -44.5kJ•mol-1……①
已知:①在液氨中加入金属锂生成B和氢气;
②一定条件下,2.30g固体B与5.35gNH4Cl固体恰好完全反应,生成固体盐C和4.48L气体D (已折算成标准状况);气体D能使湿润的红色石蕊试纸变蓝色。
(1)A的化学式为 ,LiH中r(Li+) r(H-)(填“大于”或“小于”)。
(2)写出液氨与金属锂反应的化学方程式 。
(3)B在加强热时生成NH3和另一种化合物E,该分解反应的化学方程式为 。
(4)化合物E也可以作储氢材料,其储氢原理可表示为:
E(s)+H2(g) A(s)+LiH(s) ΔH= -165kJ·mol-1…………②
A(s)+LiH(s) ΔH= -165kJ·mol-1…………②
储氢材料可以通过加热的方式释放氢气。从实用化角度考虑,选择 (填“A”或“E”)作储氢材料更合理,理由是 。
-
I、请回答:
(1)H2O2的电子式 。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由 。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式 。
(4)完成以下氧化还原反应的离子方程式:
( )MnO4-+( ) C2O42-+ =( )Mn2+ ( ) CO2↑+
II、化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。请推测并回答:
(1)甲的化学式 。
(2)甲与AlCl3反应得到NaAlH4的化学方程式 。
(3)NaA1H4与水发生氧化还原反应(有H2产生)的化学方程式 。
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(即把铁锈转化为铁单质),脱锈(铁锈的成分表示为Fe2O3)过程发生反应的化学方程式为: 。
(5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。
判断该同学设想的制备和验纯方法的合理性并说明理由:
制备过程 ,
验纯方法 。
-
I 请回答:
(1)HClO的结构式 。
(2)明矾可用来净水,用离子方程式表示其理由 。
(3)MgCO3悬浊液经煮沸可转化为更难溶的Mg(OH)2,转化的化学方程式是 。
(4)完成以下氧化还原反应的离子方程式:
( )Fe3+ + ( )Cl2+ = ( )FeO42- + ( )Cl- +
II 盐湖提锂脱镁渣主要成分为Mg(OH)2、Li2CO3和少量CaCO3,利用盐湖提锂脱镁渣制备高纯轻质氧化镁,为盐湖镁资源综合回收利用提供了一条可行途径,生产流程如图所示:

回答下列问题:
(1)固体A的成分是 。
(2)固体A在真空、1200℃条件下与硅单质反应生成金属镁,反应的化学方程式为 。
(3)沉淀物X中存在Mg5(CO3)4(OH)2·4H2O,则盐湖提锂脱镁渣与NH4HCO3溶液反应生成Mg5(CO3)4(OH)2·4H2O的化学方程式是 。
(4)实际生产中NH4HCO3与Mg(OH)2等物质的量之比要比(3)中反应理论值大的原因是
。
(5)欲检验沉淀物X是否煅烧完全,请设计简要的实验方案:
。
-
I.(7分)请回答:
(1)CO2的电子式 。
(2)钠燃烧不能用CO2灭火,用化学方程式表示其理由 。
(3)重晶石(BaSO4)不溶于酸,用饱和Na2CO3处理转化为易溶于酸的BaCO3,写出反应的离子方程式 。
(4)完成以下氧化还原反应的离子方程式:
( )Cr2O + ( )H2O2+ _____ =( ) Cr3++ ( ) O2 ↑ + ________
+ ( )H2O2+ _____ =( ) Cr3++ ( ) O2 ↑ + ________
II.(8分)化合物K3Fe(A2B4)3·3H2O是重要的催化剂。将化合物K3Fe(A2B4)3·3H2O受热完全分解,只得到气体产物和固体产物。经分析,气体产物只有甲、乙和水蒸气。已知甲、乙均由A、B两元素组成,且摩尔质量:M(甲)<M(乙)。A元素的最外层电子数是次外层电子数2倍,B元素的主族序数是其所在周期数的3倍。经分析,固体产物只有Fe、FeO 和K2AB3。某同学再进行以下定量分析。
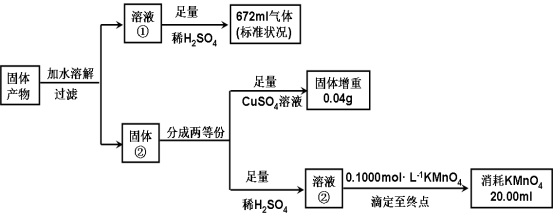
(1)甲的化学式: 。
(2)溶液②与KMnO4发生氧化还原的离子方程式: 。
(3)由以上实验数据的分析可知n(Fe):n(FeO) :n(K2AB3) = : : 。
(4)某同学认为:溶液②由紫红色变为无色,振荡试样半分钟内不变色,即可证明溶液②与KMnO4溶液反应到达滴定终点。判断该同学设想的合理性并说明理由 。
-
(16分) Ⅰ请回答:
(1)CO2的电子式____________________
(2)钠燃烧不能用CO2灭火,用化学方程式表示其理由________________
(3)重晶石(BaSO4)不溶于酸,用饱和Na2CO3处理转化为易溶于酸的BaCO3,写出反应的离子方程式__________________
Ⅱ。化合物K3Fe(A2B4)3.3H2O 是重要的催化剂。将化合物K3Fe(A2B4)3.3H2O受热完全分解,只得到气体产物和固体产物。 经分析,气体产物只有甲、乙和水蒸气。已知甲、乙均由A、B两元素组成,且摩尔质量:M(甲)>M(乙)。A元素的最外层电子数是次外层电子数的2倍,B元素的主族序数是其所在周期数的3倍。 经分析,固体产物只有Fe、FeO和K2AB3。某同学再进行以下定量分析。
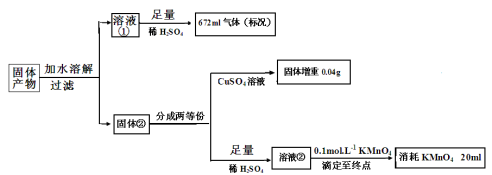
(1)甲的化学式:____________________
(2)溶液②与KMnO4发生氧化还原反应的离子方程式:_______________________
(3)由以上实验数据的分析可知n(Fe):n(FeO):n(K2AB3)= : :
(4)某同学认为:溶液②由紫红色变为无色,振荡试样半分钟内不变色,即可证明溶液②与KMnO4溶液反应达滴定终点。判断该同学设想的合理性并说明理由
-
Ⅰ.(6分) 请回答:
(1)H2O2的电子式___________。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由________________。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式_____________。
(4)完成以下氧化还原反应的离子方程式:
( )MnO4-+( )C2O42-+______=( )Mn2++( )CO2↑+________
Ⅱ.(12分) 化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(1)甲的化学式__________。
(2)甲与AlCl3反应得到NaAlH4的化学方程式__________。
(3)NaAlH4与水发生氧化还原反应的化学方程式__________。
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式 。
(5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生H2,即可证明得到的甲一定是纯净的。
判断该同学设想的制备和验纯方法的合理性并说明理由___________。
-
请回答:
(1)H2O2的电子式___________。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由________________。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式___________。
(4)完成以下氧化还原反应的离子方程式:
(______)MnO4-+(______)C2O42-+______=(______)Mn2++(______)CO2↑+________。
Ⅱ.SnSO4是一种重要的硫酸盐,在工业生产中有着广泛的应用。其制备路线如图:
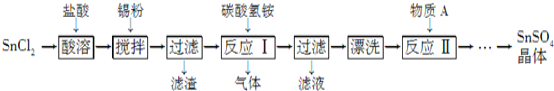
已知:在酸性条件下,溶液中的Sn2+可被空气中的氧气氧化成Sn4+;SnCl2能水解生成碱式氯化亚锡。
(1)写出物质A的名称:_____。
(2)SnCl2用盐酸而不用水溶解的原因是___________(用化学方程式表示)。
(3)锡粉的作用是除去酸溶时产生的少量Sn4+,请写出产生Sn4+的离子方程式: _________。
(4)反应Ⅰ生成的沉淀为SnO,写出该反应的化学方程式:___________________。 该反应的温度需要控制在75 ℃左右的原因是______________。
-
(1)镁燃烧不能用CO2灭火,用化学方程式表示其理由 。
(2)用H2O2和稀H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,请写出表示该过程的化学方程式 。
(3)在NaAlO2溶液中通入过量的CO2 (用离子方程式表示)
(4)污水及自来水处理的方法有很多。
Fe2(SO4)3 净水的原理是 。
使用时发现Fe2(SO4)3 并不能使酸性废水中的悬浮物沉降除去,其原因是 。
在酸性环境下,向含重铬酸根的废水中加入FeSO4溶液,然后调节pH,使生成的Cr3+转化为Cr(OH)3,写出第一步反应的离子方程式 。
(5)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+,则下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是 。
①硫酸铝和氨水 ②偏铝酸钠和稀盐酸 ③ 硫酸锌和氢氧化钠 ④ 硫酸锌和氨水
-
下列化学反应中,既是氧化还原反应,又可以用离子方程式表示的为( )
A.铁粉放入硫酸铜溶液
B.CO2气体通入澄清石灰水
C.大理石高温分解
D.KClO3在MnO2催化下加热制O2
-
氧化还原反应在生产、生话中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂。用所学知识回答问题:
(1)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的化学方程式为 ,反应中消耗1mol的MnO4—时转移电子数为 。
(2)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是 mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是 ,又变为棕黄色的原因是 。
,碳元素的化合价为 ;用ClO2处理泄漏的氰化钠,得到无毒的NaCl、N2和CO2。若处理4×10-5mol·L-1的废水1000L,至少需要ClO2的质量为 g。
B(s)+LiH(s) ΔH= -44.5kJ•mol-1……①
A(s)+LiH(s) ΔH= -165kJ·mol-1…………②



