-
(12分)氮及其化合物在工农业生产、生活中有着重要作用。
(1)下图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式 。
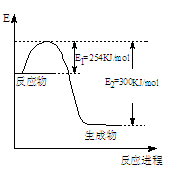
(2)已知:H-H、N≡N键能分别为435 kJ·mol-1、943 kJ·mol-1,则结合(1)图中数据,计算N-H的键能 kJ·mol-1。
(3)已知:N2(g)+2O2(g) N2O4(l);△H1= -19.5 kJ·mol-1;
N2H4(l)+O2(g) N2(g)+2H2O(g) ;△H2= -534.2 kJ·mol-1
肼(N2H4)与氧化剂N2O4反应生成N2和水蒸气。写出该反应的热化学方程式 。
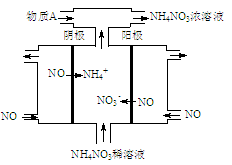
(4)工业上可电解NO制备NH4NO3,其工作原理如图所示,该阳极发生的电极反应式为 。为使电解产物全部转化为5mol NH4NO3,需补充的物质是 (填化学式),此时电子转移的物质的量为 mol。
-
(8分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
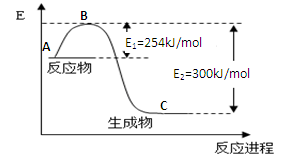
(1)上图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:________;
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能________kJ·mol-1
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后E1和E2的变化是:E1______,E2______(填“增大”、“减小、”“不变”)。
(4)用NH3催化还原NOX还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ;△H1= akJ·mol-1
N2(g)+O2(g) 2NO(g);△H2= bkJ/mol
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=kJ/mol(用含a、b的式子表示)
【解析】(1)根据反应进程可判断反应物的能量高,生成物的能量低,所以热化学方程式为N2(g)+3H2(g) 2NH3(g) △H=-92 kJ/mol。
2NH3(g) △H=-92 kJ/mol。
(2)反应热就是断键吸收的能量和成键所放出的能量的差值,所以有943kJ/mol+3×435 kJ/mol-2×3×x=-92 kJ/mol ,解得x=390 kJ/mol。
(3)催化剂能降低反应的活化能,但不能改变反应热,所以E1和E2均减小。
(4)考查盖斯定律的应用,将已知的2个热化学方程式叠加即得到
4NH3+6NO=6H2O+5N2 △H=(a-3b)kJ/mol。所以1mol NH3还原NO至N2,则该反应过程中的反应热 kJ/mol。
kJ/mol。
-
氮是地球上含量丰富的一种元素,氮及其化合物在工 农业生产、生活中有着重要作用,
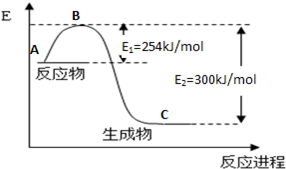
(1)上图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:________。
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能________kJ·mol-1。
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后E1和E2的变化是:E1,E2______,
△H________ (填“增大”、“减小”、“不变”)。
(4)用NH3催化还原NOX还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)= 2N2(g)+6H2O(g) ;△H1=akJ·mol-1
N2(g)+O2(g)=2NO(g); △H2=bkJ/mol
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=kJ/mol(用含a、b的式子表示)。
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)下图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:____________________________________________。
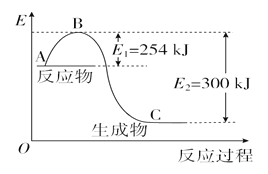
(2)已知化学键键能是形成或拆开1 mol化学键放出或吸收的能量,单位kJ·mol-1。若已知下列数据:
| 化学键 | HH | 
|
| 键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N—H的键能________kJ·mol-1。
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ΔH1=-a kJ·mol-1 ①
N2(g)+O2(g)===2NO(g) ΔH2=-b kJ·mol-1 ②
若1 mol NH3还原NO至N2,则该反应过程中的反应热ΔH3=________ kJ·mol-1(用含a、b的式子表示)。
-
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,
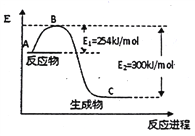
请写出N2和H2反应的热化学方程式:______________________________________________;
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ • mol-1 | 435 | 943 |
试根据表中及图中数据计算N-H的键能____________kJ• mol-1
(3)合成氨反应通常用铁触媒作催化剂。使用铁触媒后的变化是:E1_______,△H________ (填“增大”、“减小、” “不变”)。
(4)用NH3催化还原NO2还可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H1=akJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=bkJ·mol-1
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=_________kJ/mol (用含a、b的式子表示)
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:_______。
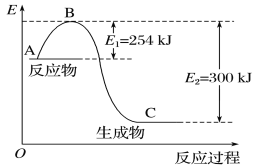
(2)若已知下列数据:
| 化学键 | H—H | N≡N |
| 键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N—H的键能:___kJ·mol-1。
(3)捕碳技术(主要指捕获CO2在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)=(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)=NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)=2NH4HCO3(aq) ΔH3
请回答下列问题:
ΔH3与ΔH1、ΔH2之间的关系是ΔH3=___。
(4)试比较下列两组△H的大小(填“>”、“<”或“=”)
①H2(g)+ O2(g)=H2O(g) △H1 H2(g)+
O2(g)=H2O(g) △H1 H2(g)+ O2(g)=H2O(l) △H2
O2(g)=H2O(l) △H2
则△H1____△H2
②S(s)+O2(g)=SO2(g) △H3
Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+10H2O(l)+2NH3(g) △H4
则△H3______△H4
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是N2和H2反应生成2 mol NH3过程中能量变
化示意图,写出生成NH3的热化学方程式:
_____________________________________________
___________________________。
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能。从化学键的角度分析,化
学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过
程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应N2(g)+3H2(g)2NH3(g) ΔH=a kJ·mol-1。
试根据表中所列键能数据估算a的数值:________。
| 化学键 | H—H | N—H | N≡N |
| 键能kJ·mol-1 | 436 | 391 | 945 |
-
氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
(1)已知:反应i:N2(g)+3H2(g)⇌2NH3(g) △H=-92.4kJ/mol
反应ii:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
则氨气完全燃烧生成氮气和水蒸气的热化学方程式_____。
(2)已知反应i断开1mol化学键所需的能量见下表:
| N≡N | H—H | N—H |
| 键能/kJ·mol-1 | 945 | 436 | ? |
则断开1molN-H键所需的能量是_______kJ
(3)如图表示反应i在500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中M点数据计算N2的平衡体积分数______;该反应的化学平衡常数K的表达式______。
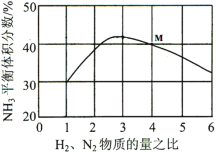
(4)如图是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是______(填“温度”或“压强”);判断L1、L2的大小关系并说明理由_______。

(5)电化学气敏传感器可用于检测环境中NH3的含量,其工作原理如图所示:
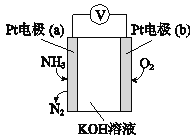
①反应消耗NH3和O2的物质的量之比为____。
②a极的电极反应式为______。
-
氮及其化合物在工农业生产、生活中有着重要作用。
(1)下图1是1molNO2和1mol C O反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式____ 。
O反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式____ 。

(2)在固定容积的密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ·mol-1 用一定物质的量的N2和H2合成NH3,三个容器的反应温度分别为T1、T2、T3且恒定不变,
2NH3(g) △H=-92.4kJ·mol-1 用一定物质的量的N2和H2合成NH3,三个容器的反应温度分别为T1、T2、T3且恒定不变, 在其它条件相同的情况下,实验测得反应均进行到t min时NH3的质量分数如图2所示:
在其它条件相同的情况下,实验测得反应均进行到t min时NH3的质量分数如图2所示:
此 时甲、乙、丙三个容器中一定达到化学平衡状态的是 容器,都达到平衡状态时,NH3的质量分数最高的是 容器(填甲、乙、丙)。
时甲、乙、丙三个容器中一定达到化学平衡状态的是 容器,都达到平衡状态时,NH3的质量分数最高的是 容器(填甲、乙、丙)。
下图3是实验室在三个不同条件的密闭容器中,分别加入浓度均为c(N2)=0.10 mol/L,c(H2) = 0.26 mol/L进行反应时,N2的浓度随时间的变化如下图①、②、③曲线所示。
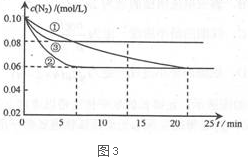
Ⅰ该反应实验②平衡时H2的转化率为 。
Ⅱ据图3所示,②装置中有一个条件与①不同,请指出②相对①改变的条件 。
Ⅲ计算实验③的平衡常数为___________________。
(3)铜与一定浓度硝酸反应时方程式可表示为:Cu+HNO3一Cu(NO3)2+NO +NO2 +H2O(方程式未配平)。3.2 g Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则得到标准状况下NO体积为 L。
-
(1)氮是地球上含量丰富的一种元素,氮及其化合物在工、农业生产和生活中有着重要作用。
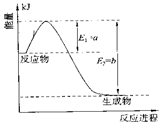
①右图是一定的温度和压强下N2和H2反应生成1molNH3过程中能量变化示意图,请写出工业合成氨的热化学反应方程式:
________________________________________________________。
(△H的数值用含字母a、b的代数式表示)
②在25°C时,将x mol·L-1的氨水与y mol·L-1的盐酸等体积混合,反应后溶液显中性,则反应后的溶液中:c(NH4+)_______c(Cl-)(填“>”、“<”或“=”)
(2)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。在25°C时,向0.1mol·L-1的NaCl溶液中逐滴加入适量的0.1mol·L-1的硝酸银溶液,有白色沉淀生成,向反应后的浊液中,继续加入0.1mol·L-1的NaI溶液,看到的现象是________________,产生该现象的原因是(用离子方程式表示)_______________________________________________________。
(3)下图为一电化学装置,电极分别为铁棒和碳棒。U形管中盛有电解质溶液。
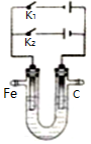
①若U形管中盛有饱和食盐水,打开K2,闭合K1, 铁棒为_______ 极, 碳棒上的电极反应式为_____________________________________________。
②若U形管中是含Cr2O72-的酸性废水,通过该装置可以除去Cr2O72-离子。闭合K2,打开K1,阳极区所发生的反应有:Fe-2e- =Fe2+和 _________________________________________ (写离子反应方程式)












