-
2019年诺贝尔化学奖授予锂离子电池的发明者,LiFePO4是锂离子电池的正极材料。用含锂废渣(主要金属元素的含量:Li 8.50%、Ni 6.55%、Mg 13.24%)制备Li2C2O4,并用其制备LiFePO4部分工艺流程如图(该流程可能造成水体砷污染):

已知:滤液1、滤液2中部分离子的浓度(g·L-1):
| Li+ | Ni2+ | Mg2+ |
| 滤液1 | 22.72 | 20.68 | 60.18 |
| 滤液2 | 21.94 | 7.7×10-3 | 0.78×10-3 |
I.制备Li2C2O4
(1)滤渣2的主要成分有__(填化学式)。
(2)Na2C2O4溶液中各离子的浓度由大到小顺序为__。
(3)写出加入Na2C2O4溶液时发生反应的离子方程式:__。
Ⅱ.制备LiFePO4
(4)将电池极Li2C2O4和FePO4置于高温下反应生成LiFePO4和一种温室气体,该反应的化学方程式是___。
(5)LiFePO4需要在高温下成型后才能作为电极,高温成型时要加入少量石墨,则石墨的作用是__(任写一点)。
(6)我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的As(Ⅴ),其机制模型如图,其中零价铁与过硫酸钠反应的离子方程式是__。在该模型中得到的铁砷共沉淀物经灼烧(无元素化合价变化)后得到一种磁性化合物,化学式为Fe7As2O14,该物质中二价铁与三价铁的个数比为__。

-
2019年诺贝尔化学奖授予锂离子电池的发明者,LiFePO4是锂离子电池的正极材料。用含锂废渣(主要金属元素的含量:Li 8.50%、Ni 6.55%、Mg 13.24%)制备Li2C2O4,并用其制备LiFePO4部分工艺流程如图(该流程可能造成水体砷污染):

已知:滤液1、滤液2中部分离子的浓度(g·L-1):
| Li+ | Ni2+ | Mg2+ |
| 滤液1 | 22.72 | 20.68 | 60.18 |
| 滤液2 | 21.94 | 7.7×10-3 | 0.78×10-3 |
I.制备Li2C2O4
(1)滤渣2的主要成分有__(填化学式)。
(2)Na2C2O4溶液中各离子的浓度由大到小顺序为__。
(3)写出加入Na2C2O4溶液时发生反应的离子方程式:__。
Ⅱ.制备LiFePO4
(4)将电池极Li2C2O4和FePO4置于高温下反应生成LiFePO4和一种温室气体,该反应的化学方程式是___。
(5)LiFePO4需要在高温下成型后才能作为电极,高温成型时要加入少量石墨,则石墨的作用是__(任写一点)。
(6)我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的As(Ⅴ),其机制模型如图,其中零价铁与过硫酸钠反应的离子方程式是__。在该模型中得到的铁砷共沉淀物经灼烧(无元素化合价变化)后得到一种磁性化合物,化学式为Fe7As2O14,该物质中二价铁与三价铁的个数比为__。

-
2019年诺贝尔化学奖授予锂离子电池的发明者,LiFePO4是锂离子电池的正极材料。用含锂废渣(主要金属元素的含量:Li 8.50%、Ni 6.55%、Mg 13.24%)制备Li2C2O4,并用其制备LiFePO4部分工艺流程如图(该流程可能造成水体砷污染):
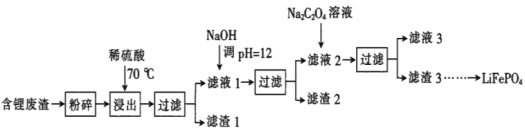
已知:滤液1、滤液2中部分离子的浓度(g·L-1):
| Li+ | Ni2+ | Mg2+ |
| 滤液1 | 22.72 | 20.68 | 60.18 |
| 滤液2 | 21.94 | 7.7×10-3 | 0.78×10-3 |
I.制备Li2C2O4
(1)滤渣2的主要成分有__(填化学式)。
(2)Na2C2O4溶液中各离子的浓度由大到小顺序为__。
(3)写出加入Na2C2O4溶液时发生反应的离子方程式:__。
Ⅱ.制备LiFePO4
(4)将电池极Li2C2O4和FePO4置于高温下反应生成LiFePO4和一种温室气体,该反应的化学方程式是___。
(5)LiFePO4需要在高温下成型后才能作为电极,高温成型时要加入少量石墨,则石墨的作用是__(任写一点)。
(6)我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的As(Ⅴ),其机制模型如图,其中零价铁与过硫酸钠反应的离子方程式是__。在该模型中得到的铁砷共沉淀物经灼烧(无元素化合价变化)后得到一种磁性化合物,化学式为Fe7As2O14,该物质中二价铁与三价铁的个数比为__。
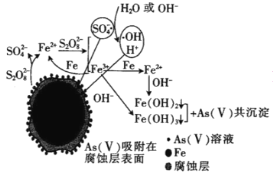
-
2019年诺贝尔化学奖授予锂离子电池的发明者,LiFePO4是锂离子电池的正极材料。用含锂废渣(主要金属元素的含量:Li 8.50%、Ni 6.55%、Mg 13.24%)制备Li2C2O4,并用其制备LiFePO4部分工艺流程如图(该流程可能造成水体砷污染):

已知:滤液1、滤液2中部分离子的浓度(g·L-1):
| Li+ | Ni2+ | Mg2+ |
| 滤液1 | 22.72 | 20.68 | 60.18 |
| 滤液2 | 21.94 | 7.7×10-3 | 0.78×10-3 |
I.制备Li2C2O4
(1)滤渣2的主要成分有__(填化学式)。
(2)Na2C2O4溶液中各离子的浓度由大到小顺序为__。
(3)写出加入Na2C2O4溶液时发生反应的离子方程式:__。
Ⅱ.制备LiFePO4
(4)将电池极Li2C2O4和FePO4置于高温下反应生成LiFePO4和一种温室气体,该反应的化学方程式是___。
(5)LiFePO4需要在高温下成型后才能作为电极,高温成型时要加入少量石墨,则石墨的作用是__(任写一点)。
(6)我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的As(Ⅴ),其机制模型如图,其中零价铁与过硫酸钠反应的离子方程式是__。在该模型中得到的铁砷共沉淀物经灼烧(无元素化合价变化)后得到一种磁性化合物,化学式为Fe7As2O14,该物质中二价铁与三价铁的个数比为__。
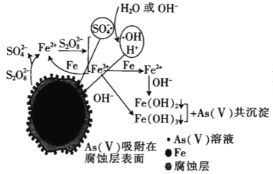
-
锂离子电池历经半个世纪岁月的考验,作出重大贡献的三位科学家被授予2019 年诺贝尔化学奖。磷酸亚铁锂( LiFePO4)是新型锂离子电池的正极材料。某小组拟设计以一种锂辉石(主要成分为Li2O· Al2O3·4SiO2,含少量铁、钙、镁)为原料制备纯净的碳酸锂,进而制备LiFePO4的工艺流程:
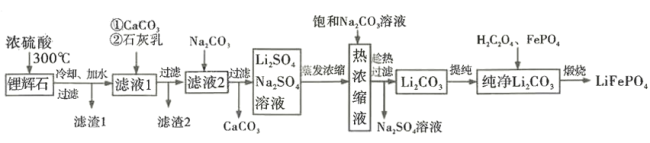
已知:LiO2·Al2O3·4SiO2+H2SO4(浓)  Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓
回答下列问题:
(1) LiFePO4含有锂、铁两种金属元素,它们焰色反应的颜色分别是_____________(填序号)。
A.紫红色、无焰色反应 B.黄色、无焰色反应
C.黄色、紫色 D.洋红色、黄绿色
(2)滤渣1的主要成分是_____________;向滤液1中加入适量的CaCO3细粉用于消耗硫酸并将Fe3+转化为红褐色沉淀,若 =3,反应的离子方程式为__________; 滤渣2的主要成分是Fe(OH)3、________、 CaSO4,其中 Fe(OH)3 脱水后可生成一种元素种类不变且摩尔质量为89 g·mol -1的新化合物,其化学式为_______________。
=3,反应的离子方程式为__________; 滤渣2的主要成分是Fe(OH)3、________、 CaSO4,其中 Fe(OH)3 脱水后可生成一种元素种类不变且摩尔质量为89 g·mol -1的新化合物,其化学式为_______________。
(3)已知碳酸锂在水中的溶解度随温度升高而减小,上述流程中趁热过滤的目的是________。
(4)煅烧制备LiFePO4时,反应的化学方程式为_____________________。
(5)某种以LiFePO4,作正极材料的锂电池总反应可表示为: LiFePO4+C Li1-xFePO4 +CLix。放电时正极的电极反应式为__________。
Li1-xFePO4 +CLix。放电时正极的电极反应式为__________。
-
2019年诺贝尔化学奖授予约翰·古德伊纳夫、斯坦利·惠廷厄姆和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。请回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为___,基态磷原子中,电子占据的最高能层符号为___;该能层能量最高的电子云在空间有___个伸展方向,原子轨道呈___形。
(2)[Co(NO3-)4]2-中Co2+的配位数为4,配体中N的杂化方式为__,该配离子中各元素的第一电离能由小到大的顺序为___(填元素符号),1mol该配离子中含σ键数目为___NA。
(3)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:

这类磷酸根离子的化学式可用通式表示为___(用n代表P原子数)。
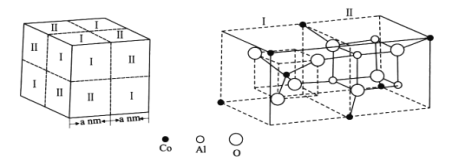
(4)钴蓝晶体结构如图,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___,晶体中Al3+占据O2-形成的___(填“四面体空隙”或“八面体空隙”)。NA为阿伏加德罗常数的值,钴蓝晶体的密度为___g·cm-3(列计算式)。
-
2019年诺贝尔化学奖授予约翰·古德伊纳夫、斯坦利·惠廷汉和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。请回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。
①基态Co原子核外电子排布式为_______________;
②基态磷原子中,电子占据的最高能层符号为______;该能层能量最高的电子云在空间有_____个伸展方向。
(2)[Co(NO3)4]2-的配体中N原子的杂化方式为____,该配离子中各元素的第一电离能由小到大的顺序为________(填元素符号),1mol该配离子中含σ键数目为_____NA。
(3)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
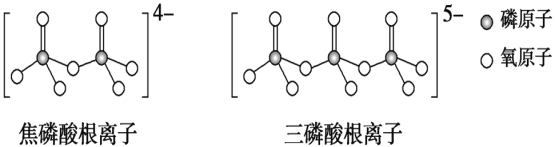
这类磷酸根离子的化学式可用通式表示为____________(用n代表P原子数)。
(4)①Li2O被广泛用作玻璃的组分,其熔点______Na2O(填高于或者低于),判断理由_____。
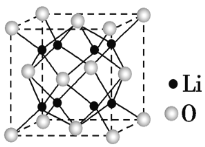
②Li2O具有反萤石结构,晶胞如图所示,已知其晶胞参数为0.4665nm,NA为阿伏加德罗常数的值,则Li2O的密度为___________g·cm-3(列出计算式)。
-
2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子电池的广泛应用要求处理电池废料以节约资源、保护环境。采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(由Al箔、LiFePO4活性材料、少量不溶于酸碱的导电剂组成)中的资源,部分流程如图:
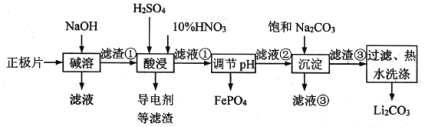
已知:Ksp(Li2CO3)=1.6×10-3。部分物质的溶解度(S)如表所示:
| T/℃ | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g | S(LiH2PO4)/g |
| 20 | 1.33 | 34.2 | 0.039 | 126 |
| 80 | 0.85 | 30.5 | —— | —— |
(1)将回收的废旧锂离子电池进行预放电、拆分破碎、热处理等预处理,筛分后获得正极片。下列分析你认为合理的是__________。
A.废旧锂离子电池在处理之前需要进行彻底放电,否则在后续处理中,残余的能量会集中释放,可能会造成安全隐患。
B.预放电时电池中的锂离子移向负极,不利于提高正极片中锂元素的回收率。
C.热处理过程可以除去废旧锂离子电池中的难溶有机物、碳粉等。
(2)写出碱溶时主要发生反应的离子方程式:________。
(3)为提高酸浸的浸出率,除粉碎、搅拌、升温外,还可采用的方法有______。(写出一种即可)
(4)酸浸时产生标况下3.36 L NO时,溶解LiFePO4________mol(其他杂质不与HNO3反应)。
(5)若滤液②中c(Li+)=4 mol·L-1,加入等体积的Na2CO3后,沉淀中的Li元素占原Li元素总量的90%,计算滤液③中c(CO32-)=__________mol/L。
(6)流程中用“热水洗涤”的原因是________。
(7)工业上将回收的Li2CO3、FePO4粉碎与足量炭黑混合高温灼烧再生制备LiFePO4,写出反应的化学方程式:_________。
-
2019年诺贝尔化学奖授予约翰·古迪纳夫、斯坦利·威廷汉和吉野彰,表彰他们对锂离子电池研究的贡献。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:
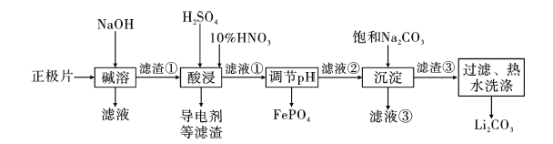
已知:KSP ( Li2CO3)=2.0×10-3 。部分物质的溶解度(S)如下表所示:
| T℃ | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g |
| 20 | 1.33 | 34.2 | 0.039 |
| 80 | 0.85 | 30.5 | —— |
| 100 | 0.72 | —— | |
(1) 流程中用“热水洗涤”的原因是____________。
(2)写出碱溶时Al箔溶解的化学方程式 ___________。
(3)酸浸时,用H2O2代替HNO3更好,其优点是________。
(4)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池放电时正极的电极反应式为____。
(5)若滤液②中c(Li+)=4mol/L,加入等体积的Na2CO3溶液后,Li+的沉降率达到90%,计算滤液③中c(CO32-)=____mol/L
-
2019年诺贝尔化学奖授予约翰·古迪纳夫、斯坦利·威廷汉和吉野彰,表彰他们对锂离子电池研究的贡献。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:
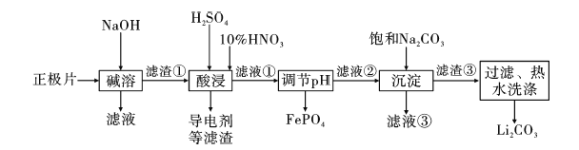
已知:Ksp ( Li2CO3)=1.6×10-3 。部分物质的溶解度(S)如下表所示:
| T℃ | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g |
| 20 | 1.33 | 34.2 | 0.039 |
| 80 | 0.85 | 30.5 | —— |
| 100 | 0.72 | —— | |
(1)从“正极”可以回收的金属有___。
(2)写出碱溶时Al箔溶解的离子方程式___。
(3)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池充电时正极的电极反应式为___。
(4)酸浸时产生标准状况下3.36LNO时,溶解 LiFePO4___mol(其他杂质不与HNO3反应),若用H2O2代替HNO3,发生反应的离子方程式为___。
(5)流程中用“热水洗涤”的原因是___。
(6)若滤液②中c(Li+)=4mol/L,加入等体积的Na2CO3后,Li+的沉降率到90%,计算滤液③中c(CO32-)=___mol/L。
(7)“沉淀”时___(填“能”或“不能”)用Na2SO4溶液代替饱和Na2CO3溶液,原因是___。















