-
配离子的稳定性可用K不稳衡量,例如Ag(NH3)2]+的K不稳= 。在一定温度下,向0.1 mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3⇌[Ag(NH3)2]+]。溶液中pNH3与δ(X)的关系如图。其中pNH3=-lg[c(NH3)]、δ(X)=
。在一定温度下,向0.1 mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3⇌[Ag(NH3)2]+]。溶液中pNH3与δ(X)的关系如图。其中pNH3=-lg[c(NH3)]、δ(X)= (X代表Ag+或Ag(NH3)2]+。下列说法不正确的是
(X代表Ag+或Ag(NH3)2]+。下列说法不正确的是
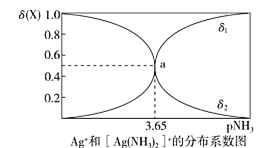
A.图中δ2代表的是δ([Ag(NH3)2]+]) B.向溶液中滴入稀硝酸,δ(Ag+)减小
C.该溶液中c(NH4+)+c(H+)=c(OH-) D.该温度时,K不稳([Ag(NH3)2]+)=10-7.3
-
配离子的稳定性可用K不稳衡量,例如[Ag(NH3)2]+的K不稳= 。在一定温度下,向0.1mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3
。在一定温度下,向0.1mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3 [Ag(NH3)2]+。溶液中pNH3与δ(X)的关系如图其中pNH3=-1g[c(NH3)]、δ(X)=
[Ag(NH3)2]+。溶液中pNH3与δ(X)的关系如图其中pNH3=-1g[c(NH3)]、δ(X)=  (X代表Ag+或[Ag(NH3)2]+)。下列说法正确的是
(X代表Ag+或[Ag(NH3)2]+)。下列说法正确的是
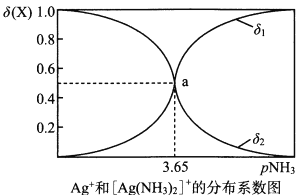
A. 图中δ1代表的是δ([Ag(NH3)2]+) B. 向溶液中滴入稀硝酸,δ(Ag+)减小
C. 该溶液中c(NH4+)+c(H+)=c(OH-) D. 该温度时,K不稳([Ag(NH3)2]+)=107.3
-
下列离子方程式书写正确的是
A.碳酸氢钾水【解析】
HCO3—+H2O  H3O++CO32—
H3O++CO32—
B.向硝酸银溶液中加入过量氨水:Ag++NH3·H2O=AgOH↓+NH4+
C.浓度均为0.1mol·L-1的氢氧化钡溶液与碳酸氢铵溶液等体积混合Ba2++2OH-+NH4++ HCO3—=BaCO3↓+NH3·H2O+H2O
D.向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3-
-
下列离子方程式书写正确的是( )
A.AgNO3溶液中加入过量氨水:Ag++NH3H2O═AgOH↓+NH4+
B.把0.4mol铁粉和0.8mol稀硝酸充分反应:Fe+4H++NO3-═Fe3++NO↑+2H2O
C.高锰酸钾与乙醇制备Mn3O4纳米粉体,同时生成乙醛:
6MnO4-+13CH3CH2OH→2Mn3O4+13CH3CHO+6OH-+10H2O
D.NH4HSO3溶液与足量NaOH溶液也混合:HSO3-+OH-═SO32-+H2O
-
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是

A.B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B.A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C.C点水电离的c(OH-)大于A点水电离的c(OH-)
D.A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
-
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是
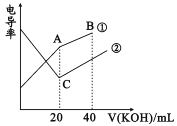
A.B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B.A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C.C点水电离的c(OH-)大于A点水电离的c(OH-)
D.A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
-
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是
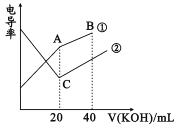
A.B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B.A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C.C点水电离的c(OH-)大于A点水电离的c(OH-)
D.A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
-
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是

A. B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B. A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C. C点水电离的c(OH-)大于A点水电离的c(OH-)
D. A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
-
已知难溶于水的盐在水中存在溶解平衡,例如氯化银在水中的溶解平衡为:
AgCl(s)  Ag+(aq) + Cl-(aq)。在一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp = [Ag+]·[Cl-] = 1.8 × 10-10 mol2·L-2
Ag+(aq) + Cl-(aq)。在一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp = [Ag+]·[Cl-] = 1.8 × 10-10 mol2·L-2
现把氯化银(足量)分别放人:①100mL蒸馏水中;②100mL 0.1mol·L-1的盐酸溶液中;③1000mL 0.1 mol·L-l的氯化铝溶液中;④100mL0.1 mol·L-1的氯化镁溶液中。充分搅拌后,相同温度下,银离子浓度由大到小的顺序是(用序号回答)________。在0.1mol·L-l氯化铝溶液中,银离子的物质的量浓度最大可达到________mol·L-1。
-
难溶化合物的饱和溶液存在溶解平衡,例如:AgCl(s) Ag++Cl-,Ag2CrO4(s)
Ag++Cl-,Ag2CrO4(s) 2Ag++
2Ag++ ,在一定温度下,其离子浓度乘积为常数,这一常数叫溶度积常数,用Ksp表示,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(
,在一定温度下,其离子浓度乘积为常数,这一常数叫溶度积常数,用Ksp表示,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c( )=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算完成下列问题:
)=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算完成下列问题:
(1)Cl-、 谁先沉淀?
谁先沉淀?
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-浓度是多少?(设混合溶液在反应中体积不变)
。在一定温度下,向0.1 mol/L硝酸银溶液中滴入稀氨水,发生反应Ag++2NH3⇌[Ag(NH3)2]+]。溶液中pNH3与δ(X)的关系如图。其中pNH3=-lg[c(NH3)]、δ(X)=
(X代表Ag+或Ag(NH3)2]+。下列说法不正确的是





