-
(背景材料)氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200℃.导热性好,热膨胀系数小,是良好的耐热冲击材料.抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料.氮化铝还是电绝缘体,介电性能良好,用作电器元件也很有希望.超细氮化铝粉末被广泛应用于大规模集成电路生产领域.其制取原理为:
Al2O3+3C+N2  2AlN+3CO
2AlN+3CO
(问题探究)某化学研究性学习小组成员根据氮化铝的制取原理,进行了如下探究.
问题1、在制取氮化铝时由于反应不完全,氮化铝产品中所含杂质除了碳以外还可能存在________.
问题2、为测定该产品中有关成分的含量,甲、乙两同学设计了以下两个实验:
(1)甲同学:称取10.00g样品,将其加入过量的氢氧化钠溶液中共热并蒸干,AlN跟氢氧化钠溶液反应生成NaAlO2,并放出氨气3.36L(标准状况).
①上述反应的化学方程式为________.
②该样品中的AlN的质量分数为________.
(2)乙同学:称取10.00g样品置于反应器中,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g•L-1(已折成标准状况,AlN不跟O2反应).该样品中含杂质碳________g.
问题3、丙同学受到甲、乙同学实验的启发,认为测定某氮化铝中含有碳或氧化铝杂质,可用图中I的一些装置来进行检验,根据AlN与NaOH溶液反应所生成氨气的体积来测定样品中氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)
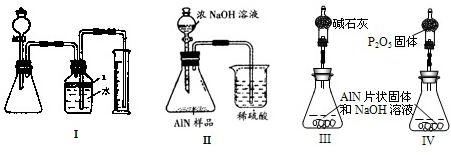
(1)实验有关操作为:①往锥形瓶中放入适量的AlN样品:②从分液漏斗往锥形瓶中加入过量的浓NaOH;③检验装置的气密性;④测定收集到水的体积.
正确的操作顺序为________.
(2)本试验中检查装置气密性的方法是________.
(3)广口瓶中的试剂X可最好选用________(填选项的标号).
A、苯 B、酒精 C、植物油 D、CCl4
(4)广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将________(填偏大、偏小或不变).
(5)若实验中测得样品的质量为wg,氨气的体积为aL(标况下),则样品中AlN的质量分数为________(AlN的式量为41).
(6)实验结束后,若观察到锥形瓶中还有固体,则样品中含有的杂质是________,为了测定是否含有其它杂质,则还需要哪些简单数据________.
问题4、丁同学认为,丙同学的实验方法,可能因气体体积测量不准,导致误差较大.建议改用图9中的Ⅱ装置进行同样实验,通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数.你认为是否可行?________(填入“可行”、“不可行”),原因是________.最简单的改进方法为________.
问题5、戊同学仔细思考了丁同学的装置后,认为此装置所测测得的样品中AlN含量偏小.其原因是________.若忽略此原因的话,只要用图9中的III或IV两个装置中的一种,只需进行简单而又必要的数据测定,可比较准确地确定样品中AlN的质量分数.较合理的装置为________(填代号).你认为戊同学的装置是否还有缺陷?________.若有,所测结果将偏高或偏低________,应作如何改进?________.(若无缺陷后两此格可不填).
-
氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200℃.导热性好,热膨胀系数小,是良好的耐热冲击材料.抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料.制取原理为:Al2O3 + 3C + N2 2AlN + 3CO
2AlN + 3CO
(1)氮化铝的晶体类型为___________。
(2)制取氮化铝要用较为纯净的N2,N2的电子式为____________。实验室中制备少量氮气
的基本原理是:NH4Cl + NaNO2 =NaCl + 2H2O + N2↑。为了得到较纯净的N2,最好的收集方法是____________。
(3)氮化铝抗酸能力极强,但抗碱蚀能力差,它能与氢氧化钠溶液反应生成NaAlO2和能使湿润红色石蕊试纸变蓝的气体,其化学反应方程式为:___________________
(4)工业上制得的AlN中含有Al2O3 、C杂质,取含杂质的粗氮化铝10.00g于某容器,加入足量浓硫酸,加热,收集到672mL气体(已折算成标准状况)。则该粗氮化铝中碳的质量分 数为___________
数为___________
-
(16分)氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200°C,导热性好,热膨胀系数小,是良好的耐热冲击材料。抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料。工业用氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。现要通过实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理
①已知Al4C3与硫酸反应可生成CH4,则该反应的离子方程式是______________。
②AlN溶于强酸生成铵盐,溶于氢氧化钠溶液生成氨气,请写出AlN与NaOH溶液反应的化学方程式___________。
(2)实验装置(如下图所示)

(3)实验过程
①连接实验装置,检验装置的气密性。称得D装置的质量为yg,滴定管的读数为amL。
②称取xgAlN样品置于锥形瓶中;塞好胶塞,关闭活塞K2、K3,打开活塞K1,通过分液漏斗加入过量____(填化学式),与锥形瓶内物质充分反应。
③待反应进行完全后,关闭活塞K1,打开活塞K3,通过分液漏斗加入过量 _______(填化学式),与锥形瓶内物质充分反应。
④打开K2,通过打气装置通入空气一段时间。
⑤记录滴定管的读数为bmL,称得D装置的质量为zg。
(4)数据处理与问答
①在上述装置中,设置活塞K2的目的是__________。
②若读取滴定管中气体的体积时,液面左高右低,则所测气体的体积_________(填“偏大”,“偏小”或“无影响”)。
③Al4C3的质量分数为 ____,AlN的质量分数为_______。
-
(16分)氮化铝(AlN)陶瓷是一种类金刚石氮化物的新型无机非金属材料,最高可稳定到2200°C,导热性好,热膨胀系数小,是良好的耐热冲击材料。抗熔融金属侵蚀的能力强,是熔铸纯铁、铝或铝合金理想的坩埚材料。工业用氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。现要通过实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理
①已知Al4C3与硫酸反应可生成CH4,则该反应的离子方程式是______________。
②AlN溶于强酸生成铵盐,溶于氢氧化钠溶液生成氨气,请写出AlN与NaOH溶液反应的化学方程式___________。
(2)实验装置(如下图所示)

(3)实验过程
①连接实验装置,检验装置的气密性。称得D装置的质量为yg,滴定管的读数为amL。
②称取xgAlN样品置于锥形瓶中;塞好胶塞,关闭活塞K2、K3,打开活塞K1,通过分液漏斗加入过量____(填化学式),与锥形瓶内物质充分反应。
③待反应进行完全后,关闭活塞K1,打开活塞K3,通过分液漏斗加入过量 _______(填化学式),与锥形瓶内物质充分反应。
④打开K2,通过打气装置通入空气一段时间。
⑤记录滴定管的读数为bmL,称得D装置的质量为zg。
(4)数据处理与问答
①在上述装置中,设置活塞K2的目的是__________。
②若读取滴定管中气体的体积时,液面左高右低,则所测气体的体积_________(填“偏大”,“偏小”或“无影响”)。
③Al4C3的质量分数为 ____,AlN的质量分数为_______。
-
氮化铝(AlN)陶瓷是一种新型无机非金属材料, 最高可稳定到2473K, 导热性好、热膨胀系数小,是良好的耐热冲击材料。制取原理为:Al2O3+3C+N2 2A1N+3CO,回答下列问题:
2A1N+3CO,回答下列问题:
(1)氮化铝的晶体类型为________。在上述化学方程式中第二周期元素的第一电离能由小到大的顺序是______。
(2)基态氧原子电子占据最高能级的原子轨道的形状是________,未成对电子数为________。
(3)等电子体具有相似的结构。CO与N2互为等电子体,CO分子中σ键与π键数目之比为_______。
(4)Cu2+处于:[Cu(NH3)4]2+的中心,若将配离子[Cu(NH3)4]2+中的2个NH3换为CN-,则有2种结构,则Cu2+是否为sp3杂化________(填“是”或“否”)理由为_________。
(5)AlN晶体结构如图所示,1个Al原子周围距离最近的Al原子数为______个;若晶胞结构的高为a nm, 底边长为b nm,NA表示阿伏伽德罗常数的值,则其密度为_______g.cm-3(列出计算式)。
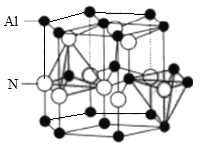
-
氮化铝(AlN)陶瓷是一种新型无机非金属材料,利用它较高的体积电阻率、绝缘强度大、导热性能好,可用作大功率半导体器件的绝缘基片、大规模和超大规模集成电路的散热基片和封装基片。工业上可用氮气和铝在高温下直接化合法来制备氮化铝粉体(AlN粉体在潮湿的空气中易发生水解反应)。已知:实验室可用饱和亚硝酸钠(NaNO2)溶液和氯化铵溶液共热制取氮气。现提供以下装置来模拟工业制取AlN粉体。
(1)写出实验室制取氮气的化学方程式:___________________________。
(2)请从下图中选择合适的装置按顺序组装一套用氮气和铝粉制AlN的装置(装置可以根据需要重复使用):________________________________。
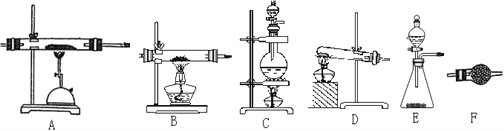
(3)实验开始后应先给_______处装置加热一段时间再给另一处装置加热,这样操作的原因是:_______________。
(4)已知:氮化铝(AlN)既能溶于强酸,又能溶于强碱,试写出AlN与HCl溶液反应的化学方程为________________。
(5)AlN制备过程中存在一些副反应致生成的AlN不纯。 研究小组的同学取2.0500 g AlN样品与浓NaOH溶液充分反应,通过测定产生氨气的量来测定AlN的纯度(假设杂质与碱反应不生成NH3,忽略NH3在强碱性溶液中的溶解)。实验装置如下:请帮该同学纠正装置中一处明显错误:___________________。当H中反应完全后持续缓慢通入氮气将生成的氨全部吹入I中被水吸收。然后将I中氨水_________________________________________________________________________(请补充完这步操作,需根据后面数据计算作答),用_______取25.00mL氨水于锥形瓶中并加入几滴_______作指示剂,用0.1000mol/L的盐酸滴定至终点,消耗盐酸体积为22.50mL,经计算得AlN的纯度为90.00 %。
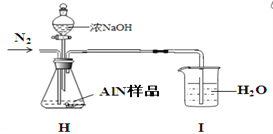
-
氮化铝(AlN)是一种新型无机材料,广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C 2AlN+3CO合成。已知AlN可与NaOH溶液反应放出有刺激性气味的气体。下列叙述正确的是
2AlN+3CO合成。已知AlN可与NaOH溶液反应放出有刺激性气味的气体。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1molAlN需转移6mol电子
C.AlN属于离子化合物,其中氮元素的化合价为+3
D.AlN与NaOH溶液反应的化学方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑
-
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3 + N2 + 3C 高温 2 AlN + 3CO ,下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为—3
D.氮化铝晶体属于分子晶体
-
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质, 被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3 + N2 + 3 C 高温 2 AlN + 3 CO 下列叙述正确的是
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为—3
D.氮化铝晶体属于分子晶体
-
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3+ N2+ 3 C 2 AlN + 3 CO 下列叙述正确的是 ( )
2 AlN + 3 CO 下列叙述正确的是 ( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为-3
D.氮化铝晶体属于分子晶体
2A1N+3CO,回答下列问题:





