-
某同学在实验室制备SO2并对SO2的性质进行了探究。回答下列问题:
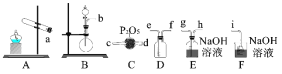
(1)制备SO2
①实验室中通常用亚硫酸钠与浓硫酸反应制备SO2气体。二氧化硫的发生装置可以选择上图中的_______,反应的化学方程式为____________。
②欲收集一瓶干燥的二氧化硫,选择上图中的装置,其连接顺序为:发生装置→_____________(按气流方向,用小写字母表示)。
(2)探究SO2的性质,用下图所示装置进行实验。

①实验过程中观察到装置A、B有如下现象:A中无变化,B中红色褪去。由此得出的实验结论是___________________。
②装置C、D中发生的现象分别是______________________、_____________________,这些现象分别说明SO2具有的性质是___________和__________;装置D中发生反应的离子方程式为_____________。
③装置E中含酚酞的NaOH溶液逐渐褪色,此实验现象有两种解释:一是由于SO2有漂白性;二是由于SO2溶于水后显酸性。请设计实验加以验证:___________。
-
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂(易被氧化),某研究性学习小组为了制备少量Na2S2O5,并探究SO2 的某些性质,设计下图所示装置(夹持装置已略去)。请回答下列问题:
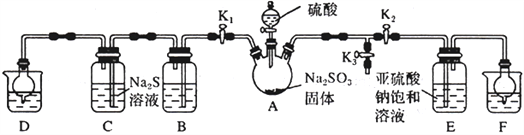
(1)向A 中滴加的硫酸最好选用__________________(填字母)。
A.98%的浓硫酸 B.70%的硫酸 C.10%的稀硫酸
(2)打开分液漏斗旋塞,发现其中的液体不能流下,应采取的操作是__________________________。
(3)关闭K1、K3,打开K2。一段时间后E 中有Na2S2O5晶体析出,装置E 中发生反应的化学方程式为__________________________。
(4)关闭K2、K3,打开K1,若探究SO2的漂白性,装置B应盛有__________溶液;若探究SO2的还原性,B 中发生反应的离子方程式可以是_____________________________________;观察到装置C 中发生的现象是__________________________。
(5)装置D和F 的作用为__________________________。
(6)设计实验验证Na2S2O5晶体在空气中已被氧化:__________________________。
(7)请指出该设计的缺陷:__________________________。
-
SO2是一种酸性氧化物,溶于水生成亚硫酸。某同学对SO2的氧化性和亚硫酸的酸性进行了探究。回答下列问題:
(一)SO2的制备
该同学制备SO2的实验装置如下:
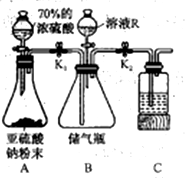
(1)装置A中发生反应的化学方程式为__________________________________________。
(2)装置C中盛有的是NaOH溶液,其作用是_________________________。
(二)验证SO2氧化性
待装置B中收集满SO2后,夹紧止水夹K1和K2取下装置 B,利用收集到的SO2验证其氧化性。
(3)设计一种验证SO2具有氧化性的方法:__________________________________________(要体现所使用检验试剂的名称和实验现象等要点)。
(4)将溶液R(足量)加人装置B的储气瓶中可将SO2排出进入检验试剂中,则溶液R是________。
(三)探究H2SO3的酸性强于HClO
由于次氯酸盐具有较强的氧化性,故不能直接将SO2通入次氯酸盐中检验H2SO3的酸性强于HClO,该同学用装置B中收集到的SO2,利用下面装置间接地完成了验证。
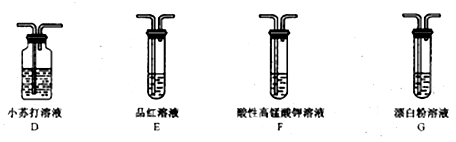
(5)装置的连接顺序为B→______________,F的作用是______________________________。
(6)可证明H2SO3的酸性强于HClO的实验现象是___________________________。
-
焦亚硫酸钠(Na2S2O5)是一种常用的食品抗氧化剂(易被氧化)。实验室利用如图所示装置制取少量焦亚硫 酸钠,并探究 SO2 的性质 (夹持装置已略去)。

请回答下列问题:(实验前已除去装置中的空气)
(1)仪器 a 的名称是_____。
(2)关闭 K2、K3,打开 K1,装置 B 中发生反应的离子方程式为_________,观察到装 置 C 中发生的现象是_____。
(3)装置 D 和 F 的作用是____。
(4)实验前,E 中所用蒸馏水需经煮沸后迅速冷却,目的是_____, 关闭 K1、K3,打开 K2,一段时间后 E 中有 Na2S2O5 晶体析出,装置 E 中发生反应的化学方程式为__________________。
(5)设计实验验证 Na2S2O5 晶体在空气中已被氧化,所需试剂为_____。
(6)在测定某葡萄酒中Na2S2O5 残留量时,取 40.00 mL 葡萄酒样品,加入指示剂,用 0.01000 mol·L−1 的碘标准液滴 定,当溶液_________,即为终点。测定实验中,消耗碘标准液 10.00 mL,该样品中Na2S2O5的残留量为_____g·L−1(以 SO2 计)。
-
某同学对SO2和亚硫酸的性质进行了探究。回答下列问题:
I.探究SO2性质
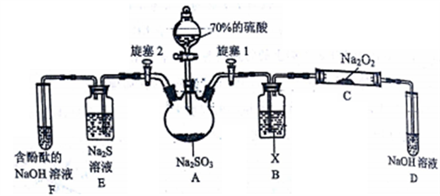
(1)关闭旋塞2,打开旋塞1,注入硫酸至浸没三颈烧瓶中固体,检验SO2与Na2O2 反应是否有氧气生成的方法是______________________________。
(2)装置B中试剂X是____________,实验结束后D溶液中的阴离子可能是_______________。
(3)设计实验检验C中固体产物的阴离子:___________________________ (简要描述操作步骤、实验现象、结论)。
(4)关闭旋塞1后,打开旋塞2,E用于验证SO2的____性,F中的现象是_______________。
II.探究H2SO3的酸性强于HC1O。
请你利用下面装置达成实验目的。
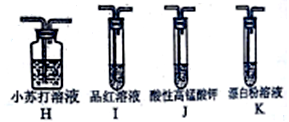
(5)装置的连接顺序为:
纯净SO2→__________(选填字母),K中反应的离子方程式是_________________________。
(6)可证明H2SO3的酸性强于HC1O的实验现象是_________________________。
-
(10分) 某同学用如图所示装置探究SO2的性质及其有关实验.
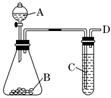
(1)实验室用亚硫酸钠固体和一定浓度的硫酸反应制备SO2气体,写出该反应的化学方程式______________________________________________________________
(2)分别将SO2气体通入下列C溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是______________,继续通入过量SO2气体,现象是________________.
②SO2通入紫色KMnO4溶液,现象是______________,其反应的离子方程式为_______________________.
③过量SO2慢慢地通入澄清石灰水中,现象___________________________________
④若C为双氧水,则通入SO2后,请大胆判断所得溶液是________(填溶质的化学式),若该同学制备的SO2气体中混有CO2气体,产生杂质的原因可能是亚硫酸钠固体中混有__________.
-
[实验化学]
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。
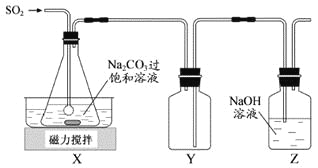
当溶液pH约为4时,停止反应,在20℃左右静置结晶。生成Na2S2O5的化学方程式为
2NaHSO3===Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为_________________。
(2)装置Y的作用是______________________________。
(3)析出固体的反应液经减压抽滤、洗涤、25℃~30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、________________和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体。用饱和SO2水溶液洗涤的目的是______。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是______。
-
[实验化学]
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。
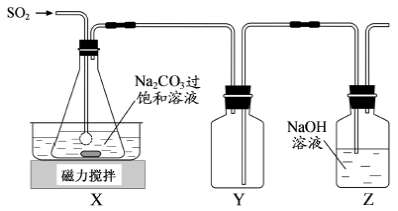
当溶液pH约为4时,停止反应,在20℃左右静置结晶。生成Na2S2O5的化学方程式为2NaHSO3===Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为____________________。
(2)装置Y的作用是______________________________。
(3)析出固体的反应液经减压抽滤、洗涤、25℃~30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、________________和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体。用饱和SO2水溶液洗涤的目的是______。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是______。
-
[实验化学]
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。

当溶液pH约为4时,停止反应,在20℃左右静置结晶。生成Na2S2O5的化学方程式为
2NaHSO3===Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为____________________。
(2)装置Y的作用是______________________________。
(3)析出固体的反应液经减压抽滤、洗涤、25℃~30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、________________和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体。用饱和SO2水溶液洗涤的目的是______。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是______。
-
[实验化学]
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。
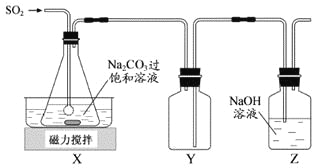
当溶液pH约为4时,停止反应,在20℃左右静置结晶。生成Na2S2O5的化学方程式为
2NaHSO3===Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为____________________。
(2)装置Y的作用是______________________________。
(3)析出固体的反应液经减压抽滤、洗涤、25℃~30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、________________和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体。用饱和SO2水溶液洗涤的目的是______。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是______。












