-
氯化亚铜( )在化工、印染、电镀等行业应用广泛。
)在化工、印染、电镀等行业应用广泛。 微溶于水,不溶于醇和稀酸,可溶于
微溶于水,不溶于醇和稀酸,可溶于 浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量
浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量 )为原料,采用硝酸铵氧化分解技术生产
)为原料,采用硝酸铵氧化分解技术生产 的工艺过程如图。回答下列问题:
的工艺过程如图。回答下列问题:
(1)步骤①中N元素被还原为最低价,写出此反应的离子方程式______________。
(2)步骤②中,亚硫酸铵要略保持过量,原因是___________,滤液中可循环利用的物质是__________。
(3)步骤⑤中,用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为 被氧化为
被氧化为 的化学方程式为______________________。
的化学方程式为______________________。
(4)用 溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品
溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品 ,将其置于过量的
,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸配成
溶液中,待样品完全溶解后,加入适量稀硫酸配成 溶液,取溶液
溶液,取溶液 用
用 溶液进行滴定,反应中
溶液进行滴定,反应中 被还原成
被还原成 ,相关数据记录如表所示:该样品中
,相关数据记录如表所示:该样品中 的质量分数__________________。
的质量分数__________________。
| 实验编号 | 1 | 2 | 3 |
| 消耗 溶液的体积/mL 溶液的体积/mL | 14.98 | 16.03 | 15.02 |
(5)制造印刷电路板产生的废液中含大量 等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到
等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到 ,电解时阴极的电极反应式为___________,生成
,电解时阴极的电极反应式为___________,生成 的离子方程式为________________________________。
的离子方程式为________________________________。
-
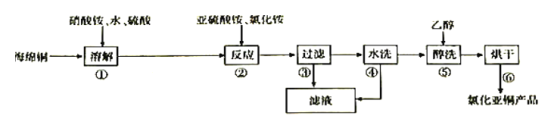
氯化亚铜(CuC1)在化工、印染、电镀等行业应用广泛。CuCl微溶于水,不溶于醇和稀酸,可溶于Cl-浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuC1的工艺过程如图所示:

回答下列问题:
(1)步骤①中N元素被还原为最低价,写出此反应的离子方程式___________。
(2)步骤②中,亚硫酸铵要略保持过量,原因是___________,滤液中可循环利用的物质是___________。
(3)步骤⑤中,醇洗的目的是______________________。
(4)常用K2Cr2O7溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品10.00g,将其置于过量的FeCl2溶液中,待样品完全溶解后,加入适量稀硫酸配成100mL溶液,取溶液10.00mL用0.1000mol·L K2Cr2O7溶液进行滴定,反应中Cr2O72-被还原成Cr3+,相关数据记录如下表所示:
| 实验编号 | 1 | 2 | 3 |
| 消耗K2Cr2O7溶液的体积/mL | 14.98 | 16.03 | 15.02 |
该样品中CuCl的质量分数___________。(保留4位有效数字)
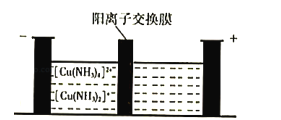
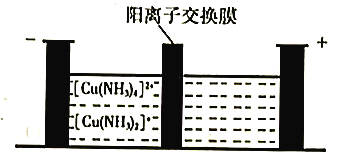
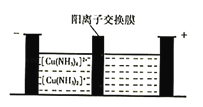
(5)制造印刷电路板产生的废液中含大量[Cu(NH3)4]2+等离子,利用膜电解技术对此废液进行电解,电解装置如下图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到CuCl,电解时阴极的电极反应式为___________,生成CuCl的离子方程式为______________________。
-
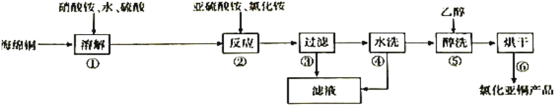
氯化亚铜(CuC1)在化工、印染、电镀等行业应用广泛。CuCl微溶于水,不溶于醇和稀酸,可溶于Cl-浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuC1的工艺过程如图。回答下列问题:
(1)步骤①中N元素被还原为最低价,写出此反应的离子方程式____。
(2)步骤②中,亚硫酸铵要略保持过量,原因是____,滤液中可循环利用的物质是____。
(3)步骤⑤中,用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3C1的化学方程式为__。
(4)用K2Cr2O7溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品10.00g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸配成100mL溶液,取溶液10.00mL用0.1000mol•LK2Cr2O7溶液进行滴定,反应中Cr2O72﹣被还原成Cr3+,相关数据记录如表所示:该样品中CuCl的质量分数____。
| 实验编号 | 1 | 2 | 3 |
| 消耗K2Cr2O7溶液的体积/mL | 14.98 | 16.03 | 15.02 |
(5)制造印刷电路板产生的废液中含大量[Cu(NH3)4]2+等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到CuCl,电解时阴极的电极反应式为__,生成CuCl的离子方程式为______。
-
[化学——选修2:化学与技术](14分)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系, 在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

回答下列问题:
(1)步骤①中得到的氧化产物是 。溶解温度应控制在60~70℃,原因是 。
(2)写出步骤③中主要反应的离子方程式 。
(3)步骤⑤包括用pH = 2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是 。
(5)步骤②、④、⑤、⑧都要进行固液分离。工业上常用的固液分离设备有 (填字母)。
A.分馏塔 8.离心机 C.反应釜 D.框式压滤机
(6)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液b mL,反应中Cr2O72-被还原为Cr3+。样品中CuCl的质量分数为 。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业.CuCl 难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu 和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl 的工艺过程如下:
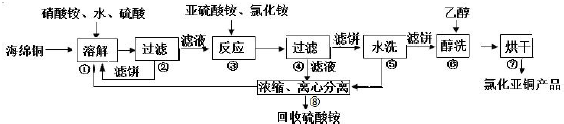
回答下列问题:
(1)步骤①中真正的氧化剂是___________,溶解温度应控制在60-70 度,原因是___________;
(2)写出步骤③中主要反应的离子方程式是___________;
(3)步骤⑧是分离滤液和洗涤液操作,实验室里混有杂质NaCl 的(NH4)2SO4 固体提纯的方法是___________;
(4)上述工艺中,步骤⑥不能省略,理由是___________;
(5)步骤②、④、⑤、⑧都要进行固液分离.工业上常用的固液分离设备有___________(填字母).
A、离心机B、分馏塔C、框式压滤机D、反应釜
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3 溶液中,待样品完全溶解后,加入适量稀硫酸,用a mol/L 的K2Cr2O7 溶液滴定到终点,消耗K2Cr2O7 溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl 的质量分数为___________。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
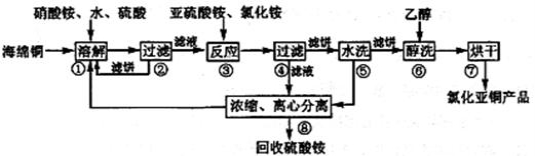
回答下列问题:
(1)写出“溶解”过程中发生的氧化还原反应的离子方程式(N元素被还原到最低价):_______,溶解温度应控制在60-70℃,原因是_______。
(2)写出步骤③中,氧化剂与还原剂的物质的量之比为________。已知NH4Cl、Cu2+的物质的量之比[n(NH4Cl)/n(Cu2+)]与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定程度后的氯化亚铜的沉淀率减少,其可能的原因是__________。

(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_____(写名称),回收的主要物质是____(写化学式)
(4)上述工艺中,步骤⑥醇洗的作用是__________。
(5)称取2.000g CuCl样品(杂质不参与反应),溶于一定量的0.5000mol/L FeCl3溶液中,加水稀释至200mL得到溶于,取20.00mL用0.1000mol/L的Ce(SO4)2溶液滴定到终点,消耗20.00mL Ce(SO4)2
有关反应式:Fe3++CuCl═Fe2++Cu2++Cl﹣ Ce4++Fe2+═Fe3++Ce3+
则样品中CuCl的质量分数_________。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

回答下列问题:
(1)步骤①中氧化还原反应的离子方程式为__________,溶解温度应控制在60~70℃,原因是______。
(2)写出步骤③中主要反应的离子方程式__________。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是__________。
(5)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amoI/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+。样品中CuCl的质量分数为________。
-
(共14分)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

回答下列问题:
(1)步骤①中得到的氧化产物是_________,溶解温度应控制在60~ 70℃,原因是________ 。
(2)写出步骤③中主要反应的离子方程式___________。若向亚硫酸氢铵溶液中加入过量氢氧化钠溶液,反应的离子方程式为 。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是________ _。
(5)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

回答下列问题:
(1)步骤①中得到的氧化产物是_______(填离子符号),溶解温度应控制在60~70℃,原因是________。
(2)写出步骤③中主要反应的离子方程式___________。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是_____________。
(5)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________。
-
【化学-选修2:化学与技术】
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料采用硝酸铵氧化分解技术生产CuC1的工艺过程如下:
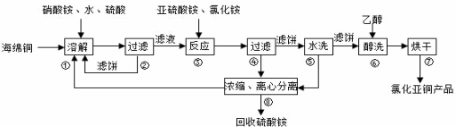
回答下列问题:
(1)步骤①中得到的氧化产物是___________,溶解温度应控制在60-70℃,原因是___________;
(2)写出步骤③中主要反应的离子方程式_________________;
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是_________________;
(5)步骤②、④、⑤、⑧都要进行固液分离.工业上常用的固液分离设备有_______(填字母)
A、分馏塔 B、离心机 C、反应釜 D、框式压滤机
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为___________。
)在化工、印染、电镀等行业应用广泛。
微溶于水,不溶于醇和稀酸,可溶于
浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量
)为原料,采用硝酸铵氧化分解技术生产
的工艺过程如图。回答下列问题:

被氧化为
的化学方程式为______________________。
溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品
,将其置于过量的
溶液中,待样品完全溶解后,加入适量稀硫酸配成
溶液,取溶液
用
溶液进行滴定,反应中
被还原成
,相关数据记录如表所示:该样品中
的质量分数__________________。
等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到
,电解时阴极的电极反应式为___________,生成
的离子方程式为________________________________。












