-
(1)H2S分子中H-S键的键角为92°,说明H2S分子是_____(选填“极性”“非极性”)分子。可用FeS与稀硫酸制取 H2S气体,而CuS不溶于稀硫酸,请据此比较FeS、H2S、CuS这三种物质电离或溶解出S2-的能力__________________。实验室制取并收集H2S气体,除FeS和稀硫酸外,还必需的试剂是___________。
(2)在NaOH和NaClO混合溶液中,多硫化钠(Na2SX)会被氧化为Na2SO4,此时1molNa2SX失去的电子数为_________mol;若Na2SX与NaClO反应的物质的量之比为1:10,则 x = ______。
(3)往Na2S和Na2S2O3混合溶液中加入稀硫酸,指出反应现象_____________________________。
(4)已知25℃:H2S Ki1 = 9.1×10-8 Ki2 = 1.1×10-12 ;H2SO3 Ki1 = 1.5×10-2 Ki2 = 1.0×10-7
将amolSO2通入含bmolNa2S的溶液中完全反应,若没有硫化氢气体产生,则a:b的值为______。
高三化学综合题中等难度题查看答案及解析
-
下列有关说法不正确的是( )
A.要清洗附着在试管壁上的硫,可用的试剂是CS2
B.硫化亚铁溶于稀硝酸中反应的离子方程式为:FeS+2H+=Fe2++H2S↑
C.常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮运浓硫酸
D.在Na2SO3和BaCO3混合物中加入过量的稀硫酸,能产生气泡并有沉淀生成
高三化学选择题中等难度题查看答案及解析
-
某学习小组设计实验探究H2S的性质,装置如图所示。下列说法正确的是( )
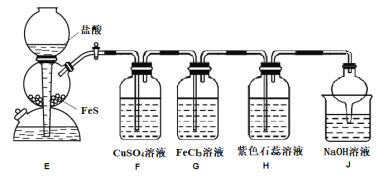
A.若E中FeS换成Na2S,该装置也可达到相同的目的
B.若F中产生黑色沉淀,说明硫酸的酸性比氢硫酸强
C.若G中产生浅黄色沉淀,说明H2S的还原性比Fe2+强
D.若H中溶液变红色,说明氢硫酸是二元弱酸
高三化学单选题简单题查看答案及解析
-
FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应时生成H2S2,H2S2易分解。实验室用稀硫酸与FeS2颗粒混合,则反应完毕后不可能生成的物质是
A.H2S B.S C.FeS D.FeSO4
高三化学选择题中等难度题查看答案及解析
-
FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应时生成H2S2,H2S2易分解。实验室用稀硫酸与FeS2颗粒混合,则反应完毕后不可能生成的物质是
A.H2S B.S C.FeS D.FeSO4
高三化学选择题中等难度题查看答案及解析
-
硫化氢(
)分子中,两个H—S键的夹角接近90°,说明
分子的空间构型为________;二氧化碳(
)分子中,两个C=O键的夹角是180°,说明
分子的空间构型为________;甲烷(
)分子中,两个相邻C—H键的夹角是109°28′,说明CH4分子的空间构型为________。
空格处是横线
高三化学填空题中等难度题查看答案及解析
-
工业上用含80% FeS2的硫铁矿制取硫代硫酸钠,涉及到的化学反应如下(杂质不与O2、盐酸反应):
4FeS2+11O2
2Fe2O3+8SO2 ①
FeS2+2HCl→ FeCl2+H2S↑+S↓ ②
2H2S+SO2→ 3S+2H2O ③
2NaOH+SO2→Na2SO3 +H2O ④
Na2SO3+S
Na2S2O3 ⑤
通过分析上述反应,进行计算:
(1)若在某密闭容器中加入150 g上述硫铁矿,并通入10 mol含氧气体积分数为0.4的富氧空气,按反应①充分反应后得到的气体中SO2的体积分数为__________(计算结果保留3位小数)。
(2)若以上各步反应的转化率均为100%,则150 g上述硫铁矿理论上最多可制得Na2S2O3___ g。
(3)若NaOH溶液吸收SO2的吸收率为90%,其它反应的转化率均为100%,则150 g上述硫铁矿最多可制得Na2S2O3多少g(写出计算过程,计算结果保留1位小数)?
(4)若反应②、④的转化率为90%,其它反应的转化率均为100%,要制得Na2S2O3最多,则原料中FeS2在反应①和②中的理论质量配比为多少(写出计算过程,计算结果保留3位小数)?
高三化学计算题困难题查看答案及解析
-
下列化学方程式或离子方程式正确的是( )
A.FeS加入稀硫酸溶液中:FeS+2H+===Fe2++H2S↑
B.Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++HCO3-+OH-===CaCO3↓+H2O
C.铜片跟浓硝酸反应:3Cu+2NO3-+8H+===3Cu2++2NO↑+4H2O
D.酸性KMnO4溶液中滴加H2O2:2MnO4-+H2O2+6H+===2Mn2++3O2↑+4H2O
高三化学选择题困难题查看答案及解析
-
能正确表示下列化学反应的离子方程式的是()
A. Fe2(SO4)3溶液和H2S反应的离子方程式:2Fe3++H2S==FeS+2H+
B. 双氧水中加入稀硫酸和KI溶液:2I-+H2O2+2H+==I2+O2↑+2H2O
C. 硫酸氢铵溶液和过量的氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D. 草酸使酸性KMnO4溶液褪色:5H2C2O4+2MnO4—+6H+==2Mn2++10CO2↑+8H2O
高三化学单选题中等难度题查看答案及解析
-
能正确表达下列反应的离子方程式为( )
A. 用稀盐酸除去水垢:2H++CaCO3===Ca2++CO2↑+H2O
B. 硫化亚铁与浓硫酸混合加热:2H++FeS===H2S↑+Fe2+
C. 向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3CO32-===Al2(CO3)3↓
D. Na2O2溶于水产生O2∶Na2O2+H2O===2Na++2OH-+O2↑
高三化学单选题中等难度题查看答案及解析