常温下,向某浓度的二元弱酸H2C2O4溶液中逐滴加入NaOH溶液,pC与溶液pH的变化关系如图所示(pC=-lgx,x表示溶液中溶质微粒的物质的量浓度)。下列说法正确的是
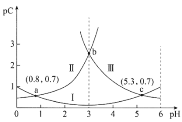
A.常温下,H2C2O4的Ka1=100.8
B.pH=3时,溶液中
C.pH由0.8增大到5.3的过程中,水的电离程度逐渐增大
D.常温下,随着pH的增大,的值先增大后减小
高三化学单选题困难题
常温下,向某浓度的二元弱酸H2C2O4溶液中逐滴加入NaOH溶液,pC与溶液pH的变化关系如图所示(pC=-lgx,x表示溶液中溶质微粒的物质的量浓度)。下列说法正确的是

A.常温下,H2C2O4的Ka1=100.8
B.pH=3时,溶液中
C.pH由0.8增大到5.3的过程中,水的电离程度逐渐增大
D.常温下,随着pH的增大,的值先增大后减小
高三化学单选题困难题
常温下,向某浓度的二元弱酸H2C2O4溶液中逐滴加入NaOH溶液,pC与溶液pH的变化关系如图所示(pC=-lgx,x表示溶液中溶质微粒的物质的量浓度)。下列说法正确的是

A.常温下,H2C2O4的Ka1=100.8
B.pH=3时,溶液中
C.pH由0.8增大到5.3的过程中,水的电离程度逐渐增大
D.常温下,随着pH的增大,的值先增大后减小
高三化学单选题困难题查看答案及解析
草酸(H2C2O4)是一种二元弱酸。常温下,向H2C2O4溶液中逐滴加入NaOH溶液,混合溶液中lgX[X为或
]与pH的变化关系如图所示。下列说法正确的是( )

A.Ⅱ表示lg随pH变化的关系曲线
B.pH=1.22的溶液中:c(HC2O4-)=c(C2O42-)
C.NaHC2O4溶液中:c(H+)<c(OH-)
D.pH=4.19的溶液中:c(Na+)<3c(HC2O4-)
高三化学单选题中等难度题查看答案及解析
草酸(H2C2O4)是一种二元弱酸。常温下,向H2C2O4溶液中逐滴加入NaOH溶液,混合溶液中lgX[X为或
]与pH的变化关系如图所示。下列说法一定正确的是
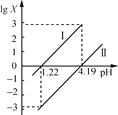
A.Ⅰ表示lg与pH的变化关系
B.pH=1.22的溶液中:2c(C2O42—)+c(HC2O4—)>c(Na+)
C.1.22<pH<4.19的溶液中:c(HC2O4—)>c(C2O42—)>c(H2C2O4)
D.pH=4.19的溶液中:c(Na+)=3c(HC2O4—)
高三化学单选题中等难度题查看答案及解析
草酸(H2C2O4)是一种二元弱酸。常温下向H2C2O4溶液中滴加NaOH溶液,混合溶液里lgX[X表示或
]随pH的变化关系如图所示。下列说法不正确的是

A. 直线I中X表示的是
B. 直线I、Ⅱ的斜率均为1
C. c(HC2O4-)>c(C2O42-)>c(H2C2O4)对应1.22<pH<4.19
D. c(Na+)=c(HC2O4-)+2c(C2O42-)对应pH=7
高三化学单选题困难题查看答案及解析
草酸(H2C2O4)是一种二元弱酸。常温下向H2C2O4溶液中滴加NaOH溶液,混合溶液里lgX[X表示或
]随pH的变化关系如图所示。下列说法不正确的是

A. 直线I中X表示的是
B. 直线I、Ⅱ的斜率均为1
C. c(HC2O4-)>c(C2O42-)>c(H2C2O4)对应1.22<pH<4.19
D. c(Na+)=c(HC2O4-)+2c(C2O42-)对应pH=7
高三化学单选题困难题查看答案及解析
常温时,向H2C2O4(二元弱酸)溶液中滴加NaOH溶液,混合溶液中lgX[X表示或
]随pH的变化关系如图所示。下列说法正确的是

A.pH=1.22时混合溶液中c(Na+)>c()+2c(
)
B.0.1mol/LNaHC2O4溶液中:c(OH−)>c(H+)
C.H2C2O4的一级电离常数为1×10−4.19
D.I中X表示的是
高三化学单选题困难题查看答案及解析
草酸(H2C2O4)是一种二元弱酸。常温下向H2C2O4溶液中滴加NaOH溶液,混合溶液里lgX[X表示或
]随pH的变化关系如图所示。下列说法不正确的是

A.直线I中X表示的是
B.直线I、Ⅱ的斜率均为1
C.c(HC2O4-)>c(C2O42-)>c(H2C2O4)对应1.22<pH<4.19
D.c(Na+)=c(HC2O4-)+2c(C2O42-)对应pH=7
高三化学单选题困难题查看答案及解析
草酸(H2C2O4)是一种二元弱酸。常温下向H2C2O4溶液中滴加NaOH溶液,混合溶液里lgX[X表示或
]随pH的变化关系如图所示。下列说法不正确的是

A.直线I中X表示的是
B.直线I、Ⅱ的斜率均为1
C.c(HC2O4-)>c(C2O42-)>c(H2C2O4)对应1.22<pH<4.19
D.c(Na+)=c(HC2O4-)+2c(C2O42-)对应pH=7
高三化学单选题困难题查看答案及解析
H2C2O4是一种二元弱酸。常温下向H2C2O4溶液中滴加NaOH溶液,混合液中lgX随pH的变化关系如图所示。下列说法不正确的是( )
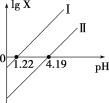
A.线Ⅰ中X表示的是
B.线Ⅰ、Ⅱ的斜率均为1
C.c(HC2O42-) > c(C2O42-) > c(H2C2O4)对应溶液pH:1.22 < pH < 4.19
D.c(Na+)=c(HC2O4-)+2c(C2O42-)对应溶液的pH=7
高三化学单选题困难题查看答案及解析
草酸(H2C2O4)是一种二元弱酸。常温下,向H2C2O4溶液中逐滴加入NaOH溶液,混合溶液中lgX[X为c(HC2O4-)/c(H2C2O4)或c(C2O42-)/c(HC2O4-)]与pH的变化关系如图所示。下列说法一定正确的是( )
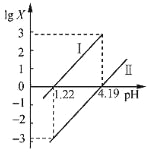
A. Ⅰ表示lgc(HC2O4-)/c(H2C2O4)与pH的变化关系
B. pH=1.22的溶液中:2c(C2O42﹣)+c(HC2O4﹣)>c(Na+)
C. 1.22<pH<4.19的溶液中:c(HC2O4﹣)>c(C2O42﹣)>c(H2C2O4)
D. pH=4.19的溶液中:c(Na+)=3c(HC2O4﹣)
高三化学多选题中等难度题查看答案及解析