-
氨气和氨水在工农业生产中均有重要应用。
(1)工业合成氨反应的化学方程式是_________。
(2)实验室常加热熟石灰[主要成分是Ca(OH)2]和氯化铵混合固体制取氨气,写出反应的化学方程式___________。
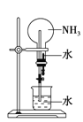
(3)如图所示,向表面皿中的NaOH固体滴几滴浓氨水,迅速盖上盖,观察现象。
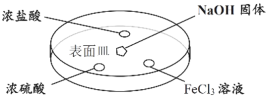
①___________液滴上方会出现白烟(填序号)
A.浓盐酸 B.浓硫酸 C.FeCl3溶液
②一段时间后浓硫酸的液滴中有白色固体,生成该白色固体的化学方程式是_______。
③FeCl3液滴中出现的现象是___________,发生反应的离子方程式是_________。
(4)利用氨水可以将大气污染物SO2吸收并生产氮肥,原理如图所示:
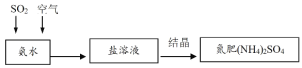
分析上述生产原理,在下列表格中填写该生产过程中利用的SO2的化学性质并进行理论论证
| SO2的化学性质 | 理论论证 |
| ______ | ______ |
| ______ | ______ |
-
氨气是一种重要化合物,在工农业生产、生活中有着重要应用。
(1) 实验室制备NH3,下列方法中可以选用的是_______________。
A.固态氯化铵与熟石灰混合加热 B.固态氯化铵加热分解
C.碱石灰中滴加浓氨水 D.氯化铵溶液与氢氧化钠溶液共热
(2) “氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收所得气体制取硝酸(固定装置略去):
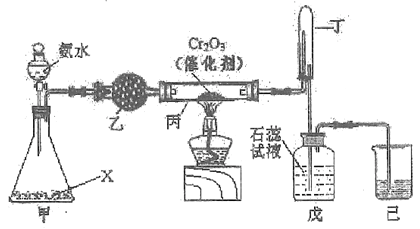
①盛装氨水仪器的名称是________。甲装置不需要加热即能同时产生氨气和氧气,则锥形瓶内固体X的化学式为____________。
②乙装置中药品的名称是_________。写出受热时丙装置发生反应的化学方程式________。
③当戊中观察到______现象,则说明戊中制得硝酸。某同学按上图组装仪器并检验气密性后进行实验,并没有观察到此现象,请分析实验失败的可能原因________,如何改进装置_________。
(3) 若将氨气和氯气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出该反应的化学方程式_____________。
-
(14分)氮元素的单质及化合物在工农业生产中有重要应用。
(1)①氮气用于工业合成氨,写出氮气的电子式 ;
②NH3的稳定性比PH3 (填写“强”或“弱”)。
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。

①浓盐酸液滴附近发生反应的化学方程式为 。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是 (写化学式,一种即可)。
③FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2+ + 2NH3·H2O= Fe(OH)2↓+ 2NH4+ 和 _______ 。
(3)将SO2气体通入氯化钡溶液,未见有沉淀生成,继续通入NH3,则出现白色沉淀,请写出反应的离子方程式______________________________________;若将SO2气体通入酸化的硝酸钡溶液,也产生白色沉淀,用离子方程式加以说明 。
(4)氮氧化物的排放会对空气造成污染,利用氧化法除去烟气中的氮氧化物。首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。
已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3
写出氧化吸收法除去氮氧化物的化学方程式___________________。
(5)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为 _________ ,若反应中有3 mol电子发生转移时,生成亚硝酸的质量为 g。
-
氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。回答下列问题。
(1)氨气的制备


①氨气制取的发生装置可以选择上图中的_________(填字母),反应的化学方程式为__________。
②选择上图装置组装一套实验装置来收集一瓶干燥的氨气,所选装置的连接顺序为:发生装置→______→______,______→_____→i(按气流方向,用小写英文字母表示)。
③可用如右装置进行氨的喷泉实验,引发喷泉的操作是__________。
(2)如图所示,NH3经一系列反应可以得到HNO3。

①反应①的化学方程式为__________________________。
②产物NO是大气污染物之一。在400℃左右且有催化剂存在的情况下,可用氨将一氧化氮还原为无色无毒气体。该反应的化学方程式_______________________。
-
氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。回答下列问题:
(1)氨气的制备

①氨气制取的发生装置可以选择上图中的_________(填字母),反应的化学方程式为____________________。
②选择上图装置组装一套实验装置来收集一瓶干燥的氨气,所选装置的连接顺序为:发生装置→______→______,______→_____→i(按气流方向,用小写英文字母表示)。
③可用如装置进行氨的喷泉实验,引发喷泉的操作是__________。

(2)如图所示,NH3经一系列反应可以得到HNO3。

①反应①的化学方程式为________________________________________。
②产物NO是大气污染物之一。在400℃左右且有催化剂存在的情况下,可用氨将一氧化氮还原为无色无毒气体。该反应的化学方程式为_______________________。
(3)在某100mL硝酸与硫酸的混合液中,HNO3和H2SO4的物质的量浓度分别为0.6 mol·L-1和0.3mol·L-1。向该混合液中加入3.84g铜粉,加热,待充分反应后,所得溶液中的Cu2+的物质的量浓度是多少____________?(写出计算过程)
-
氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。回答下列问题:
(1)氨气的制备
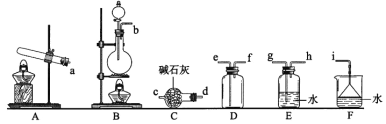
①氨气制取的发生装置可以选择上图中的_________(填字母),反应的化学方程式为_____________________________________________。
②选择上图装置组装一套实验装置来收集一瓶干燥的氨气,所选装置的连接顺序为:发生装置→______→______→______→_____→i(按气流方向,用小写英文字母表示)。
③可用如图装置进行氨的喷泉实验,引发喷泉的操作是_______________________________。
(2)如图所示,NH3经一系列反应可以得到HNO3。

①反应①的化学方程式为________________________________________。
②产物NO是大气污染物之一。在400℃左右且有催化剂存在的情况下,可用氨将一氧化氮还原为无色无毒气体。该反应的化学方程式为_______________________。
(3)在某100mL硝酸与硫酸的混合液中,HNO3和H2SO4的物质的量浓度分别为0.6 mol·L-1和0.3mol·L-1。向该混合液中加入3.84g铜粉,加热,待充分反应后,所得溶液中的Cu2+的物质的量浓度为____________。
-
氯化铵是一种重要的化工原料,应用广泛.
(1)实验室通常用NH4Cl固体与Ca(OH)2固体混合共热制取氨气.
①写出实验室制取氨气的反应方程式________
②浓氨水可以用来检验有毒气体氯气的泄漏,反应式为3Cl2+8NH3=N2+6NH4Cl,在该反应中,氧化剂是________(填化学式),检测时观察到的现象是________,21.3g氯气能氧化氨气________mol.
(2)用浓氯化铵溶液处理的舞台幕布难着火,其原因是________(填字母).
①幕布的着火点升高
②幕布的质量增加
③氯化铵分解吸收热量,降低了温度
④氯化铵分解产生的气体隔离了部分空气
A.①②B.③④C.①③D.②④
(3)实验室可用NH4Cl溶液与饱和的NaNO2溶液反应制取纯净的氮气,反应方程式为:NaNO2+NH4Cl NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
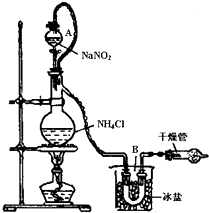
实验装置如图所示,试回答:
①装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是________(填写编号).
a.防止饱和溶液蒸发
b.保证实验装置不漏气
c.使饱和NaNO2溶液容易滴下
②加热前必须进行的一个操作步骤是________.
③收集N2最适宜的方法是________(填写编号)
a.排空气法收集在集气瓶中
b.排水法收集在集气瓶中
c.直接收集在球胆或塑料袋中.
-
(16分)氯化铵是一种重要的化工原料,应用广泛。
(1)实验室通常用NH4Cl固体与Ca(OH)2固体混合共热制取氨气。
①写出实验室制取氨气的反应方程式________ ________。
②浓氨水可以用来检验有毒气体氯气的泄漏,反应式为3Cl2 +8NH3= N2 + 6NH4Cl,在该反应中,氧化剂是 (填化学式),检测时观察到的现象是________ ________,21.3 g氯气能氧化氨气________mol。
(2)用浓氯化铵溶液处理的舞台幕布难着火,其原因是________(填字母)。
①幕布的着火点升高
②幕布的质量增加
③氯化铵分解吸收热量,降低了温度
④氯化铵分解产生的气体隔离了部分空气
A.①② B.③④ C.①③ D.②④
(3)实验室可用NH4Cl溶液与饱和的NaNO2溶液反应制取纯净的氮气,反应方程式为:
NaNO2+NH4Cl  NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
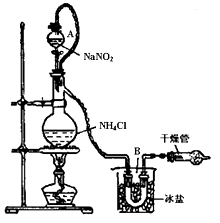
实验装置如下图所示,试回答:
①装置中A部分的分液漏斗与蒸馏烧瓶之间连接
的导管所起的作用是________(填写编号)。
a.防止饱和溶液蒸发
b.保证实验装置不漏气
c.使饱和NaNO2溶液容易滴下
②加热前必须进行的一个操作步骤是________ ________。
③收集N2最适宜的方法是________(填写编号)
a.排空气法收集在集气瓶中
b.排水法收集在集气瓶中
c.直接收集在球胆或塑料袋中
-
化学变化中既有物质变化,也有能量变化,研究化学反应有利于指导工业生产.下列是常见的化学反应:①电解熔融氯化钠 ②氮气与氢气合成氨气 ③锌与稀硫酸反应 ④煅烧石灰石.
(1)从不同角度可以对上述反应进行分类:从反应前后能量变化角度看上述反应属于放热反应的是______(填序号,下同);从有无电子转移角度看上述反应属于非氧化还原反应的是______;从反应前后物质种类的变化角度看,①和④均属于______反应;①和②在变化过程中断裂的化学键类型分别为______、______.
(2)反应③在实验室中用于制备氢气,要提高生成氢气的速率下列措施合理的是______.
a.加入硝酸,增大氢离子的浓度 b.用浓硫酸代替稀硫酸
c.加入少量铜粉 d.将稀硫酸的体积加倍.
反应③可以设计成原电池反应,其中负极上反应的物质是______,电子流向______极.
(3)反应②是可逆反应,常应用于工业生产,升高温度正反应速率______(填“增大”、“减小”或“不变”,下同),逆反应速率______;请列举一项该反应达到平衡的标志______.
-
将10.7g 氯化铵固体与足量熟石灰混合加热,使之充分反应。
(1)写出反应的化学方程式: 。
(2)生成的氨气在标准状况下的体积是 L。
(3)若将这些氨气溶于水配成500mL氨水,该氨水的物质的量浓度是 mol·L-1。
(4)在400℃左右且有催化剂存在的情况下,用氨可以把一氧化氮还原成氮气,方程式为:4NH3+6NO=5N2+6H2O,此反应中氧化产物与还原产物的物质的量之比为 。














