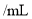-
84消毒液是一种以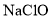 为有效成分的高效消毒剂,广范应用于家庭和公共区域的杀菌消毒。某品牌消毒液中
为有效成分的高效消毒剂,广范应用于家庭和公共区域的杀菌消毒。某品牌消毒液中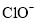 含量的测定步骤如下:
含量的测定步骤如下:
步骤1:用滴定管量取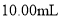 消毒液原液于锥形瓶中。
消毒液原液于锥形瓶中。
步骤2:向锥形瓶中加入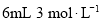 的
的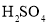 和过量的
和过量的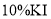 溶液,立即加盖摇匀,置于暗处约
溶液,立即加盖摇匀,置于暗处约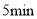 。
。
步骤3:将步骤2中溶液加水稀释至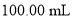 ,取出
,取出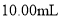 。立即用
。立即用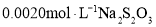 标准溶液滴定至溶液呈淡黄色,加入淀粉溶液作指示剂,继续滴加
标准溶液滴定至溶液呈淡黄色,加入淀粉溶液作指示剂,继续滴加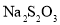 标准溶液至终点,记录标准溶液消耗的体积。(已知:
标准溶液至终点,记录标准溶液消耗的体积。(已知: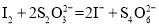 )
)
将上述步骤3重复2次,测得的实验数据见下表。
| 次数 | 待测溶液体积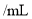 | 标准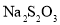 溶液体积 溶液体积 |
| 滴定前刻度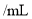 | 滴定后刻度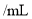 |
| 1 | 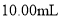
| 1.00 | 24.00 |
| 2 | 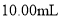
| 2.01 | 22.00 |
| 3 | 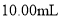
| 3.00 | 23.01 |
(1)步骤2中发生反应的离子方程式为___________。
(2)滴定终点的现象是___________。
(3)步骤2未加盖摇匀,会使测定结果___________。(填“偏大”“编小”或“无影响”)
(4)计算该品牌消毒原液中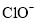 的物质的量浓度___________(写出计算过程)
的物质的量浓度___________(写出计算过程)
-
过氧乙酸( )是一种高效消毒剂,常用于环境消毒杀菌,可以迅速杀死多种微生物。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
)是一种高效消毒剂,常用于环境消毒杀菌,可以迅速杀死多种微生物。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
①在三颈烧瓶中加入一定量冰醋酸与浓H2SO4的混合液体,再缓缓加入适量30%的双氧水。
②不断搅拌并控制B中混合液的温度为20~30℃至反应结束。
③接入冷凝管和抽气泵,在锥形瓶中收集得到产品。
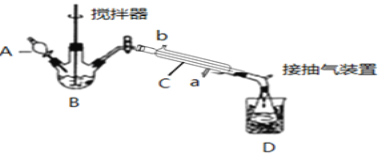
请回答下列问题:
(1)仪器B的名称是__;仪器C中冷水流入口是__(填a或b);
(2)为更好地控制反应温度,应采用方法是__;
(3)生成过氧乙酸的化学方程式为__;
(4)不同反应物比例,实验测得生成过氧乙酸含量(%)随时间的变化数据(见下表),由表中数据可知,反应物最佳比例(CH3COOH/H2O2)是__,反应所需时间约__(选填1、3、5、7)小时;
| 反应物比例CH3COOH/H2O2 | 反应时间(小时) |
| 0.5 | 1 | 3 | 5 | 7 |
| 2∶1 | 7.38 | 8.46 | 9.42 | 11.26 | 13.48 |
| 1∶1 | 10.56 | 12.92 | 13.54 | 20.72 | 20.70 |
| 1∶2 | 6.14 | 7.10 | 7.96 | 10.38 | 12.36 |
(5)请设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率;可供选择的试剂和主要器材有:a.过氧乙酸溶液、b.1mol/L的FeCl3溶液、c.0.5mol/L的Fe2(SO4)3溶液、d.0.5mol/L的CuCl2溶液、e.1mol/L的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i.带导气管的试管。
你选择的试剂及器材是a、__、f、g、i(选填序号),实验方案是__。
(6)碘量法取2.00mL过氧乙酸试样稀释成100mL,从中取出5.00mL,滴加酸性KMnO4溶液至恰好粉红色以除去残余H2O2,再加入10mL10%KI溶液和几滴淀粉溶液,摇匀,反应完全后再用0.1000mol/L的Na2S2O3标准液滴定至终点(反应方程式为2Na2S2O3+I2=Na2S4O6+2NaI),共消耗14.30mLNa2S2O3标准液。该样品中过氧乙酸的物质的量浓度是__mol/L。(结果保留小数点后两位)
提示:CH3COOOH+2I-+2H+=I2+CH3COOH+H2O)
-
某品牌的家用消毒剂其有效成分对氯间二甲苯酚(结构简式如下图所示),可以杀灭常见的病毒与细菌。下面有关物质的说法正确的是

A. A B. B C. C D. D
-
某品牌的家用消毒剂其有效成分为对氯间二甲苯酚(结构简式如下图所示),可以杀灭常见 的病毒与细菌。下面有关该物质的说法正确的是
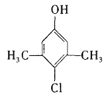
A.该物质的分子式是C8H10ClO
B.1mol该物质最多可以与2mol NaOH反应
C.1mol该物质可以与2mol液溴发生取代反应
D.该物质可以发生加成、取代、消去、氧化等反应
-
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化氢的含量
步骤如下并填写下列空白:
(1)将10.00 mL密度为ρ g/mL的过氧化氢溶液稀释至250mL。量取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,作被测试样。此过程中需要用到的定量仪器 。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请完成该反应方程
___MnO4- + __H2O2 + ___H+ → ___Mn2+ + __H2O + __ _____
(3) 滴定时,将高锰酸钾标准溶液注入滴定管中,滴定到达终点的现象是
(4)重复滴定二次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为___________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果____(填“偏高”“偏低”“不变”)。
Ⅱ.探究过氧化氢的性质
该化学小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、淀粉碘化钾溶液、二氧化锰,实验仪器及用品可自选。)
请将他们所选的实验试剂和实验现象填入下表:
| 实 验 内 容 | 实 验 试 剂 | 实 验 现 象 |
| 探究氧化性 | | |
| 探究不稳定性 | | |
-
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
84消毒液
有效成分 NaClO
规格 1 000 ml
质量分数 25%
密度 1.19 g·cm-3
(1)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=____mol·L-1。
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL该消毒液。下列说法正确的是________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
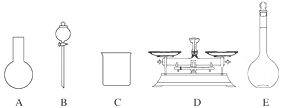
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(3)配制溶液的过程如下,该同学的错误步骤有(______)

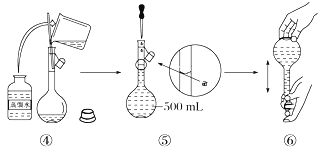
A.1处 B.2处 C.3处 D.4处
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。需用浓硫酸的体积为____mL。
-
氯气是工业生产中的重要原料,含氯消毒剂在生活中有着广泛的用途。
(1)工业生产中通过电解饱和食盐水获取大量氯气,化学方程式为________________。
(2)氯气可用于制取“84”消毒液(有效成分为NaClO),离子方程式为_______________。
-
二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂。实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2。(“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。)下列说法正确的是
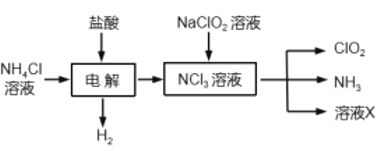
A.电解过程中每消耗1molHCl转移1mol电子
B.X溶液中主要阴离子是OH−
C.除去ClO2中的NH3可用水
D.ClO2的有效氯含量约为2.63g
-
下列物质的用途不正确的是
①Ca(ClO)2是84消毒液的有效成分 ②Fe2O3可用作红色涂料
③氢氧化铁胶体能用于净水和杀菌消毒 ④液氨可用作制冷剂
⑤Na2O2可用作潜水艇的供氧剂 ⑥H2O2可用作绿色氧化剂
⑦二氧化硫可用来漂白馒头 ⑧钠失火后可用二氧化碳作灭火剂
A. ①③⑦⑧ B. ①②⑦⑧ C. ①③④⑤ D. ②③⑤⑦
-
“84消毒液”因1984年北京某医院研制使用而得名,在日常生活中使用广泛,其有效成分是NaClO。某化学研究性学习小组在实验室制备NaClO溶液,并进行性质探究和成分测定
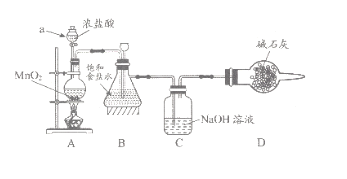
(1)该学习小组按上图装置进行实验(部分夹持装置省去),反应一段时间后,分别取B、C瓶中的溶液进行实验,实验现象如下表。
已知:1.饱和NaClO溶液pH为11;
2.25°C时,弱酸电离常数为:H2CO3:K1=4.4×10-7,K2=4.7×10-11;HClO:K=3×10-8
| B瓶 | C瓶 |
| 实验1:取样,滴加紫色石蕊试液 | 变红,不褪色 | 变蓝,不褪色 |
| 实验2:测定溶液的pH | 3 | 12 |
回答下列问题:
①仪器a的名称_____,装置A中发生反应的离子方程式________。
②实验1中B瓶溶液中产生现象的原因是_________。
③若将C瓶溶液换成 NaHCO3溶液,按上述操作步骤进行实验,C瓶现象为:实验1中紫色石蕊试液立即褪色;实验2中溶液的pH=7。结合平衡移动原理解释紫色石蕊试液立即褪色的原因______。
(2)测定C瓶溶液中NaClO含量(单位:g/L)的实验步骤如下:
Ⅰ.取C瓶溶液20ml于锥形瓶中,加入硫酸酸化,加入过量KI溶液,盖紧瓶塞并在暗处充分反应。
Ⅱ.用0.1000mol/LNa2S2O3标准溶液滴定锥形瓶中的溶液,指示剂显示终点后,重复操作2~3次,Na2S2O3溶液的平均用量为24.00ml。(已知:I2+2S2O32-=2I-+S4O62-)
①步骤Ⅰ的C瓶中发生反应的离子方程式为_______。
②步骤Ⅱ通常选用___作指示剂,滴定至终点的现象______。
③C瓶溶液中NaClO含量为_____g/L(保留2位小数)
 为有效成分的高效消毒剂,广范应用于家庭和公共区域的杀菌消毒。某品牌消毒液中
为有效成分的高效消毒剂,广范应用于家庭和公共区域的杀菌消毒。某品牌消毒液中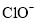 含量的测定步骤如下:
含量的测定步骤如下: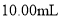 消毒液原液于锥形瓶中。
消毒液原液于锥形瓶中。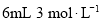 的
的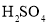 和过量的
和过量的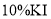 溶液,立即加盖摇匀,置于暗处约
溶液,立即加盖摇匀,置于暗处约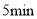 。
。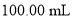 ,取出
,取出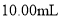 。立即用
。立即用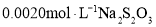 标准溶液滴定至溶液呈淡黄色,加入淀粉溶液作指示剂,继续滴加
标准溶液滴定至溶液呈淡黄色,加入淀粉溶液作指示剂,继续滴加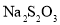 标准溶液至终点,记录标准溶液消耗的体积。(已知:
标准溶液至终点,记录标准溶液消耗的体积。(已知: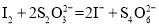 )
)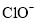 的物质的量浓度___________(写出计算过程)
的物质的量浓度___________(写出计算过程)