-
海水是巨大的资源宝库,从海水中可以提取食盐、溴,还可以制得金属镁等,下图是制取原理流程图:

回答下列问题:
(1)操作1的名称是_______________。
(2)步骤①除去粗盐中的杂质(Mg2+、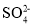 、Ca2+),加入药品顺序正确的是_______________。
、Ca2+),加入药品顺序正确的是_______________。
A.NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸.
C.NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
D.Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
(3)步骤②中空气与水蒸气的作用是_______________。步骤②中已获得Br2,步骤③中又将Br2还原成Br-,其目的是_______________。
(4)写出步骤③的离子反应方程式_______________。
(5)写出步骤④的化学反应方程式_______________,下列物质可以用作镁蒸气的冷却剂的是_______________。
A.空气 B.Ar C.CO2
-
海水是巨大的资源宝库。下图是从海水中提取食盐和溴的主要流程。
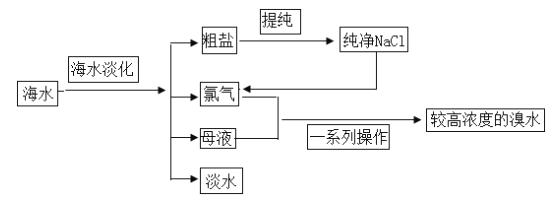
(1)粗盐除含 NaCl 外,还含有少量 MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是粗盐提纯的
操作流程。
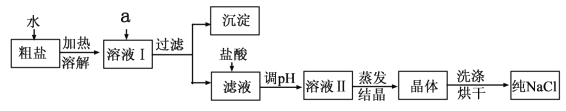
提供的试剂:
Na2CO3溶液、 K2CO3溶液、 NaOH 溶液、 BaCl2溶液、 Ba(NO3)2溶液、饱和 NaCl 溶液。
①除去溶液 I 中的 MgCl2、 CaCl2、 Na2SO4,从提供的试剂中选出 a 所代表的试剂,按滴加顺序依次为: 过量的NaOH 溶液、_______、_______;
②如何证明操作①中 NaOH 溶液已经过量?_______。
③蒸发过程所用的主要仪器有:铁架台、酒精灯、_______;
(2)某同学在实验室中用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的操作是:_______。
②分离溴的四氯化碳溶液的操作方法是:_______。
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料, Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为 100℃。他们参观生产过程后,设计了如下装置简图:
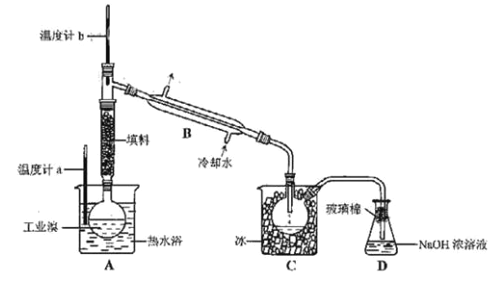
①图中仪器 B 的名称:_______。
②用热水浴加热的优点是:_______。
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:_______℃。
-
海水是巨大的资源宝库。下图是从海水中提取食盐和溴的主要流程。
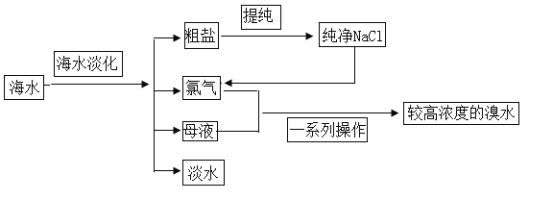
(1)粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。

提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
①除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、_____________、_____________;
②如何证明操作①中NaOH溶液已经过量?_______________________________________
③蒸发过程所用的主要仪器有:铁架台、酒精灯、_______________________;
(2)某同学欲用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的具体操作是:______。②分离碘的四氯化碳溶液的操作方法是:________。
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为100℃。他们参观生产过程后,设计了如下装置简图:
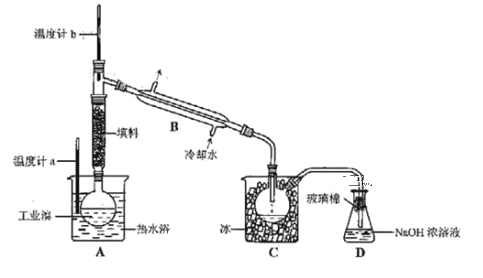
①图中仪器B的名称:__________。
②用热水浴加热的优点是:________。
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:____。
-
海水是巨大的资源宝库.如图1是从海水中提取食盐和溴的主要流程.
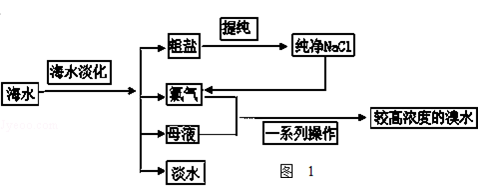
(1)粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质.如图2是粗盐提纯的操作流程.
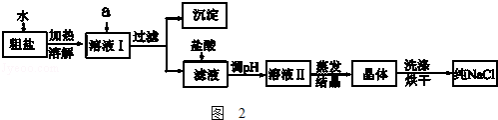
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液.
①除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、
②如何证明操作①中NaOH溶液已经过量?
③蒸发过程所用的主要仪器有:铁架台、酒精灯、 、 ;
(2)某同学欲四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,分离出四氯化碳层的操作:
(3)工业上将较高浓度的溴水经进一步处理得到工业溴.某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性.水的沸点为100℃.他们参观生产过程后,设计了如图3装置简图:

①图中仪器B的名称: ②温度计水银球的位置:
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:
-
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示;下列描述错误的是:
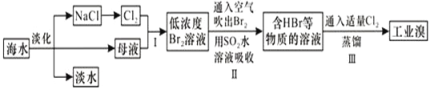
A. 淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
B. 以NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
C. 步骤Ⅱ中鼓入热空气吹出溴,是因为溴蒸气的密度比空气的密度小
D. 用SO2水溶液吸收Br2的离子反应方程式为:Br2+SO2+2H2O═4H++SO42﹣+2Br﹣
-
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示;下列描述错误的是:
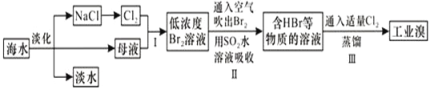
A. 淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
B. 以NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
C. 步骤Ⅱ中鼓入热空气吹出溴,是因为溴蒸气的密度比空气的密度小
D. 用SO2水溶液吸收Br2的离子反应方程式为:Br2+SO2+2H2O═4H++SO42﹣+2Br﹣
-
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示;下列描述错误的是:
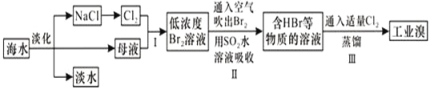
A. 淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
B. 以NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
C. 步骤Ⅱ中鼓入热空气吹出溴,是因为溴蒸气的密度比空气的密度小
D. 用SO2水溶液吸收Br2的离子反应方程式为:Br2+SO2+2H2O═4H++SO42﹣+2Br﹣
-
海水是巨大的资源宝库。下图是人类从海水资源获取某些重要化工原料的流程示意图。
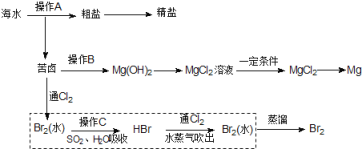
回答下列问题:
(1)操作B是______________(填实验基本操作名称)。
(2)操作B需加入下列试剂中的一种,最合适的是_________。
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液
(3)工业上制取金属镁时是电解熔MgCl2,电解反应方程式为_________________。
(4)上图中虚线框内流程的主要作用是____________。
-
海洋是巨大的资源宝库,从其中提取食盐和溴的过程如图所示。下列描述错误的是( )
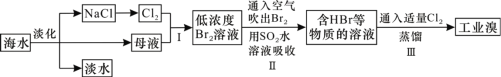
A.淡化海水的方法主要有蒸馏法、电渗析法、离子交换法
B.以NaCl为原料可以生产烧碱、纯碱、金属钠、氯气、盐酸等化工产品
C.SO2水溶液吸收Br2的离子反应方程式为Br2+SO2+2H2O=4H++SO42-+2Br-
D.步骤Ⅱ中鼓入热空气吹出溴,是因为溴蒸气的密度比空气的密度小
-
海水是巨大的资源宝库,下列说法正确的是
A.碘元素又称“海洋元素”
B.镁是海水中含量最多的金属元素
C.从海水中提取食盐和碘的过程都是物理变化
D.氯碱工业的主要原料是食盐

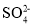 、Ca2+),加入药品顺序正确的是_______________。
、Ca2+),加入药品顺序正确的是_______________。












