-
有机物在生活中无处不在,对人类的生产生活有着重要的作用。
(1)下列物质中不属于有机物的是_____(填字母)。
a.CO2 b.CH4 c.CH3COOH
(2)下列有机物不属于合成高分子的是_____(填字母)。
a.塑料 b.聚乙烯 c.蛋白质
(3)下列物质中不属于糖类的是_____(填字母)。
a.淀粉 b.氨基酸 c.纤维素
(4)下列不属于油脂水解产物的是_____(填字母)。
a.高级脂肪酸 b.甘油(丙三醇) c.乙烯
(5)下列物质中的组成元素与另两种不同的是_____(填字母)。
a.蛋白质 b.糖类 c.油脂
(6)蔗糖的水解产物是_____、_____(填名称),淀粉的化学式为_____。
(7)写出乙烯与溴水反应的化学方程式:_____,该反应类型为_____反应。
(8)乙醇能使酸性KMnO4溶液褪色,这是因为乙醇具有_____性。
高一化学填空题简单题查看答案及解析
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)如图1是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式 。
(2)在0.5L的密闭容器中,充入一定量的氮气和氢气进行反应,三种气体的物质的量随时间的变化曲线如图2所示。则Y是 ,2min内N2的反应速率υ(N2)= 。
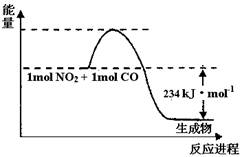
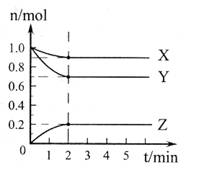
图1 图2
(3)硝酸工业在国民经济、国防工业和航天事业中占有重要地位。随着化学纤维、近代有机合成、火箭、导弹等工业的迅速发展,需要使用大量的硝酸。
①工业生产中用铂系金属作为催化剂,用氨氧化法制取硝酸。第一步反应为氨在催化剂作用下与氧气发生反应生成NO,写出反应化学方程式 。
②铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3 → Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)。反应中还原产物是 ,0.6mol Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则得到标准状况下气体体积为 L。
高一化学填空题简单题查看答案及解析
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
(1)如图1是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式________.
(2)在0.5L的密闭容器中,充入一定量的氮气和氢气进行反应,三种气体的物质的量随时间的变化曲线如图2所示.则Y是________,2min内N2的反应速率υ(N2)=________.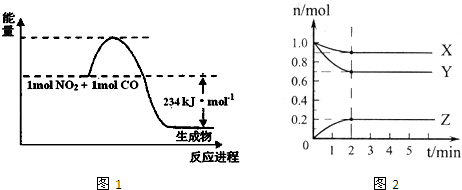
(3)硝酸工业在国民经济、国防工业和航天事业中占有重要地位.随着化学纤维、近代有机合成、火箭、导弹等工业的迅速发展,需要使用大量的硝酸.
①工业生产中用铂系金属作为催化剂,用氨氧化法制取硝酸.第一步反应为氨在催化剂作用下与氧气发生反应生成NO,写出反应化学方程式________.
②铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平).反应中还原产物是________,0.6mol Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则得到标准状况下气体体积为________L.高一化学填空题中等难度题查看答案及解析
-
氯及其化合物在工农业生产和人类生活中有着重要的作用。回答下列问题:
(1)25℃时将氯气溶于水形成“氯气-氯水”体系,该体系存在多个含氯元素的平衡关系,其中之一为:Cl2(溶液)+H2O
HClO+H++Cl-,体系中Cl2(溶液)、HClO和ClO-三者的物质的量分数(α)随pH(酸碱度)变化的关系如图所示。已知HClO的杀菌能力比ClO-强,用氯气处理饮用水时,杀菌效果最强的pH范围为__(填字母)。
A.0~2 B.2~4.7 C.4.7~7.5 D.7.5~10

(2)写出次氯酸光照分解的化学方程式___,如果在家中直接使用自来水养金鱼,除去其中残留的次氯酸可采取的简易措施为__。
(3)NaClO、NaClO2、ClO2等含氯化合物都是常见的消毒剂,这是因为它们都具有强氧化性。
①写出工业上用氯气和NaOH溶液生产消毒剂NaClO的化学方程式___;
②84消毒液(主要成分是NaClO)与洁厕灵(主要成分是盐酸)混在一起使用会产生有毒气体Cl2,其反应的离子方程式为__;
③NaClO2中Cl元素化合价为__;
④ClO2的杀菌效果比Cl2好,等物质的量的ClO2杀菌效果是Cl2的__倍(杀菌效果与单位物质的量的氧化剂得电子的物质的量有关,ClO2与Cl2消毒杀菌后均被还原为Cl-)。
高一化学综合题中等难度题查看答案及解析
-
金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)下列物质中不属于合金的是 ____________。
A.钢 B.青铜 C.黄铜 D.水银
(2)在钠、铝、铁三种金属元素中,金属活动性最强的是______ ,所形成的氧化物中适宜做耐火材料的是_______。向盛有硫酸铝溶液的试管中滴加氨水,反应的离子方程式为____________ 。
(3)乙同学为了获得持久白色的Fe(OH)2沉淀,准备用如图所示装置,用不含O2的蒸馏水配制的NaOH溶液与新制的FeSO4溶液反应。获得不含O2的蒸馏水的方法是_________。反应开始时,打开止水夹的目的是____________;一段时间后,关闭止水夹,在试管_______(填“A”或“B”)中观察到白色的Fe(OH)2

(4)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是______ 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
高一化学综合题困难题查看答案及解析
-
(13分)下表为元素周期表的一部分,A、B、D、E、G、L、Q为部分元素。其中L的单质在人类的生产和生活中有着十分重要的作用,Q的化合物可以有黑色、红色、蓝色、白色等多种颜色。
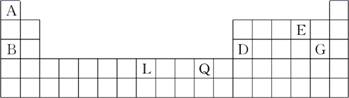
(1)请回答下列问题:
①写出G-的结构示意图:________。
②元素L在周期表中的位置:________。
③元素Q的单质为红色,写出单质Q在空气中生锈的化学方程式:_______________。
(2)由A、D、E、G、L五种元素组成的物质[DL(EA)nG6-n]m(其中m、n为正整数,n<5、m<10)广泛应用于日常生活用水和工业污水的处理。某化工厂以工业生产废料(D、L的单质及其氧化物)为原料制取[DL(EA)nG6-n]m,设计的生产流程如下:

①选用的试剂X应为________。
②下列关于[DL(EA)nG6-n]m的说法正确的是________(填序号)。
A.该物质中L元素的化合价为+2
B.该物质在熔融态不导电
C.该物质在强酸和强碱性溶液中均不能稳定存在
D.该物质溶于水能电离出(EA)离子,是一种碱
③写出上述流程的酸性溶液中加入BGE3时,发生反应的离子方程式:_______________。
高一化学填空题简单题查看答案及解析
-
2011年为“国际化学年”,其主题是“化学 我们的生活我们的未来”.下列对化学学科的认识错误的是( )
A.化学学科的发展对人类物质文明的进步有着重要作用
B.化学学科主要是在微观层面上研究物质的一门以实验为基础的自然科学
C.化学学科肩负着开发和研究新材料、新能源等领域的重要责任
D.我们应该珍爱生命,化学学科是研究、接触有毒有害物质,我们应该远离化学高一化学选择题中等难度题查看答案及解析
-
氮是地球上富含丰富的一种元素,氮及其化合物的工农业生成、生活中有着重要作用。请回答下列问题:
(1)如图1是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图(图中涉及物质为气态),请写出NO2和CO反应的热化学方程式____________________。
(2)在0.5L的密闭容器中,充入一定量的氮气和氢气进行反应,三种气体的物质的量随时间的变化曲线如图2所示。则Y是__________,2min内N2的反应速率v(N2)=__________。
(3)已知:一定量的N2(g)与H2(g)反应,生成2molNH3(g),放出92.2kJ热量。与依据事实,写出该反应的热化方程式__________。
一定条件下,在密闭容器中充入0.5molN2(g)与1.5molH2(g),二者充分反应后放出热量__________46.1kJ。(填“>”、“<”或“=”)

高一化学简答题中等难度题查看答案及解析
-
(13分)氨在人类的生产和生活中有着广泛的应用
(1)下列含氮物质属于盐的是 属于非电解质的是 。
A.NH3
B.NH3•H2O
C.NH4NO3
D.HNO3
E.N2
(2)0.1 mol的N2H4气体和0.2molNH3气体,它们在同温、同压下的体积比是 ,所含的原子数比是 。
(3)氨气溶解于水,得到的溶液称为氨水。氨溶解于水时与水发生反应生成一水合氨(NH3·H2O),它是一种弱碱。写出一水合氨的电离方程式 。从上述电离方程式可知,往氨水中加入稀硫酸生成的盐是 (填化学式)
(4)标准状况下,将 2.24L的氨气溶于水配成 0.5L溶液,所得溶液的物质的量浓度为 mol/L。
(5)氨可与Cl2反应,反应方程式如下:8NH3+3Cl2=6NH4Cl+N2,利用该反应的原理,在工业上可用于检验输送氯气的管道是否漏气。该反应中,________ __是还原剂;若反应中有1.5mol氧化剂参与反应,则发生转移的电子的物质的量为____________mol,被氧化的物质有 mol。
高一化学填空题中等难度题查看答案及解析
-
材料是人类赖以生存和发展的重要物质基础。
①有机高分子材料的出现是材料发展史上的一次重大突破。下列物质中含有有机高分子材料的是__________;
A.普通水泥 B.普通玻璃 C.汽车轮胎
②生产和生活中,合金几乎无处不在。我国最早使用的合金是___________(填“铜合金”或“铝合金”);
③钢铁是目前用量最大、用途最广的金属材料,在潮湿空气中容易发生腐蚀。请写出钢铁发生电化学腐蚀的负极反应式__________。
高一化学综合题简单题查看答案及解析