-
根据反应KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是( )

A.石墨b是原电池的负极,发生氧化反应
B.忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol
C.甲烧杯中的电极反应式:MnO4-+5e-+8H+=Mn2++4H2O
D.电池工作时,盐桥中的K+向甲烧杯中移动
-
根据反应KMnO4+FeSO4+H2SO4-MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是( )
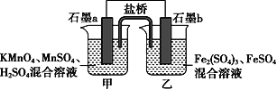
A.石墨b是原电池的负极,乙中发生氧化反应
B.电池工作时,盐桥中的K+向甲烧杯中移动
C.甲烧杯中的电极反应式: +5e-+8H+=Mn2++4H2O
+5e-+8H+=Mn2++4H2O
D.忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol
-
酸性条件下高锰酸钾溶液与硫酸亚铁反应,化学方程式如下:KMnO4+H2SO4+FeSO4→Fe2(SO4)3+K2SO4+MnSO4+H2O(未配平)下列说法正确的是( )
A.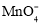 是氧化剂,Fe3+是还原产物
是氧化剂,Fe3+是还原产物
B.反应时可将酸化作用的H2SO4改为盐酸
C.生成1 mol Fe2(SO4)3时,转移2 mol电子
D.取反应后的溶液加KSCN溶液,有血红色沉淀生成
-
高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下:KMnO4+FeSO4+H2SO4→K2SO4+MnSO4+Fe2(SO4)3+H2O(未配平)。下列说法正确的是( )
A.KMnO4是氧化剂,Fe3+是还原产物 B.Fe2+的还原性强于 Mn2+
C.氧化剂和还原剂物质的量之比为 5:1 D.生成 1mol 水时,转移 2.5 mol 电子
-
高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下:KMnO4+FeSO4+H2SO4―→K2SO4+MnSO4+Fe2(SO4)3+H2O。(未配平)下列说法正确的是( )
A. Fe2+的还原性强于Mn2+
B. MnO4-是氧化剂,Fe3+是还原产物
C. 氧化剂和还原剂物质的量之比为5:1
D. 生成1 mol水时,转移2.5 mol电子
-
高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下(未配平):
KMnO4+ FeSO4+ H2SO4= K2SO4+ MnSO4+ Fe2(SO4)3+ H2O
下列说法正确的是
A.MnO4-是氧化剂,Fe3+是还原产物
B.Fe2+的还原性强于Mn2+
C.取反应后的溶液加KSCN溶液,可观察到有血红色沉淀生成
D.生成1mol 水时,转移2.5mol电子
-
Ⅰ、某化学反应的反应物和产物为:KMnO4 + KI + H2SO4 → MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化剂是 。
(2)如果该反应方程式中I2和KIO3的系数都是5,KMnO4的系数是 。
(3)在给出的化学式上标出电子转移的方向和数目: KMnO4 + KI + H2SO4 →
(4)如果没有对该方程式中的某些系数作限定,可能的配平系数有许多组。原因是______________。
Ⅱ、向盛有KI溶液的试管中加入少许CCl4后滴加氯水, CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式:

(2)整个过程中的还原剂是 。
(3)把KI换成KBr,则CCl4层变为橙红色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。据此判断下列反应能否进行HBrO3+HCl→ Br2+Cl2+H2O(未配平) 。(填“能”或“否”)
(4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若用Kl与Cl2反应制KIO3,至少需要消耗Cl2 L。(标准状况,保留2位小数)
-
配平下列方程并改写成离子方程式
(1)SO2 + KMnO4 + H2O → K2SO4 + MnSO4 + H2SO4
(2)Cu+HNO3 → Cu(NO3)2+NO↑+H2O
-
某反应体系中的物质有KMnO4、FeSO4、H2SO4、Fe2(SO4)3、MnSO4、K2SO4、H2O
(1)请将除水之外的反应物、产物填入以下横线中
________+________+________------________+________+________+H2O
(2)反应中,被氧化的元素是________,氧化剂是________,还原产物是________
(3)将氧化剂和还原剂填入空格中,并标出电子转移的方向和数目

-
(5分)利用氧化还原反应原理配平以下化学方程式,并填空:
FeSO4 + KNO3 + H2SO4 === K2SO4 + Fe2(SO4)3 + NO↑+ H2O
①氧化产物为________
②当电子转移了0.3mol时,有________g氧化剂参加反应


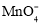 是氧化剂,Fe3+是还原产物
是氧化剂,Fe3+是还原产物