下表中所列的五种短周期元素,原子序数连续,但与表中排列顺序无关。用m表示基态原子的价电子数,用n表示基态原子的未成对电子数,m—n的值如下表所示:

下列说法错误的是
A.第一电离能:A<C B.电负性:E<D
C.原子序数:B<E D.核外未成对电子数:C=D
高三化学多选题中等难度题
下表中所列的五种短周期元素,原子序数连续,但与表中排列顺序无关。用m表示基态原子的价电子数,用n表示基态原子的未成对电子数,m—n的值如下表所示:

下列说法错误的是
A.第一电离能:A<C B.电负性:E<D
C.原子序数:B<E D.核外未成对电子数:C=D
高三化学多选题中等难度题
碳、氮、氧是地球上丰富的元素。
(1)C、N、O的第一电离能由大到小的顺序为(用元素符号表示)_________。
(2)前四周期元素中,基态原子未成对电子数与氮相同的元素有_________种。
(3)试判断NH3溶于水后,形成NH3·H2O的合理结构:_______(填字母代号),推理依据是____ ___________。
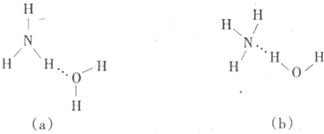
(4)H2O分子与H+结合的过程中未发生改变的是_________(填序号)。
a.微粒的空间构型 b.O原子的杂化方式 c.H—O—H的键角
(5)C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有__________个。
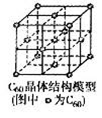
高三化学填空题困难题查看答案及解析
A、B、C、D、E、F为元素周期表中前四周期的元素,原子序数依次增大。A、C原子2p能级上均有两个未成对电子,EC2与BC2-为等电子体,D基态原子有11种运动状态的电子,F是第四周期未成对电子最多的原子。请回答下列问题:
(1)上述元素中第一电离能最大的是__(填元素符号)。A基态原子的电子排布式是__,E在周期表中的位置是第__周期__族。
(2)科学家成功地在高压下将AC2转化为具有空间立体网状结构的晶体,该晶体中A的杂化轨道类型是__。
(3)D+、AB-、F6+三种离子组成的化合物D3F(AB)6,其中化学键的类型有__,该化合物中存在一个复杂离子,该离子的化学式为__。
(4)“酒精检测仪”中有红色FC3和少量H2SO4,检测酒驾时反应的化学方程式为___。
高三化学综合题中等难度题查看答案及解析
已知A、B、C、D四种短周期元素,它们的核电荷数依次增大。A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族。 E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 。
(2)E2+离子的价层电子排布图是 ,F原子的电子排布式是 。
(3)A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 ,B元素的气态氢化物的VSEPR模型为 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为 。
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程为 。
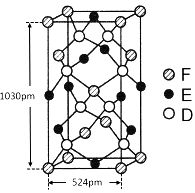
(6)某种化合物由D,E,F三种元素组成,其晶胞如图所示,则其化学式为 ,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度d= g/cm3。(保留两位小数)
高三化学推断题困难题查看答案及解析
已知A、B、C、D四种短周期元素,它们的核电荷数依次增大,A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族,E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号 ______ ,该能层具有的原子轨道数为 ______。
(2)E2+离子的价层电子排布图是 ______ ,F原子的电子排布式是 ______ 。
(3)A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 ______ ,B元素的气态氢化物的VSEPR模型为 ______ 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为 ______ 。
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程式为 ______ 。
(6)某种化合物由D,E,F三种元素组成,其晶胞如图所示,则其化学式为 ______,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度d= ______ g/cm3(列出计算式,无需计算)。
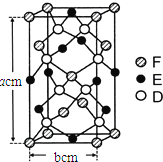
高三化学综合题困难题查看答案及解析
(10分)T、X、Y、Z是中学化学常见的四种短周期元素,原子序数依次增大,其结构或性质信息如下表:
| 元素 | 结构或性质信息 |
| T | 基态原子的L层上s电子数等于p电子数 |
| X | 基态原子最外层未成对电子数在该元素所在周期中最多 |
| Y | 基态原子的第一电离能在该元素所在周期中最小 |
| Z | 单质常温、常压下是气体。基态原子的M层上有1个未成对p电子 |
请根据信息回答有关问题(用具体元素符号或化学式作答)
(1)T、X、Y三种元素的电负性由大到小的顺序是________。
(2)写出元素Z基态原子的电子排布式。
(3)X的氢化物分子间能形成氢键,Z的氢化物分子间不易形成氢键,试分析原因是________。
(4)分子HTX中,有________个键,________个
键。
高三化学填空题简单题查看答案及解析
已知元素X、Y、Z、W、R为前四周期元素,且原子序数依次增大。X基态原子核外有三个未成对电子,Z、W分别是短周期中电负性最大和最小的元素;R2+离子的3d轨道中有三对成对电子。请回答下列问题:
(1)R基态原子的电子排布式为__________,元素X、Y、Z的第一电离能由大到小的顺序为(用元素符号表示)___________________。
(2)化合物XZ3的空间构型为______,R2+与NH3形成的配离子中,提供孤对电子的是_____。
(3)Z的氢化物由固体变为气态所需克服的微粒间的作用力是________。
(4)Z、W、R形成某种化合物的晶胞结构如右图所示,其化学式为___________。
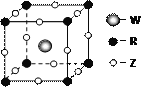
(5)XY2-能被酸性KMnO4溶液氧化,其中MnO4-被还原为Mn2+,反应的离子方程式是________________。
高三化学推断题中等难度题查看答案及解析
已知元素X、Y、Z、W、R为前四周期元素,且原子序数依次增大。X基态原子核外有三个未成对电子,Z、W分别是短周期中电负性最大和最小的元素;R2+离子的3d轨道中有三对成对电子。请回答下列问题:
(1)R基态原子的电子排布式为__________,元素X、Y、Z的第一电离能由大到小的顺序为(用元素符号表示)___________________。
(2)化合物XZ3的空间构型为______,R2+与NH3形成的配离子中,提供孤对电子的是_____。
(3)Z的氢化物由固体变为气态所需克服的微粒间的作用力是________。
(4)Z、W、R形成某种化合物的晶胞结构如右图所示,其化学式为___________。
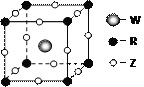
(5)XY2-能被酸性KMnO4溶液氧化,其中MnO4-被还原为Mn2+,反应的离子方程式是________________。
高三化学推断题中等难度题查看答案及解析
已知元素X、Y、Z、W、R为前四周期元素,且原子序数依次增大。X基态原子核外有三个未成对电子,Z、W分别是短周期中电负性最大和最小的元素;R2+离子的3d轨道中有三对成对电子。请回答下列问题:
(1)R基态原子的电子排布式为__________,元素X、Y、Z的第一电离能由大到小的顺序为(用元素符号表示)___________________。
(2)化合物XZ3的空间构型为______,R2+与NH3形成的配离子中,提供孤对电子的是_____。
(3)Z的氢化物由固体变为气态所需克服的微粒间的作用力是________。
(4)Z、W、R形成某种化合物的晶胞结构如右图所示,其化学式为___________。
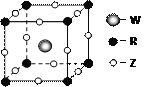
(5)XY2-能被酸性KMnO4溶液氧化,其中MnO4-被还原为Mn2+,反应的离子方程式是________________。
高三化学推断题中等难度题查看答案及解析
、
、
、
、
是元素周期表中前四周期的元素,各周期至少含有一种元素,且原子序数依次增大。
、
、
三种元素原子的最外层电子数相同,
与
能够形成原子之比为
的化合物
,
是前四周期基态原子含有未成对电子数目最多的元素,
与
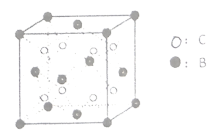
形成的晶体
结构如图所示。试用元素符号回答下列问题:
(1)、
、
三种元素的电负性由大到小的顺序为_______。
(2)与
两种元素能够形成两种常见的化合物,则在这两种化合物分子中,原子的杂化方式分别为______和______,且这两种分子____(填选项)。
A 都是极性分子 B 都是非极性分子 C 其中一种是极性分子另一种是非极性分子
(3)元素处于周期表的____区,其单质晶体堆积模型的名称为_____。
(4)元素的基态原子价层电子排布图为______。
(5)已知能溶于某浓度的硝酸中,得到蓝色溶液的同时,会逸出一种与
互为等电子体的纯净气体,则该反应的化学方程式为_____。经研究证实,所得溶液呈蓝色,是因为溶液中含有由
、
、
三种元素形成的一种配位离子,试写出该离子的结构式______。
(6)由晶体的晶胞可知,
离子呈简单立方堆积模型,形成立方体空隙,则
离子对这些立方体空隙的填充率为_____
。
高三化学综合题困难题查看答案及解析
A、B、C、D、E、F均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属元素。A是形成化合物种类最多的元素;B原子基态电子排布中只有一个未成对电子;C是同周期元素中原子半径最小的元素;D的基态原子在前四周期元素的基态原子中单电子数最多;E与D相邻,E的某种氧化物X与C的氢化物的浓溶液加热时反应常用于实验室制取气态单质C;F与D的最外层电子数相等。
回答下列问题(相关回答均用元素符号表示):
(1)D的基态原子的核外电子排布式是______________。
(2)B的氢化物的沸点比C的氢化物的沸点________(填“高”或“低”),原因是______________________。
(3)A的电负性________(填“大于”或“小于”)C的电负性,A形成的氢化物A2H4中A的杂化类型是________。
(4) X在制取C单质中的作用是________,C的某种含氧酸盐常用于实验室中制取氧气,此酸根离子中化学键的键角________(填“>”“=”或“<”)109°28′。
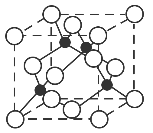
(5)已知F与C的某种化合物的晶胞结构如图所示,则该化合物的化学式是__________________,若F与C原子最近的距离为a cm,则该晶体的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的数值为NA)。
高三化学填空题困难题查看答案及解析