-
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以纯铜屑为原料制取的流程如下:
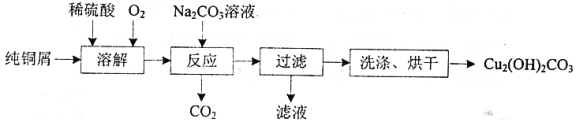
(1)“溶解”步骤反应的离子方程式为_______.温度宜控制在50℃左右,若高于50℃,溶液中O2溶解量减少、Cu的转化率降低,若低于50℃ ,_____
(2)“反应”步骤生成Cu2(OH)2CO3的化学方程式为_________。反应后溶液中铜元素残留量受pH和反应时间的影响如图所示:
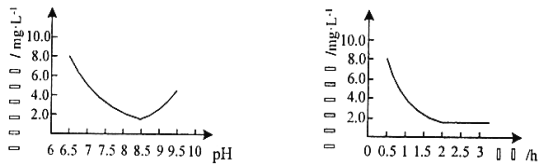
判断反应的最佳条件: pH为___、反应时间为____h。
(3)检验Cu2(OH)2CO3洗涤是否完全的方法是____________________
(4) Cu2(OH)2CO3也可以表示为CuCO3·Cu(OH)2。 查阅文献,上述反应条件下还可能生成少量CuCO3·Cu(OH)2。为测定产品的纯度[产品中Cu2(OH)2CO3的质量分数],取10.97g干燥样品,400℃左右加热,测得固体质量随时间变化关系如图所示。
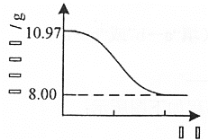
已知: 8.00g固体为黑色纯净物。
有关物质的摩尔质量如表:
| 物质 | CuCO3·Cu(OH)2 | CuCO3·2Cu(OH)2 | CuO |
| 摩尔质量/g·mol-1 | 222 | 320 | 80 |
请计算产品的纯度(写出计算过程,结果保留3位有效数字)。______
-
碱式碳酸铜是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:

步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70 ℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式___________________________________________。
(2)上图装置中NaOH溶液的作用是_________________________。
(3)步骤二中,水浴加热所需仪器有________、________(加热、夹持仪器、石棉网除外),水浴加热的优点是_______________________。
(4) 已知:CuCO3、Cu(OH)2受热均易分解,产物中都有CuO生成。碱式碳酸铜可表示为xCuCO3·yCu(OH)2·zH2O(x、y、z取整数),测定碱式碳酸铜组成的方法有多种,现采用氢气还原法,请回答如下问题:(已知M(Cu)=63.5 g·mol-1)。
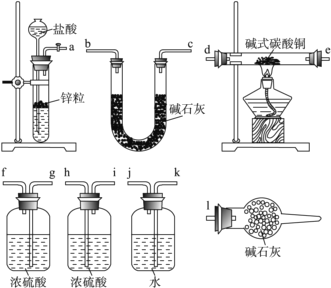
①写出xCuCO3·yCu(OH)2·zH2O与氢气反应的化学方程式:__________________;
②实验装置用上面所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):( a )→( )( )→( )( )→( )( )→( )( )→( )( )→( l )_____
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为______ g,化学式为____________。
④某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?__________(填“可行”或“不可行”)请说明理由________________________。
-
碱式碳酸铜是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
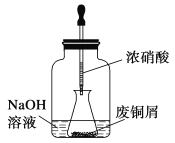
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓硝酸缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70 ℃左右,用0.4 mol·L-1的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式___________________________________________。
(2)上图装置中NaOH溶液的作用是_________________________。
(3)步骤二中,水浴加热所需仪器有________、________(加热、夹持仪器、石棉网除外),水浴加热的优点是_______________________。
(4) 已知:CuCO3、Cu(OH)2受热均易分解,产物中都有CuO生成。碱式碳酸铜可表示为xCuCO3·yCu(OH)2·zH2O(x、y、z取整数),测定碱式碳酸铜组成的方法有多种,现采用氢气还原法,请回答如下问题:(已知M(Cu)=63.5 g·mol-1)。
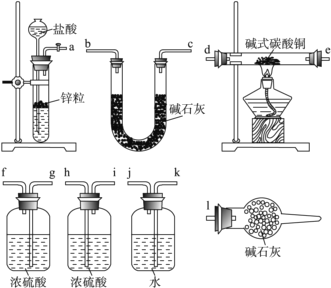
①写出xCuCO3·yCu(OH)2·zH2O与氢气反应的化学方程式:__________________;
②实验装置用上面所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):( a )→( )( )→( )( )→( )( )→( )( )→( )( )→( l )_____
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为______ g,化学式为____________。
④某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?__________(填“可行”或“不可行”)请说明理由________________________。
-
(10分)孔雀石主要成分是Cu2(OH)2CO3,还含少量难溶的FeCO3及Si的化合物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:
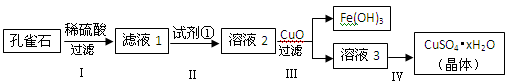
(1)步骤Ⅰ中涉及的反应用离子方程式表示为_____________________________。
(2)为将溶液中Fe2+氧化成Fe3+步骤Ⅱ中加入的试剂①最好是__________(填代号)。
a.KMnO4 b.H2O2 c.Fe粉 d.KSCN
(3)步骤Ⅳ获得硫酸铜晶体,需要经过_________、_________、过滤等操作。
(4)孔雀石与焦炭一起加热可以生成Cu及其它无毒物质,写出该反应的化学方程式_____________。
(5)测定硫酸铜晶体(CuSO4·xH2O)中结晶水的x值:称取2.5g硫酸铜晶体,加热至质量不再改变时,称量粉末的质量为1.6g。则计算得x=______
-
孔雀石的主要成分为Cu2(OH)2CO3(难溶),还含少量Fe2O3、SiO2.实验室以孔雀石为原料制备CuCl2•3H2O及CaCO3的步骤如下:

(1)写出孔雀石和盐酸反应的离子方程式 .
(2)滤渣A成分的化学式是 ,气体B的分子式是 .
(3)将CuCl2溶液酸化后,经过加热浓缩、 、过滤、洗涤、干燥,得到CuCl2•3H2O晶体.
(4)某种胃药片的治酸剂为CaCO3,该药片中CaCO3质量分数的测定步骤如下(假设其他成分不发生反应):
a.配制0.1mol•L﹣1的HCl溶液和0.1mol•L﹣1的NaOH溶液各250mL
b.取0.6g磨碎后的胃药于锥形瓶中
c.向锥形瓶内加入75.00mL 0.1mol•L﹣1的HCl溶液充分反应
d.用0.1mol•L﹣1的NaOH溶液与锥形瓶中剩余盐酸反应,恰好消耗15.00mL
①配制上述NaOH溶液所用到的玻璃仪器除烧杯、玻璃棒外还有 .
②胃药中碳酸钙的质量分数为 .
-
工业上用含有少量氧化铁杂质的废铜粉为原料,制取硫酸铜的主要过程如下图所示:
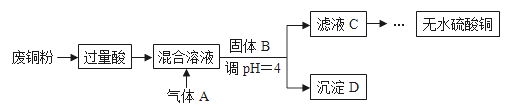
下列有关说法不正确的是
A. “过量酸”不适合用硝酸或浓硫酸,固体B可以用CuO、Cu(OH)2或Cu2(OH)2CO3
B.通入的气体A可以是O2或Cl2
C.通入气体A之前的混合溶液中存在的阳离子是:Fe2+、Cu2+、H+[
D.将从溶液中得到的硫酸铜晶体在空气中加热,可制得无水硫酸铜
-
明矾在日常生活中用途非常广泛。用废铝灰(含Al、Al2O3、Fe、Fe2O3、FeO等)为原料制取明矾的工艺流程如下图。回答下列问题:

已知:Fe3+开始沉淀到沉淀完全时溶液的pH为1.9~3.7。
(1)加快“酸溶”速率的措施有_______(列举一种即可),其中“酸溶”时,Al2O3溶解的化学方程式为_______。
(2)“氧化”时,发生反应的离子方程式为__________。
(3)“步骤①”的目的是________;检验“ 过滤2”滤液中是否含Fe3+可用试剂_________。
(4)“步骤②”包含的操作有____________、___________、过滤及干燥。
-
硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、、氧化剂和催化剂等。
(1)用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸、铜和氧化铁反应过程中属于氧化还原反应的离子方程式是________;向混合溶液中通入热空气的反应的离子方程式是____;由滤液得到无水硫酸铜的实验操作是_____________。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:
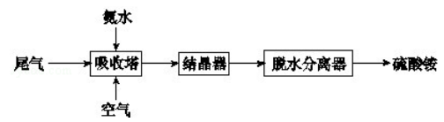
①吸收塔中发生反应的化学方程式是_____________。
②有数据表明,吸收塔中溶液的pH在5.5-6.0之间,生产效率较高。当控制一定流量的尾气时,调节溶液的pH的方法是_________________。
-
碱式碳酸铜和氯气都是用途广泛的化工原料。
(1)工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H+、Cl−)制备碱式碳酸铜,其制备过程如下:

已知:Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
①氯酸钠的作用是 ;
②反应A后调节溶液的pH范围应为 。
③第一次过滤得到的产品洗涤时,如何判断已经洗净? 。
④造成蓝绿色产品中混有CuO杂质的原因是 。
(2)某学习小组在实验室中利用下图所示装置制取氯气并探究其性质。
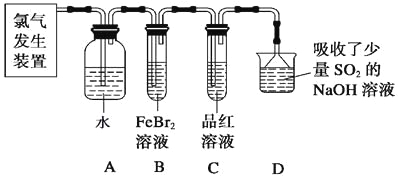
①实验室用二氧化锰和浓盐酸加热制取氯气,所用仪器需要检漏的有 。
②若C中品红溶液褪色,能否证明氯气与水反应的产物有漂白性,说明原因 。此时B装置中发生反应的离子方程式是___________ _____。
③写出A溶液中具有强氧化性微粒的化学式 。若向A溶液中加入NaHCO3粉末,会观察到的现象是 。
-
某铜矿石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以此铜矿石为原料制备CuSO4·5H2O及CaCO3,部分步骤如下:

请回答下列问题:
(1)溶液A除含有Cu2+外,还可能含有的金属离子有________(填离子符号);在溶液A中加入H2O2反应的离子方程式是______________。
(2)可用生成的CO2制取优质碳酸钙。制备时,先向氯化钙溶液中通入氨气,再通入CO2。
①实验室通常采用加热氯化铵和氢氧化钙混合物的方法制取氨气。某学习小组选取下图所给部分装置制取并收集纯净的氨气。
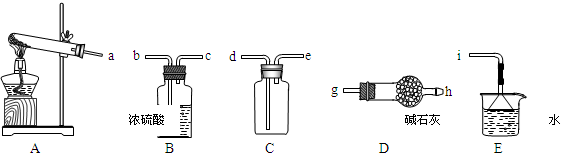
如果按气流方向连接各仪器接口,你认为正确的顺序为a→______、______→______、______→ i。其中与i相连漏斗的作用是______________。
②实验室中还可用固体氢氧化钠和浓氨水制取少量氨气,下列最适合完成该实验的简易装置是
_________(填编号)

(3)测定铜矿石中Cu2(OH)2CO3质量百分含量的方法是:a.将1.25g铜矿石制取的CuSO4·5H2O于锥形瓶中,加入适量水完全溶解;b.向溶液中加入100mL0.25mol/L的氢氧化钠溶液使Cu2+完全沉淀;c.过滤;d.滤液中的氢氧化钠溶液用0.5mol/L盐酸滴定至终点,耗用10mL盐酸。则铜矿石中Cu2(OH)2CO3质量分数为_____________。

















