-
为了测定实验室长期存放的Na2SO3固体的纯度,准确称取Wg固体样品,配成250mL溶液。设计了以下两种实验方案:
方案Ⅰ:取25.00mL上述溶液,加入足量的用过量盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1g。
方案Ⅱ:取25.00mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2g。
(1)配制250mLNa2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、天平、药匙、_______、______。
(2)写出Na2SO3固体氧化变质的化学方程式______________。
(3)方案Ⅰ加入过量的盐酸酸化的BaCl2溶液,目的是___________,在过滤前,需要检验是否沉淀完全,其操作是______________。
(4)方案Ⅰ中,若滤液浑浊,将导致测定结果____________(填“偏高”或“偏低”)。
(5)若操作正确,结果为m1<m2,试分析原因是_________。
(6)取25.00mL上述溶液,用cmol/L酸性KMnO4溶液滴定测定Na2SO3的纯度,已知酸性条件下,KMnO4通常被还原为Mn2+滴定达到终点时的现象为___________,若达到滴定终点时用去VmL KMnO4溶液,则Na2SO3固体的纯度表达式为______。
高二化学实验题中等难度题查看答案及解析
-
为了测定实验室长期存放的Na2SO3固体的纯度,准确称取W g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案Ⅰ:取25.00 mL上述溶液,加入足量的用过量盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1 g。
方案Ⅱ:取25.00 mL上述溶液,加入过量的盐酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2 g。
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、天平、药匙、______、______。
(2)写出Na2SO3固体氧化变质的化学方程式__________。
(3)方案Ⅰ加入过量的盐酸酸化的BaCl2溶液,目的是________,在过滤前,需要检验是否沉淀完全,其操作是_______。
(4)方案Ⅰ中,若滤液浑浊,将导致测定结果_______(填“偏高”或“偏低”)。
(5)若操作正确,结果为m1<m2,试分析原因是___________。
(6)取25.00 mL上述溶液,用c mol/L酸性KMnO4溶液滴定测定Na2SO3的纯度,已知酸性条件下,KMnO4通常被还原为Mn2+,滴定达到终点时的现象为____________。
高二化学实验题中等难度题查看答案及解析
-
为了测定实验室长期存放的Na2SO3固体的纯度,准确称取w g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取25.00 mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取25.00 mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定。(5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O)
滴定次数实验数据
1
2
3
4
待测溶液体积/mL
25.00
25.00
25.00
25.00
滴定管初读数/mL
0.00
0.20
0.10
0.15
滴定管末读数/mL
19.95
20.20
19.15
20.20
实验中所记录的数据如下表:
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻璃棒、胶头滴管、量筒、药匙和_________、____________。
(2)操作I为________操作Ⅱ为____________
(3)方案I中如何判断加入的氯化钡已经过量_____________,在方案Ⅱ中滴定终点的判断方法是________________。
(4)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为_________。
(5)上述实验中,由于操作错误所引起的误差分析正确的是_________
A.方案I中若没有洗涤操作,实验结果将偏小
B.方案I中若没有操作Ⅱ,实验结果将偏大
C.方案Ⅱ中,滴定管在滴定前无气泡,滴定后出现气泡,实验结果偏小
D.方案Ⅱ中,滴定终点时仰视读数,实验结果偏大
高二化学实验题中等难度题查看答案及解析
-
为了测定实验室长期存放的Na2SO3固体的纯度,准确称取M g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取50.00 mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取50.00 mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定。
实验中所记录的数据如下表:
滴定次数
实验数据
1
2
3
4
待测溶液体积/mL
50.00
50.00
50.00
50.00
滴定管初读数/mL
0.00
0.20
0.10
0.15
滴定管末读数/mL
20.95
21.20
20.15
21.20
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、滴管、药匙和_______________、_________________。
(2)操作I为__________________操作Ⅱ为______________
(3)在方案Ⅱ中滴定终点的判断方法是_______________________________。
(4) 在方案Ⅱ中发生的离子反应方程式为__________________________
(5)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为___________。(写成分数形式)
(6)有同学提出方案Ⅲ,取50.00mL上述溶液→加入足量的盐酸酸化的硝酸钡溶液→操作I→洗涤→操作Ⅱ→称重,则上述实验中,由于操作错误所引起的实验误差分析正确的是__________(填序号)。
a.方案I中如果没有洗涤操作,实验结果将偏小
b.方案I中如果没有操作Ⅱ,实验结果将偏大
c.方案Ⅲ中如果没有洗涤操作,实验结果将偏小
d.方案Ⅲ中如果没有操作Ⅱ,实验结果将偏大
高二化学实验题中等难度题查看答案及解析
-
为了测定实验室长期存放的Na2SO3固体的纯度,准确称取M g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取50.00 mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取50.00 mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定。
实验中所记录的数据如下表:
滴定次数
实验数据
1
2
3
4
待测溶液体积/mL
50.00
50.00
50.00
50.00
滴定管初读数/mL
0.00
0.20
0.10
0.15
滴定管末读数/mL
20.95
21.20
20.15
21.20
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、滴管、药匙和_______、________。
(2)操作I为______________,操作Ⅱ为______________。
(3)在方案Ⅱ中滴定终点的判断方法是_______________________________。
(4)在方案Ⅱ中发生的离子反应方程式为____________________________。
(5)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为___________。(写成分数形式)
(6)方案Ⅱ中氧化还原滴定过程中,导致待测液Na2SO3浓度变小的是_____(填序号)。
a.用碱式滴定管量取50mL待测液过程时,开始仰视,滴定结束时俯视
b.用碱式滴定管量取50mL待测液过程时,一开始有气泡,滴定结束后没气泡
c.酸式滴定管用蒸馏水润洗后,没有用酸性KMnO4溶液多次润洗
d.锥形瓶用蒸馏水润洗后,直接装50.00mL的待测液
e.滴定过程时,开始时平视,滴定结束时仰视
高二化学实验题中等难度题查看答案及解析
-
某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在天平上准确称取烧碱样品wg,在烧坏中加蒸馏水溶解
B.在250mL容量瓶中定量成250mL烧碱溶液
C.用移液管移取25.00 mL烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂
D.将物质的量浓度为 Cmol/L 的标准盐酸 溶液装入酸式滴定管,调整液面,记下开始刻度数为Vml
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点耗酸体积 V1ml
回答下列问题:
(1)操作中的雏形瓶下垫一张白纸的作用是__________________。
(2)操作中液面应调整到零刻度或零刻度以下(稍下)的某一刻度,尖嘴部分应___________。
(3)滴定终点时锥形瓶内溶液颜色变化是__________。
(4)若酸式滴定管没有用标准 润洗,会对测定结果有何影响_____________(填偏高、偏低或无影响,其他操作均正确)。
(5)该烧碱样品的纯度计算式是_____________。
高二化学实验题简单题查看答案及解析
-
I.某烧碱样品含有少量不与酸作用的杂质,为了测定其纯度,进行以下操作:
A.在250 mL的容量瓶中准确配制250 mL烧碱溶液
B.用碱式滴定管移取25 mL烧碱溶液于锥形瓶中并滴入2滴甲基橙指示剂
C.在天平上准确称取烧碱样
品m g,在烧杯中用蒸馏水溶解
D.将浓度为c mol·L-1的标准硫酸装入酸式滴定管,调整液面记下开始读数V1
E.在锥形瓶下垫一张白纸,滴定至橙色为止,记下读数V2
就此实验完成下列填空:
(1)正确的操作步骤的顺序是(用编号字母填写):________________。
(2)下列操作中可能使所测NaOH的质量分数偏低的是__________。
a.滴定操作中,锥形瓶残留少量蒸馏水
b.B步操作中,装入烧碱溶液之前未用待测液润洗
c.D步操作中酸式滴定管在装入标准H2SO4溶液前未用标准液润洗
d.读取硫酸体积时,开始时仰视读数,结束时俯视读数
(3)该烧碱样品纯度的计算式为______________________。
II.以下是FeSO4·7H2O的实验窒制备流理图。
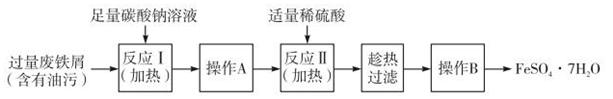
根据题意完成下列填空:
(1)反应1需要加热数分钟,其原因是 ;操作A为 。
(2)测定FeSO4·7H2O产品中Fe2+含量的常用方法是KMnO4溶液滴定法。已知称取3.0g FeSO4·7H2O产品,配制成溶液,用硫酸酸化的0.01moL·L-1 KMnO4溶液滴定,消耗KMnO4溶液的体积为200.00mL。KMnO
4溶液应盛装在 滴定管中,发生反应的离子方程式为 ,计算上述样品中FeSO4·7H2O的质量分数为 (保留两位有效数字)。[
高二化学实验题困难题查看答案及解析
-
化学兴趣小组用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
①称量1.0 g样品溶于水,配成250mL溶液;
②用碱式滴定管准确量取25.00mL所配溶液于锥形瓶中,滴加2~3滴酚酞溶液;
③用0.1000 mol·L-1的标准盐酸滴定并重复三次,每次实验数据记录如下:
滴定次数
待测液体积/mL
所消耗盐酸标准溶液的体积/mL
滴定前
滴定后
1
25.00
1.50
21.40
2
25.00
2.50
22.60
3
25.00
0.60
23.20
(1)称量时,样品应放在________称量(选填字母序号)。
a.小烧杯中 b.洁净纸片上 c.托盘上
(2)如图是某次滴定时的滴定管中的液面,其读数为________mL。
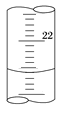
(3)判断滴定终点到达时的现象为_______________________________。
(4)若出现下列情况,测定结果偏高的是________(选填字母序号)。
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管在滴定前有气泡,滴定后气泡消失
(5)通过计算可知该烧碱样品的纯度为________。(杂质不与酸反应)。
高二化学实验题中等难度题查看答案及解析
-
某学生为了测定部分变质的Na2SO3样品的纯度,设计了如图实验,回答下列问题:
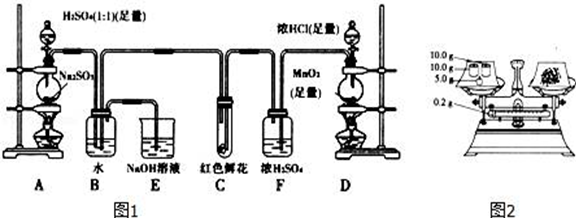
(1)写出A装置中玻璃仪器的名称:酒精灯__________________
(2)实验开始后,写出B中反应的离子方程式__________________
(3)E装置的作用是__________________
(4)按图2所示称取一定量的Na2SO3样品放入A装置的烧瓶中,滴入足量的H2SO4完全反应.然后将B中完全反应后的溶液与足量的BaCl2溶液反应,过滤、洗涤、干燥,得白色沉淀23.3g,则样品中Na2SO3的纯度为__________________(精确到0.1%)
(5)在过滤沉淀时若滤液出现浑浊,则必须要重复操作,若该学生没有重复过滤,则测定的结果将__________________
(6)要使测定结果准确,第一:装置气密性必须良好;第二:应先点燃__________________处酒精灯(填装置字母).
高二化学实验题中等难度题查看答案及解析
-
某纯碱样品中含有少量氯化钠,现欲测定其碳酸钠的质量分数,设计如下实验方案:
(方案1)称取一定质量的纯碱样品(已知锥形瓶和硫酸溶液的质量190.720 g),利用左图装置测定纯碱样品的纯度,每隔相同时间读得电子天平的数据如表:
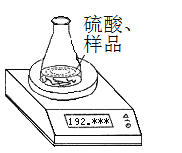
读数次数
质量(g)
锥形瓶+硫酸+试样
第1次
192.955
第2次
192.764
第3次
192.328
第4次
192.075
第5次
192.075
(1)计算纯碱样品的纯度时,必需的数据是_____________________________(填具体数据)。不必作第6次读数的原因是________________________________________________。
(2)计算纯碱样品的纯度为_________________________(保留小数后两位)。
(方案2)测定上述样品(1.15 g)中,Na2CO3质量分数的另一种方案,其操作流程如下:
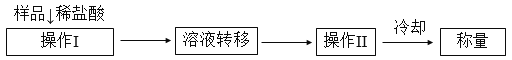
(1)溶液转移至__________(填写仪器名称),操作II的名称是______________。
(2)需直接测定的物理量是____________________。
(3)测定过程中需要的仪器有电子天平.蒸发皿、酒精灯、还需要__________、__________(固定、夹持仪器除外)。
(4)在转移溶液时,如溶液转移不完全,则Na2CO3质量分数的测定结果__________(填“偏小”、“偏大”或“不变”)
(方案3)实验装置如图:
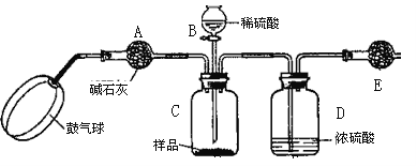
实验步骤:
①如图连接装置并加入所需药品。
②称量并记录E的质量m1(称量时注意封闭E的两端)。
③按动鼓气球,持续约1分钟。
④连接上E。
⑤打开分液漏斗B的活塞,将稀硫酸快速加入C中后,关闭活塞。
⑥按动鼓气球,持续约1分钟。
⑦称量并记录E的质量m2(称量时注意封闭E的两端及D右端的出口)。
⑧重复步骤⑥和⑦的操作,直到球形干燥管的质量基本不变,记为m3。
⑨计算。
请填空和回答问题:
(1)C中发生反应的离子方程式为:______________________________________。B仪器的名称为__________。如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果将__________(填“偏高”、“偏低”或“不变”)。
(2)浓硫酸的作用是_________________,若没有D,则实验结果__________(填“偏高”、“偏低”或“无影响”)。
(3)步骤③和⑥的作用是____________________,____________________。鼓气球的速度是快速好,还是缓慢鼓入?为什么?__________________________________________。
(4)E装置的固体试剂为__________(填编号)
A.碱石灰 B.无水氯化钙 C.浓硫酸 D.生石灰
(5)步骤⑧的目的是________________________________________________。
(6)试样中纯碱样品的质量分数计算式为_____________________________________。
(7)本实验设计中若有需要改进的地方,请指出该进之处并说明原因。
_______________________________________________________________________。
(8)实验还可以用其它定量实验方法测定试样中纯碱的质量分数,请简述一种不同的定量实验方法。___________________________________________________________ 。
高二化学实验题中等难度题查看答案及解析